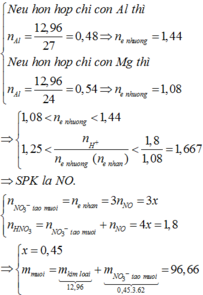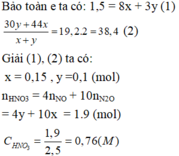Cho FexOy tác dụng vừa đủ với HNO3 tạo ra 0,08 mol NO(sản phẩm khử duy nhất và dung dịch X chứa 58,08 gam muối .Xác định FexOy.

Những câu hỏi liên quan
Nung hỗn hợp X gồm Al và FexOy trong khí trơ, thu được 22,88 gam rắn Y gồm Al2O3, Al, Fe và FexOy. Cho toàn bộ Y vào dung dịch NaOH loãng dư, thu được 0,12 mol khí H2 và m gam rắn Z. Hòa tan hết m gam Z trong dung dịch chứa 0,72 mol HNO3, thu được 0,08 mol khí NO (sản phẩm khử duy nhất của N+5) và dung dịch chứa 53,12 gam muối. Công thức của FexOy và khối lượng của Al2O3 trong Y là: A. Fe2O3 và 4,08 gam B. Fe3O4 và 6,12 gam C. Fe3O4 và 4,08 gam D. Fe2O3 và 6,12 gam
Đọc tiếp
Nung hỗn hợp X gồm Al và FexOy trong khí trơ, thu được 22,88 gam rắn Y gồm Al2O3, Al, Fe và FexOy. Cho toàn bộ Y vào dung dịch NaOH loãng dư, thu được 0,12 mol khí H2 và m gam rắn Z. Hòa tan hết m gam Z trong dung dịch chứa 0,72 mol HNO3, thu được 0,08 mol khí NO (sản phẩm khử duy nhất của N+5) và dung dịch chứa 53,12 gam muối. Công thức của FexOy và khối lượng của Al2O3 trong Y là:
A. Fe2O3 và 4,08 gam
B. Fe3O4 và 6,12 gam
C. Fe3O4 và 4,08 gam
D. Fe2O3 và 6,12 gam
Nung hỗn hợp X gồm Al và FexOy trong khí trơ, thu được 22,88 gam rắn Y gồm Al2O3, Al, Fe và FexOy. Cho toàn bộ Y vào dung dịch NaOH loãng dư, thu được 0,12 mol khí H2 và m gam rắn Z. Hòa tan hết m gam Z trong dung dịch chứa 0,72 mol HNO3, thu được 0,08 mol khí NO (sản phẩm khử duy nhất của N+5) và dung dịch chứa 53,12 gam muối. Công thức của FexOy và khối lượng của Al2O3 trong Y là A. Fe2O3 và 6,12 gam B. Fe3O4 và 6,12 gam C. Fe3O4 và 4,08 gam D. Fe2O3 và 4,08 gam
Đọc tiếp
Nung hỗn hợp X gồm Al và FexOy trong khí trơ, thu được 22,88 gam rắn Y gồm Al2O3, Al, Fe và FexOy. Cho toàn bộ Y vào dung dịch NaOH loãng dư, thu được 0,12 mol khí H2 và m gam rắn Z. Hòa tan hết m gam Z trong dung dịch chứa 0,72 mol HNO3, thu được 0,08 mol khí NO (sản phẩm khử duy nhất của N+5) và dung dịch chứa 53,12 gam muối. Công thức của FexOy và khối lượng của Al2O3 trong Y là
A. Fe2O3 và 6,12 gam
B. Fe3O4 và 6,12 gam
C. Fe3O4 và 4,08 gam
D. Fe2O3 và 4,08 gam
Đáp án C
Cho Y tác dụng với NaOH loãng dư thu được 0,12mol H2 do vậy Y chứa 0,08 mol Al.
Rắn Z thu được gồm Fe và FexOy.
Hòa tan hết Z trong 0,72 mol HNO3 thu được 0,08 mol NO và 53,12 gam muối.
Bảo toàn N: n N O 3 - t r o n g m u o i = 0 , 72 - 0 , 08 = 0 , 64 m o l
Bảo toàn e:
n O t r o n g Z = 0 , 64 - 0 , 08 . 3 2 = 0 , 2 m o l → m = 0 , 2 . 16 + 0 , 24 . 56 = 16 , 64 g a m
Trong Y: m A l 2 O 3 = 22 , 88 - 16 , 64 - 0 , 08 . 27 = 4 , 08
→ n A l 2 O 3 = 0 , 04 m o l
Bảo toàn O: n O t r o n g Z = 0 , 2 + 0 , 04 . 3 = 0 , 32
Vậy: x : y = 0,24 : 0,32 = 3:4 nên oxi là Fe3O4.
Đúng 0
Bình luận (0)
Nung hỗn hợp X gồm Al và FexOy trong khí trơ, thu được 22,88 gam rắn Y gồm Al2O3, Al, Fe và FexOy. Cho toàn bộ Y vào dung dịch NaOH loãng dư, thu được 0,12 mol khí H2 và m gam rắn Z. Hòa tan hết m gam Z trong dung dịch chứa 0,72 mol HNO3, thu được 0,08 mol khí NO (sản phẩm khử duy nhất của N+5) và dung dịch chứa 53,12 gam muối. Công thức của FexOy và khối lượng của Al2O3 trong Y là A. Fe2O3 và 6,12 gam. B. Fe3O4 và 6,12 gam. C. Fe3O4 và 4,08 gam. D. Fe2O3 và 4,08 gam.
Đọc tiếp
Nung hỗn hợp X gồm Al và FexOy trong khí trơ, thu được 22,88 gam rắn Y gồm Al2O3, Al, Fe và FexOy. Cho toàn bộ Y vào dung dịch NaOH loãng dư, thu được 0,12 mol khí H2 và m gam rắn Z. Hòa tan hết m gam Z trong dung dịch chứa 0,72 mol HNO3, thu được 0,08 mol khí NO (sản phẩm khử duy nhất của N+5) và dung dịch chứa 53,12 gam muối. Công thức của FexOy và khối lượng của Al2O3 trong Y là
A. Fe2O3 và 6,12 gam.
B. Fe3O4 và 6,12 gam.
C. Fe3O4 và 4,08 gam.
D. Fe2O3 và 4,08 gam.
Đáp án C
Cho Y tác dụng với NaOH loãng dư thu được 0,12mol H2 do vậy Y chứa 0,08 mol Al.
Rắn Z thu được gồm Fe và FexOy.
Hòa tan hết Z trong 0,72 mol HNO3 thu được 0,08 mol NO và 53,12 gam muối.
Bảo toàn N:
![]()
Bảo toàn e:
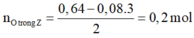
![]()
Trong Y: ![]()
Bảo toàn O:
![]()
Vậy: x : y = 0,24 : 0,32 = 3:4 nên oxi là Fe3O4.
Đúng 0
Bình luận (0)
Cho 12,96 gam hỗn hợp Al và Mg tác dụng vừa đủ với dung dịch chứa 1,8 mol HNO3 tạo ra sản phẩm khử X duy nhất. Làm bay hơi dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là: A. 96,66. B. 116,64. C. 105,96. D. 102,24.
Đọc tiếp
Cho 12,96 gam hỗn hợp Al và Mg tác dụng vừa đủ với dung dịch chứa 1,8 mol HNO3 tạo ra sản phẩm khử X duy nhất. Làm bay hơi dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là:
A. 96,66.
B. 116,64.
C. 105,96.
D. 102,24.
Cho 12,96 gam hỗn hợp Al và Mg tác dụng vừa đủ với dung dịch chứa 1,8 mol HNO3 tạo ra sản phẩm khử X duy nhất. Làm bay hơi dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là A. 96,66 B. 116,64 C. 105,96 D. 102,24
Đọc tiếp
Cho 12,96 gam hỗn hợp Al và Mg tác dụng vừa đủ với dung dịch chứa 1,8 mol HNO3 tạo ra sản phẩm khử X duy nhất. Làm bay hơi dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là
A. 96,66
B. 116,64
C. 105,96
D. 102,24
Cho 12,96 gam hỗn hợp Al và Mg tác dụng vừa đủ với dung dịch chứa 1,8 mol HNO3 tạo ra sản phẩm khử X duy nhất. Làm bay hơi dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là A. 96,66 B. 116,64 C. 105,96 D. 102,24
Đọc tiếp
Cho 12,96 gam hỗn hợp Al và Mg tác dụng vừa đủ với dung dịch chứa 1,8 mol HNO3 tạo ra sản phẩm khử X duy nhất. Làm bay hơi dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là
A. 96,66
B. 116,64
C. 105,96
D. 102,24
Đáp án A
X là NO
=> nNH4NO3 = ¼ nHNO3 = 0,45 mol và nNO3 muối KL = nHNO3 – nNO = 1,35 mol
=> mmuối = mKL + mNO3 muối KL = 96,66g
Đúng 0
Bình luận (0)
Cho 12,96 gam hỗn hợp Al và Mg tác dụng vừa đủ với dung dịch chứa 1,8 mol HNO3 tạo ra sản phẩm khử X duy nhất. Làm bay hơi dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là A. 102,24 B. 116,64. C. 105,96. D. 96,66.
Đọc tiếp
Cho 12,96 gam hỗn hợp Al và Mg tác dụng vừa đủ với dung dịch chứa 1,8 mol HNO3 tạo ra sản phẩm khử X duy nhất. Làm bay hơi dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là
A. 102,24
B. 116,64.
C. 105,96.
D. 96,66.
Đáp án D
+ N ế u h ỗ n h ợ p c h ỉ c ó A l t h ì n A l = 12 , 96 27 = 0 , 48 ⇒ n e n h ư ờ n g = 1 , 44 N ế u h ỗ n h ợ p c h ỉ c ó M g t h ì n A l = 12 , 96 24 = 0 , 54 ⇒ n e n h ư ờ n g = 1 , 08 ⇒ 1 , 08 < n e n h ư ờ n g g < 1 , 44 1 , 8 1 , 44 = 1 , 25 < n H + n e n h ư ờ n g ( n e n h ậ n ) < 1 , 8 1 , 08 = 1 , 667 ⇒ S P K l à N O . + n N O 3 - t ạ o m u ố i = n e n h ậ n = 3 n N O = 3 x n H N O 3 = n N O 3 - t ạ o m u ố i + n N O = 4 x = 1 , 8 ⇒ x = 0 , 45 m m u ố i = m k i m l o ạ i ⏟ 12 , 96 + m N O 3 - t a ọ m u ố i ⏟ 0 , 45 . 3 . 62 = 96 , 66
Bảng mối liên hệ giữa n H + n e l e c t r o n n h ậ n và sản phẩm khử:
| 2 H + + N O 3 - + 1 e → N O 2 + H 2 O |
n H + n e l e c t r o n n h ậ n = 2 |
| 4 H + + N O 3 - + 3 e → N O + 2 H 2 O |
n H + n e l e c t r o n n h ậ n = 1 , 333 |
| 10 H + + 2 N O 3 - + 8 e → N 2 O + 5 H 2 O |
n H + n e l e c t r o n n h ậ n = 1 , 25 |
| 12 H + + 2 N O 3 - + 10 e → N 2 + 6 H 2 O |
n H + n e l e c t r o n n h ậ n = 1 , 2 |
| 10 H + + N O 3 - + 8 e → N H 4 + + 3 H 2 O |
n H + n e l e c t r o n n h ậ n = 1 , 25 |
Đúng 0
Bình luận (0)
Cho 2,8 gam bột sắt tác dụng hoàn toàn với V mL dung dịch HNO3 0,5M thu được sản phẩm khử NO duy nhất và dung dịch X. X có thể tác dụng vừa đủ với dung dịch chứa 0,03 mol AgNO3. Giá trị của V là A. 420. B. 340 C. 320. D. 280
Đọc tiếp
Cho 2,8 gam bột sắt tác dụng hoàn toàn với V mL dung dịch HNO3 0,5M thu được sản phẩm khử NO duy nhất và dung dịch X. X có thể tác dụng vừa đủ với dung dịch chứa 0,03 mol AgNO3. Giá trị của V là
A. 420.
B. 340
C. 320.
D. 280
Cho 13,5 gam nhôm tác dụng vừa đủ với 2,5 lít dung dịch HNO3, phản ứng tạo ra muối nhôm và một hỗn hợp khí gồm NO và N2O(là sản phẩm khử duy nhất). Tính nồng độ mol của dung dịch HNO3. Biết rằng tỉ khối của hỗn hợp khí đối với hiđro bằng 19,2. A. 0,95 B. 0,86 C. 0,76 D. 0,9
Đọc tiếp
Cho 13,5 gam nhôm tác dụng vừa đủ với 2,5 lít dung dịch HNO3, phản ứng tạo ra muối nhôm và một hỗn hợp khí gồm NO và N2O(là sản phẩm khử duy nhất). Tính nồng độ mol của dung dịch HNO3. Biết rằng tỉ khối của hỗn hợp khí đối với hiđro bằng 19,2.
A. 0,95
B. 0,86
C. 0,76
D. 0,9