trong tự nhiên bo có 2 đồng vị là 105 B và 115 B. khối lượng nguyên tử trung bình của bo là 10,82u. tính hàm lượng % số nguyên tử của đồng vị 11 b

Những câu hỏi liên quan
rong tự nhiên Bo có 2 đồng vị là 10B và 11B. Khối lượng nguyên tử trung bình của Bo là 10,82u. Mỗi khi có 73 nguyên tử 10B thì có bao nhiêu nguyên tử 11B ???
x là phần trăm của 10B.
Khối lượng trung bình 10,82= \(\frac{10x+11\left(100-x\right)}{100}\)
Tính ra %10B = 18%. %11B= 82%.
Tỉ lệ \(\frac{\%10B}{\%11B}=\frac{9}{41}\)
Từ tỉ lệ này tính thì 73 nguyên tử 10B có \(\frac{73\cdot41}{9}\simeq332.5\) nguyên tử 11B.
Thế kết quả vào kiểm tra lại Khối lượng trung bình của B là 10,8199 .
Chúc bạn học học tốt![]()
Đúng 0
Bình luận (1)
Trong thiên nhiên nguyên tố Bo có 2 đồng vị, biết một loại đồng vị là chiếm 80%. Tìm số khối của đồng vị thứ hai biết khối lượng nguyên tử trung bình của Bo là 10,8. A. 14. B. 12. C. 10. D. 13.
trong tự nhiên Bo có 2 đồng vị là 10B và 11B. Khối lượng nguyên tử trung bình của Bo là 110,82u. Mỗi khi có 73 nguyên tử 10B thì có bao nhiêu nguyên tử 11B ???
Trong tự nhiên, nguyên tố bo có 2 đồng vị: B 11 , nguyên tử khối coi là bằng 11, thành phần 80,1% ; B 10 nguyên tử khối coi là bằng 10, thành phần 19,9%. Hãy tính nguyên tử khối trung bình của nguyên tố bo trong tự nhiên.
Nguyên tử khối trung bình A của nguyên tố bo trong tự nhiên :
![]()
Nguyên tử khối trung bình của nguyên tố bo : 10,8.
Đúng 0
Bình luận (0)
Bài 3. Nguyên tố Bo có 2 đồng vị: 10 5B và 11 5B. Nguyên tử khối trung bình của Bo là 10,812. a. Tính phần trăm số nguyên tử mỗi loại đồng vị. b. Mỗi khi có 94 nguyên tử 10 5B thì có bao nhiêu nguyên tử 11 5B ?
tìm số khối của đồng vị thứ hai của các nguyên tố sau:
a/ nguyên tử trung bình của Bạc là 107,88.Bạc có hai đồng vị, trong đó Bạc 109 Ag chiếm 44%
b/nguyên tử khối trung bình của Bo là 10,812.Bo có hai đồng vị, trong đó đồng vị 10 5 B chiếm 18,8%
a)
\(\overline{NTK}_{Ag}=107,88\\ \Leftrightarrow\dfrac{109.44\%+A_2.56\%}{100\%}=107,88\\ \Leftrightarrow A_2=107\left(đ.v.C\right)\)
b)
\(\overline{NTK}_B=10,812\\ \Leftrightarrow\dfrac{10.18,8\%+A_2.81,2\%}{100\%}=10,812\\ \Leftrightarrow A_2=11\left(đ.v.C\right)\)
Đúng 2
Bình luận (0)
Tính nguyên tử khối trung bình của các nguyên tố. Biết rằng trong tự nhiên, đồng vị của các nguyên tố này tồn tại theo số liệu sau:a) Bo có 2 đồng vị:dfrac{10}{5}Bleft(18,89%right);dfrac{11}{5}Bleft(81,11%right)b) Ne có 2 đồng vị:dfrac{20}{10}Neleft(91%right);dfrac{22}{10}Nec) Br có 2 đồng vị 79Br (54,5%) và 81Brd) Mg có 3 đồng vị: dfrac{24}{12}Mg(78,99%); dfrac{25}{12}Mg(10,00%) , còn lại làdfrac{26}{12}Mge) rgon có 3 đồng vị: dfrac{36}{18}Ar(0,34%); dfrac{38}{18}Arleft(0,06%right);dfrac{40}{18...
Đọc tiếp
Tính nguyên tử khối trung bình của các nguyên tố. Biết rằng trong tự nhiên, đồng vị của các nguyên tố này tồn tại theo số liệu sau:
a) Bo có 2 đồng vị:\(\dfrac{10}{5}B\left(18,89\%\right);\dfrac{11}{5}B\left(81,11\%\right)\)
b) Ne có 2 đồng vị:\(\dfrac{20}{10}Ne\left(91\%\right);\dfrac{22}{10}Ne\)
c) Br có 2 đồng vị 79Br (54,5%) và 81Br
d) Mg có 3 đồng vị: \(\dfrac{24}{12}Mg\)(78,99%); \(\dfrac{25}{12}Mg\)(10,00%) , còn lại là\(\dfrac{26}{12}Mg\)
e) rgon có 3 đồng vị: \(\dfrac{36}{18}Ar\)(0,34%); \(\dfrac{38}{18}Ar\left(0,06\%\right);\dfrac{40}{18}Ar\)
f) Sắt (Fe) có 4 đồng vị 54Fe (5,84%), 56Fe (91,68%), 57Fe (2,17%), 58Fe (0,31%).
\(a,\overline{NTK}_B=\dfrac{10.18,89\%+11.81,11\%}{100\%}=10,8111\left(đ.v.C\right)\\ b,\overline{NTK}_{Ne}=\dfrac{20.91\%+22.\left(100\%-91\%\right)}{100\%}=20,18\left(đ.v.C\right)\\ c,\overline{NTK}_{Br}=\dfrac{79.54,5\%+81.\left(100\%-54,5\%\right)}{100\%}=79,91\left(đ.v.C\right)\\ d,\overline{NTK}_{Mg}=\dfrac{24.78,99\%+25.10\%+26.\left(100\%-78,89\%-10\%\right)}{100\%}\\ =24,3202\left(đ.v.C\right)\)
\(e,\overline{NTK}_{Ar}=\dfrac{36.0,34\%+38.0,06\%+40.\left(100\%-0,34\%+0,06\%\right)}{100\%}\\ =39,9852\left(đ.v.C\right)\\ f,\overline{NTK}_{Fe}=\dfrac{54.5,84\%+56.91,68\%+57.2,17\%+58.0,31\%}{100\%}\\ =55,9111\left(đ.v.C\right)\)
Đúng 2
Bình luận (2)
Trong tự nhiên Bo có 2 đồng vị là B 11 (81%) và B 10 (19%). Nguyên tử khối trung bình của Bo là:
A. 81
B. 19
C. 10,18
D. 10,81
Chọn D
Nguyên tử khối trung bình của Bo là:
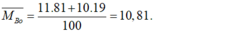
Đúng 0
Bình luận (0)
trong tự nhiên, nguyên tố clo có 2 đồng vị là 35Cl và 37Cl. Nguyên tử khối trung bình của Clo bằng 35,5. a) Tính phần trăm số nguyên tử của mỗi đồng vị trên?
b tính % khối lượng của cl35 có trong phân tử HCLO4 biết NTKtb của H+1 o=16,2














