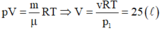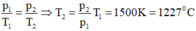Một bình kín chứa 1mol Nito ở áp suất 105 N/m2 , nhiệt độ 300K . Thể tích bình xấp xỉ bằng bao nhiêu ?

Những câu hỏi liên quan
Một bình kín chứa 1 mol khí nitơ ở áp suất
10
5
N
/
m
2
ở
27
°
C
Thể tích của bình xấp xỉ bằng bao nhiêu? A. 2,5l B. 2,8 l C. 25 l D. 27,7 l
Đọc tiếp
Một bình kín chứa 1 mol khí nitơ ở áp suất 10 5 N / m 2 ở 27 ° C
Thể tích của bình xấp xỉ bằng bao nhiêu?
A. 2,5l
B. 2,8 l
C. 25 l
D. 27,7 l
Đáp án C.
Ta có: p V = m μ R T ⇒ V = ν R T p 1 = 25 l
Đúng 0
Bình luận (0)
Một bình kín chứa 1 moi khí nitơ ở áp suất
10
5
N
/
m
2
ở
27
°
C. Thể tích của bình xấp xỉ bằng bao nhiêu? A. 2,5ℓ B. 2,8 ℓ C. 25 ℓ D. 27,7 ℓ
Đọc tiếp
Một bình kín chứa 1 moi khí nitơ ở áp suất 10 5 N / m 2 ở 27 ° C. Thể tích của bình xấp xỉ bằng bao nhiêu?
A. 2,5ℓ
B. 2,8 ℓ
C. 25 ℓ
D. 27,7 ℓ
Một bình kín chứa một lượng khí Nito xác định ở áp suất 105 N/m , nhiệt độ 27 độ C . Nung bình đến khi áp suất khí là 5.105 N/m2 . Nhiệt độ khí sau khi nung nóng là
Trạng thái 1: \(\left\{{}\begin{matrix}p_1=10^5Pa\\T_1=27^oC=300K\end{matrix}\right.\)
Trạng thái 2: \(\left\{{}\begin{matrix}p_2=5\cdot10^5Pa\\T_2=???\end{matrix}\right.\)
Quá trình đẳng tích:
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\Rightarrow\dfrac{10^5}{300}=\dfrac{5\cdot10^5}{T_2}\)
\(\Rightarrow T_2=1500K=1227^oC\)
Đúng 3
Bình luận (0)
Một bình hình trụ đặt thẳng đứng có dung tích 8 lít và đường kính trong 20 cm, được đậy kín bằng một nắp có khối lượng 2 kg. Trong bình chứa khí ở nhiệt độ
100
°
C dưới áp suất bằng áp suất khí quyển (
10
5
N/
m
2
). Khi nhiệt độ trong bình giảm xuống còn 20
°
C thì: Áp suất khí trong bình bằng bao...
Đọc tiếp
Một bình hình trụ đặt thẳng đứng có dung tích 8 lít và đường kính trong 20 cm, được đậy kín bằng một nắp có khối lượng 2 kg. Trong bình chứa khí ở nhiệt độ 100 ° C dưới áp suất bằng áp suất khí quyển ( 10 5 N/ m 2 ). Khi nhiệt độ trong bình giảm xuống còn 20 ° C thì: Áp suất khí trong bình bằng bao nhiêu?
Xét lượng khí trong bình.
Trạng thái đầu: V 1 = 8 lít; T 1 = 100 + 273 = 373 K ; p 1 = 10 5 N/ m 2
Trạng thái cuối: V 2 = 8 lít; T 2 = 20 + 273 = 293 K; p 2 = ?
Vì thể tích không đổi nên:
p 1 / T 1 = p 2 / T 2 ⇒ p 2 = p 1 T 2 / T 1 = 7,86. 10 4 N/ m 2
Đúng 0
Bình luận (0)
Một bình hình trụ đặt thẳng đứng có dung tích 8 lít và đường kính trong 20 cm, được đậy kín bằng một nắp có khối lượng 2 kg. Trong bình chứa khí ở nhiệt độ
100
°
C dưới áp suất bằng áp suất khí quyển (
10
5
N/
m
2
). Khi nhiệt độ trong bình giảm xuống còn 20
°
C thì: Muốn mở nắp bình cần một lực bằ...
Đọc tiếp
Một bình hình trụ đặt thẳng đứng có dung tích 8 lít và đường kính trong 20 cm, được đậy kín bằng một nắp có khối lượng 2 kg. Trong bình chứa khí ở nhiệt độ 100 ° C dưới áp suất bằng áp suất khí quyển ( 10 5 N/ m 2 ). Khi nhiệt độ trong bình giảm xuống còn 20 ° C thì: Muốn mở nắp bình cần một lực bằng bao nhiêu?
Cần tác dụng vào nắp một lực thằng được trọng lượng của nắp và lực gây ra bởi sự chênh lệch áp suất giữa không khí bên ngoài và bên trong bình:
F = mg + S( p 1 - p 2 ) = mg + π d 2 /4( p 1 - p 2 ) = 692N
Đúng 0
Bình luận (0)
Một bình kín chứa 1 mol khí Nito, áp suất 10 5 Pa, ở nhiệt độ 27 ° C . Do có một lượng khí thoát ra ngoài nên áp suất của khí trong bình chỉ còn 0,8. 10 5 Pa, nhiệt độ vẫn được giữ không đổi. Lượng khí đã thoát ra ngoài bằng:
A. 0,4mol
B. 0,8mol
C. 0,2mol
D. 0,1mol
Đáp án: C
Ban đầu, khí Nito có khối lượng mm, thể tích V, áp suất p, nhiệt độ T
PT: p 1 V = m M R T 1
- Sau một thời gian, khí Heli có khối lượng m′, thể tích V, áp suất p2, nhiệt độ T
PT: p 2 V = m ' M R T 2
Lấy 2 1 ta được:
p 2 p 1 = m ' m ↔ 0,8 1 = m ' m → m ' = 0,8 m
=> Lượng khí Nito đã thoát ra:
Δ m = m − m ' = m − 0,8 m = 0,2 m = 0,2.1.28 = 5,6 g
Số mol khí Nito thoát ra ngoài là: n = m M = 5,6 28 = 0,2 m o l
Vậy lượng khí đã thoát ra ngoài bằng: 0,2mol
Đúng 0
Bình luận (0)
Một bình kín chứa 1 mol khí nitơ ở áp suất
10
5
N
/
m
2
ở
27
°
C
Nung bình đến khi áp suất khí là
5
.
10
5
N
/
m
2
.Nhiệt độ khí bây giờ là? A.
127
°...
Đọc tiếp
Một bình kín chứa 1 mol khí nitơ ở áp suất 10 5 N / m 2 ở 27 ° C
Nung bình đến khi áp suất khí là 5 . 10 5 N / m 2 .Nhiệt độ khí bây giờ là?
A. 127 ° C
B. 60 ° C
C. 135 ° C
D. 1227 ° C
Đáp án D.
Ta có: p 1 T 1 = p 2 T 2 ⇒ T 2 = p 2 p 1 . T 1 = 1500 K = 1227 0 C
Đúng 0
Bình luận (0)
Một bình kín chứa 1 mol khí nitơ ở áp suất
10
5
N
/
m
2
ở 27°C. Nung bình đến khi áp suất khí là 5.
10
5
N/m:. Nhiệt độ khí bây giở là? A.
127
°
C B.
60
°
C...
Đọc tiếp
Một bình kín chứa 1 mol khí nitơ ở áp suất 10 5 N / m 2 ở 27°C. Nung bình đến khi áp suất khí là 5. 10 5 N/m:. Nhiệt độ khí bây giở là?
A. 127 ° C
B. 60 ° C
C. 135 ° C
D. 1227 ° C
- Một bình kín chứa khí oxi ở nhiệt độ 293 K và áp suất 105 pa.Nếu đem bình phơi nắng nhiệt độ 313K thì áp suất trong bình sẽ bao nhiêu.
Quá trình đẳng tích:
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\Rightarrow\dfrac{10^5}{293}=\dfrac{p_2}{313}\)
\(\Rightarrow p_2=110238Pa\)
Đúng 3
Bình luận (0)