X, Y là những nguyên tố có điện tích hạt nhân lần lượt là 12, 17. Cấu hình electron lớp ngoài cùng của nguyên tử X, Y và liên kết trong hợp chất tạo thành từ X và Y là

Những câu hỏi liên quan
X, Y là những nguyên tố có điện tích hạt nhân lần lượt là 9, 19.Cấu hình electron lớp ngoài cùng của nguyên tử X, Y và liên kết trong hợp chất tạo thành từ X và Y là A.
2
s
2
2
p
5
,
4
s
1
và liên kết cộng hóa trị. B.
2
s
2
2
p...
Đọc tiếp
X, Y là những nguyên tố có điện tích hạt nhân lần lượt là 9, 19.
Cấu hình electron lớp ngoài cùng của nguyên tử X, Y và liên kết trong hợp chất tạo thành từ X và Y là
A. 2 s 2 2 p 5 , 4 s 1 và liên kết cộng hóa trị.
B. 2 s 2 2 p 3 , 3 s 2 3 p 1 và liên kết cộng hóa trị.
C. 3 s 2 3 p 5 , 4 s 1 và liên kết ion.
D. 2 s 2 2 p 5 , 4 s 1 và liên kết ion.
Chọn D
Cấu hình electron nguyên tử X: [He]2s22p5.
Cấu hình electron nguyên tử Y: [Ar]4s1
X là phi kim điển hình (nhóm VIIA) và Y là kim loại điển hình (nhóm IA) nên liên kết trong hợp chất tạo thành từ X và Y là liên kết ion.
Đúng 0
Bình luận (0)
X, Y là những nguyên tố có điện tích hạt nhân lần lượt là 9, 19.Cấu hình electron lớp ngoài cùng của nguyên tử X, Y và liên kết trong hợp chất tạo thành từ X và Y là A. 2s22p5, 4s1 và liên kết cộng hóa trị. B. 2s22p3, 3s23p1 và liên kết cộng hóa trị. C. 3s23p1, 4s1 và liên kết ion. D. 2s22p5, 4s1 và liên kết ion.
Đọc tiếp
X, Y là những nguyên tố có điện tích hạt nhân lần lượt là 9, 19.Cấu hình electron lớp ngoài cùng của nguyên tử X, Y và liên kết trong hợp chất tạo thành từ X và Y là
A. 2s22p5, 4s1 và liên kết cộng hóa trị.
B. 2s22p3, 3s23p1 và liên kết cộng hóa trị.
C. 3s23p1, 4s1 và liên kết ion.
D. 2s22p5, 4s1 và liên kết ion.
X là nguyên tố hóa học có số điện tích hạt nhân
1
,
76
.
10
-
18
. Y là nguyên tố có số electron lớp ngoài cùng bằng 7. Hợp chất tạo bởi X, Y có công thức và liên kết hóa học là A.
X
2
Y
, liên kết cộng hóa trị B.
X
Y
2
, liên kết cho – nh...
Đọc tiếp
X là nguyên tố hóa học có số điện tích hạt nhân 1 , 76 . 10 - 18 . Y là nguyên tố có số electron lớp ngoài cùng bằng 7. Hợp chất tạo bởi X, Y có công thức và liên kết hóa học là
A. X 2 Y , liên kết cộng hóa trị
B. X Y 2 , liên kết cho – nhận
C. XY, liên kết cộng hóa trị
D. XY, liên kết ion
X là nguyên tố hóa học có số điện tích hạt nhân là 1,76.10-18 (C). Y là nguyên tố có số electron lớp ngoài cùng bằng 7. Hợp chất tạo bởi X, Y có công thức và liên kết hóa học là A. X2Y, liên kết cộng hóa trị. B. XY2, liên kết cho – nhận. C. XY, liên kết cộng hóa trị. D. XY, liên kết ion.
Đọc tiếp
X là nguyên tố hóa học có số điện tích hạt nhân là 1,76.10-18 (C). Y là nguyên tố có số electron lớp ngoài cùng bằng 7. Hợp chất tạo bởi X, Y có công thức và liên kết hóa học là
A. X2Y, liên kết cộng hóa trị.
B. XY2, liên kết cho – nhận.
C. XY, liên kết cộng hóa trị.
D. XY, liên kết ion.
Ta có ![]()
Y có số lớp e lớp ngoài cùng là 7 nên là 1 halogen.
Vậy lk giữa X và Y là XY: lk ion
Đáp án D
Đúng 0
Bình luận (0)
X, Y là những nguyên tố có đơn vị điện tích hạt nhân lần lượt là 6, 16. Công thức và liên kết hợp chất tạo thành từ X và Y là A. XY và liên kết cộng hóa trị. B.
X
2
Y
và liên kết ion. C. XY và liên kết ion. D.
X
Y
2
và liên kết cộng hóa trị.
Đọc tiếp
X, Y là những nguyên tố có đơn vị điện tích hạt nhân lần lượt là 6, 16. Công thức và liên kết hợp chất tạo thành từ X và Y là
A. XY và liên kết cộng hóa trị.
B. X 2 Y và liên kết ion.
C. XY và liên kết ion.
D. X Y 2 và liên kết cộng hóa trị.
Chọn D
Cấu hình electron nguyên tử X: [He]2s22p2
Cấu hình electron nguyên tử Y: [Ne] 3s23p4
Ta có:
: X : + 2 : Y . . : → : Y .. : : X : : Y : ..
→ Hợp chất cộng hóa trị tạo thành từ X và Y là XY2.
Đúng 0
Bình luận (0)
Nguyên tố X không phải là khí hiếm, nguyên tử có phân lớp electron ngoài cùng là 3p. Nguyên tử nguyên tố Y có phân lớp e ngoài cùng là 3s. Tổng số e ở hai phân lớp ngoài cùng của X và Y là 7. Điện tích hạt nhân của X và Y lần lượt là A. X (18+); Y (10+) B. X (13+); Y (15+) C. X (12+); Y (16+) D. X (17+); Y (12+)
Đọc tiếp
Nguyên tố X không phải là khí hiếm, nguyên tử có phân lớp electron ngoài cùng là 3p. Nguyên tử nguyên tố Y có phân lớp e ngoài cùng là 3s. Tổng số e ở hai phân lớp ngoài cùng của X và Y là 7. Điện tích hạt nhân của X và Y lần lượt là
A. X (18+); Y (10+)
B. X (13+); Y (15+)
C. X (12+); Y (16+)
D. X (17+); Y (12+)
Nguyên tố X không phải là khí hiếm, nguyên tử có phân lớp electron ngoài cùng là 3p. Nguyên tử nguyên tố Y có phân lớp e ngoài cùng là 3s. Tổng số e ở hai phân lớp ngoài cùng của X và Y là 7. Điện tích hạt nhân của X và Y lần lượt là A. X (18+);Y(10+). B. X (13+);Y(15+). C. X (12+);Y(16+). D. X (17+);Y(12+)
Đọc tiếp
Nguyên tố X không phải là khí hiếm, nguyên tử có phân lớp electron ngoài cùng là 3p. Nguyên tử nguyên tố Y có phân lớp e ngoài cùng là 3s. Tổng số e ở hai phân lớp ngoài cùng của X và Y là 7. Điện tích hạt nhân của X và Y lần lượt là
A. X (18+);Y(10+).
B. X (13+);Y(15+).
C. X (12+);Y(16+).
D. X (17+);Y(12+)
Đáp án D
Cấu hình electron của nguyên tố X, Y lần lượt là 1s22s22p63s23px và 1s22s22p63sy.
Ta có: x + y = 7.
• TH1: y = 1 → x = 6
→ Cấu hình electron của nguyên tố X, Y lần lượt là 1s22s22p63s23p6 và 1s22s22p63s1.
Mà X không phải là khí hiếm → loại.
• TH2: y = 2 → x = 5
→ Cấu hình electron của nguyên tố X, Y lần lượt là 1s22s22p63s23p5 và 1s22s22p63s2.
Vậy điện tích hạt nhân của X, Y lần lượt là X (17+) và Y (12+) → Chọn D.
Đúng 0
Bình luận (0)
Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là
3
s
2
, nguyên tử của nguyên tố Y có cấu hình electron lớp ngoài cùng là
2
s
2
2
p
3
. Công thức phân tử của hợp chất tạo bởi X và Y có dạng
Đọc tiếp
Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là 3 s 2 , nguyên tử của nguyên tố Y có cấu hình electron lớp ngoài cùng là 2 s 2 2 p 3 . Công thức phân tử của hợp chất tạo bởi X và Y có dạng
![]()
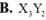
![]()
![]()
Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là 3s2, nguyên tử của nguyên tố Y có cấu hình electron lớp ngoài cùng là 2s22p3. Công thức phân tử của hợp chất tạo bởi X và Y có dạng A. X2Y3. B. X3Y2. C. X5Y2. D. X2Y2.
Đọc tiếp
Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là 3s2, nguyên tử của nguyên tố Y có cấu hình electron lớp ngoài cùng là 2s22p3. Công thức phân tử của hợp chất tạo bởi X và Y có dạng
A. X2Y3.
B. X3Y2.
C. X5Y2.
D. X2Y2.
Đáp án B
X là nguyên tố nhóm IIA (hóa trị II)
Y là nguyên tố nhóm VA (hóa trị III)
Như vậy, công thức hợp chất phải là X3Y2
Đúng 0
Bình luận (0)






