1 mol khí lí tưởng thực hiện chu trình 1 - 2 - 3 - 4 - 1 như hình VI.2. Nhiệt độ T 3 có giá trị bằng
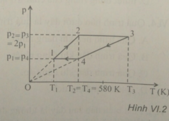
A. 1160 K.
B. 580 K.
C. 290 K.
D. 145 K.
1 mol khí lí tưởng thực hiện chu trình 1 – 2 – 3 – 4 – 1 như hình VI.2. Nhiệt độ T 3 có giá trị bằng
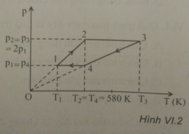
A. 1160 K
B. 580 K
C. 290 K
D. 145 K
Chọn A.
Vì 3 - 4 là quá trình đẳng tích (do đồ thị là đường thẳng có đường kéo dài đi qua O trong đồ thị p-T) nên:
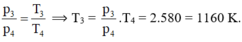
Một khí lí tưởng thực hiện quá trình đẳng tích 1 – 2 rồi đẳng áp 2 – 3 (Hình 33.2) Trong mỗi đoạn, khí nhận nhiệt hay tỏa nhiệt?
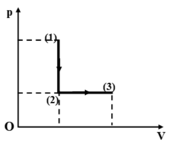
A. 1 – 2 nhận nhiệt; 2 – 3 nhận nhiệt
B. 1 – 2 nhận nhiệt; 2 – 3 tỏa nhiệt.
C. 1 – 2 tỏa nhiệt; 2 – 3 nhận nhiệt
D. 1 – 2 tỏa nhiệt; 2 – 3 tỏa nhiệt
Chọn C.
Quá trình 1-2 là làm lạnh đẳng tích → khí tỏa nhiệt, ∆ U = Q 12 < 0
Quá trình 2-3 là làm giãn nở đẳng áp → khí nhận nhiệt và sinh công A = - p 2 V 3 - V 2
Một lượng khí lí tưởng thực hiện quá trình đẳng áp 1 – 2 rồi đẳng nhiệt 2 – 3 (Hình 33.1). Trong mỗi đoạn, khí nhận công hay sinh công?
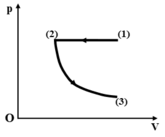
A. 1 – 2 nhận công; 2 – 3 sinh công
B. 1 – 2 nhận công; 2 – 3 nhận công
C. 1 – 2 sinh công; 2 – 3 sinh công.
D. 1 – 2 sinh công; 2 – 3 nhận công.
Chọn A.
Đoạn 1-2 là quá trình nén đẳng áp → khí nhận công
Quá trình 2-3 là giãn nở đẳng nhiệt → khí sinh công
Một khí lí tưởng thực hiện quá trình đẳng tích 1 – 2 rồi đẳng áp 2 – 3. Trong mỗi đoạn, khí nhận nhiệt hay tỏa nhiệt?
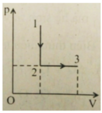
A. 1 – 2 nhận nhiệt; 2 – 3 nhận nhiệt
B. 1 – 2 nhận nhiệt; 2 – 3 tỏa nhiệt
C. 1 – 2 tỏa nhiệt; 2 – 3 nhận nhiệt
D. 1 – 2 tỏa nhiệt; 2 – 3 tỏa nhiệt
Từ đồ thị, ta có:
Quá trình 1→2: Quá trình đẳng tích, trong quá trình này
Thể tích không đổi
Lại có: p 1 T 1 = p 2 T 2 và p 1 > p 2
Ta suy ra T 2 > T 1
=> Nhiệt độ tăng nên nội năng tăng
=> Khí tỏa nhiệt
Quá trình 2→3: Quá trình đẳng áp, trong quá trình này:
Áp suất không đổi
Thể tích khí tăng V 3 > V 2
=> Nhiệt độ khí tăng => Nội năng tăng
=> Khí sinh công => Khí nhận nhiệt
Đáp án: C
Một lượng khí lí tưởng thực hiện quá trình đẳng áp 1 – 2 rồi đẳng nhiệt 2 – 3. Trong mỗi đoạn, khí nhận công hay sinh công?
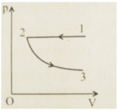
A. 1 – 2 nhận công; 2 – 3 sinh công
B. 1 – 2 nhận công; 2 – 3 nhận công
C. 1 – 2 sinh công; 2 – 3 sinh công
D. 1 – 2 sinh công; 2 – 3 nhận công
Từ đồ thị, ta có:
Quá trình 1→2: Quá trình đẳng áp, trong quá trình này
Áp suất không đổi
Thể tích giảm V 2 < V 1
Lại có V 1 T 1 = V 2 T 2
⇒ V 1 V 2 = T 1 T 2 > 1 ⇒ T 1 > T 2
=> Nhiệt độ giảm
=> Vật nhận công
Quá trình 2→3: Quá trình đẳng nhiệt, trong quá trình này:
Nhiệt độ không đổi
Thể tích khí tăng nên vật thực hiện công
Đáp án: A
Một lượng khí lí tưởng thực hiện qua trình thể hiện bởi đoạn thẳng 1 – 2 trển đồ thi p – V (Hình vẽ). Trong quá trình đó, chất khí
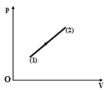
A. sinh công, tỏa nhiệt.
B. sinh công, nhận nhiệt.
C. nhận công, nhận nhiệt.
D. nhận công, tỏa nhiệt.
Chọn B.
Dựa vào đồ thị ta thấy từ (1) sang (2), thể tích của khối khí tăng, áp suất tăng nên khối khí sinh công.
Áp suất tăng, nhiệt độ tăng nên khối khí nhận nhiệt.
Một lượng khí lí tưởng thực hiện qua trình thể hiện bởi đoạn thẳng 1 – 2 trển đồ thị p – V (Hình vẽ). Trong quá trình đó, chất khí
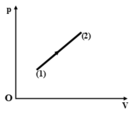
A. sinh công, tỏa nhiệt
B. sinh công, nhận nhiệt
C. nhận công, nhận nhiệt
D. nhận công, tỏa nhiệt
Chọn B.
Dựa vào đồ thị ta thấy từ (1) sang (2), thể tích của khối khí tăng, áp suất tăng nên khối khí sinh công.
Áp suất tăng, nhiệt độ tăng nên khối khí nhận nhiệt.
Một mol khí ôxi thực hiện chu trình 1 – 2 – 3 – 1 (Hình VI.3). Trong mỗi giai đoạn 1 – 2; 2 – 3; 3 – 1, chất khí
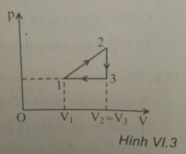
A. 1 – 2 nhận nhiệt, sinh công; 2 – 3 tỏa nhiệt, nhận công hoặc không sing công; 3 – 1 nhận công, tỏa nhiệt.
B. 1 – 2 tỏa nhiệt, sinh công; 2 – 3 tỏa nhiệt, nhận công; 3 – 1 nhận công, tỏa nhiệt
C. 1 – 2 nhận nhiệt, sinh công; 2 – 3 nhận nhiệt, nhận công; 3 – 1 nhận công, tỏa nhiệt.
D. 1 – 2 nhận nhiệt, nhận công; 2 – 3 tỏa nhiệt, nhận công; 3 – 1 nhận nhiệt, thực hiện công
Chọn A.
Theo nguyên lí I nhiệt động lực học:
Q = ∆U - A = ∆U + A’
(Q: Nhiệt lượng mà hệ nhận được, A’ là công mà hệ sinh ra, ∆U: độ biến thiên nội năng)
Giai đoạn 1-2: V tăng (khí dãn nở) => khí sing công (A’ > 0).
Mặt khác, tích pV tăng => T tăng => ∆U > 0.
Do đó Q > 0. Vậy khí nhận nhiệt, sinh công
Gia đoạn 2-3: Quá trình đẳng tích, p giảm. T giảm: khí tỏa nhiệt, không sinh hoặc nhận công.
Giai đoạn 3-1: Quá trình đẳng áp, V giảm, T giảm: chất khí nhận công, tỏa nhiệt.
Một mol khí ôxi thực hiện chu trình 1 - 2 - 3 - 1 (Hình VI.3). Trong mỗi giai đoạn 1 - 2 ; 2 - 3 ; 3 - 1 , chất khí

A. 1 - 2 nhận nhiệt, sinh công; 2 - 3 tỏa nhiệt, nhận công hoặc không sing công; 3 - 1 nhận công, tỏa nhiệt.
B. 1 - 2 tỏa nhiệt, sinh công; 2 - 3 tỏa nhiệt, nhận công; 3 - 1 nhận công, tỏa nhiệt.
C. 1 - 2 nhận nhiệt, sinh công; 2 - 3 nhận nhiệt, nhận công; 3 - 1 nhận công, tỏa nhiệt.
D. 1 - 2 nhận nhiệt, nhận công; 2 - 3 tỏa nhiệt, nhận công; 3 - 1 nhận nhiệt, thực hiện công.
Chọn A.
Theo nguyên lí I nhiệt động lực học: Q = ∆U - A = ∆U + A’
(Q: Nhiệt lượng mà hệ nhận được, A’ là công mà hệ sinh ra, ∆U: độ biến thiên nội năng)
Giai đoạn 1-2: V tăng (khí dãn nở) => khí sing công (A’ > 0).
Mặt khác, tích pV tăng => T tăng => U > 0.
Do đó Q > 0. Vậy khí nhận nhiệt, sinh công
Gia đoạn 2-3: Quá trình đẳng tích, p giảm. T giảm: khí tỏa nhiệt, không sinh hoặc nhận công.
Giai đoạn 3-1: Quá trình đẳng áp, V giảm, T giảm: chất khí nhận công, tỏa nhiệt.