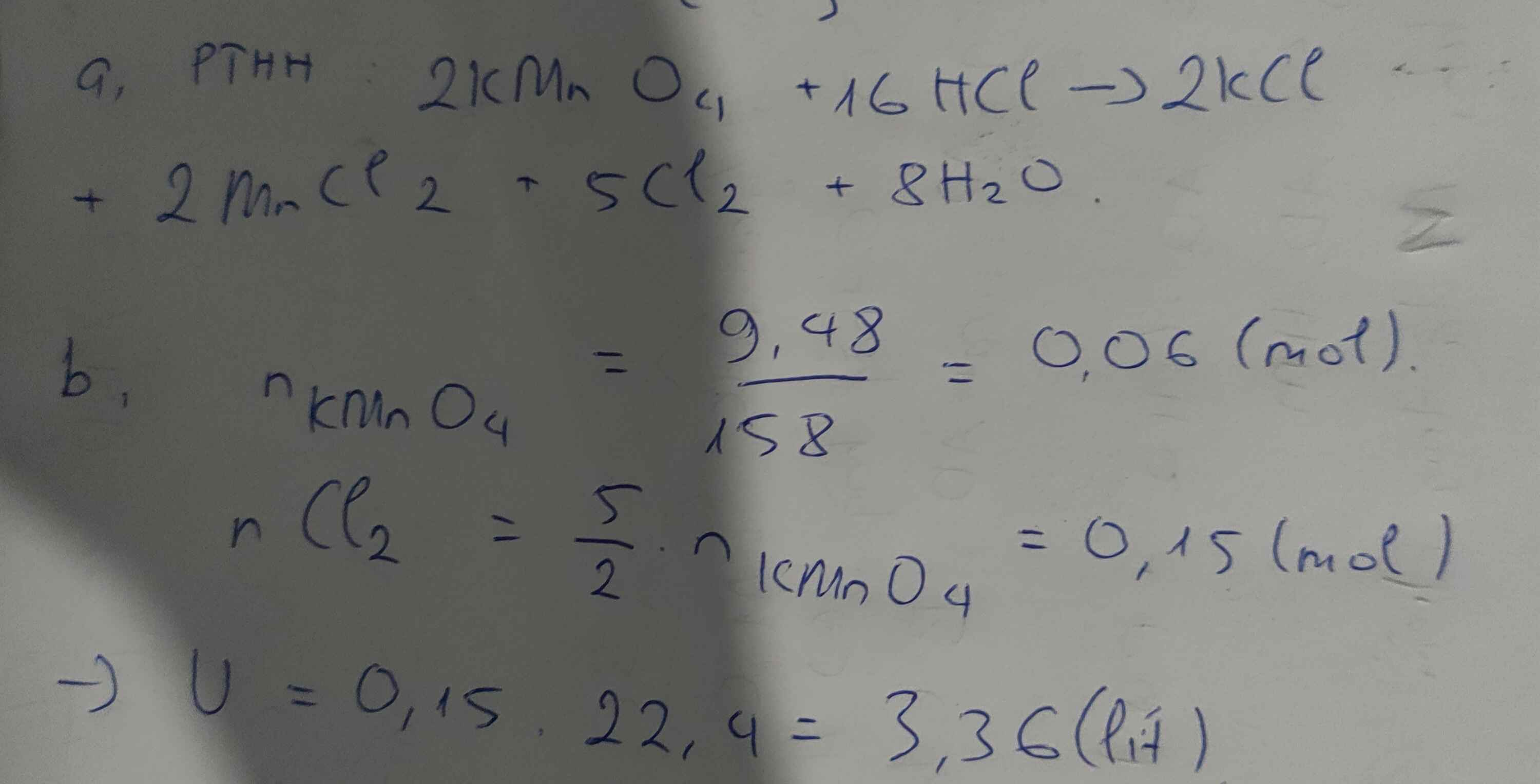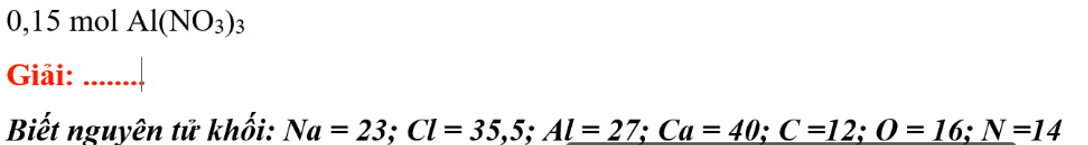Hóa học
Đọc tiếp
Bài 2.
a) \(\left(1\right)2HCl\rightarrow H_2+Cl_2\)
\(\left(2\right)Cl_2+H_2\rightarrow2HCl\)
\(\left(3\right)2Fe+3Cl_2\underrightarrow{t_o}2FeCl_3\)
\(\left(4\right)2FeCl_3+Fe\rightarrow3FeCl_2\)
\(\left(5\right)2NaOH+Cl_2\rightarrow H_2O+NaCl+NaClO\)
b) \(\left(1\right)2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(\left(2\right)Cl_2+H_2\rightarrow2HCl\)
\(\left(3\right)2HCl+FeO\rightarrow FeCl_2+H_2O\)
\(\left(4\right)3FeCl_2+4HNO_3\rightarrow2FeCl_3+Fe\left(NO_3\right)_3+NO+2H_2O\)
\(\left(5\right)2FeCl_3+Fe\rightarrow3FeCl_2\)
\(\left(6\right)FeCl_3+3AgNO_3\rightarrow Fe\left(NO_3\right)_3+3AgCl\downarrow\)
Đúng 3
Bình luận (0)
Câu 1:
a)
\(2Fe+3Cl_2\underrightarrow{t^o}2FeCl_3\)
\(Mg+Cl_2\underrightarrow{t^o}MgCl_2\)
\(2NaBr+Cl_2\rightarrow2NaCl+Br_2\)
\(2KI+Cl_2\rightarrow2KCl+I_2\)
\(H_2+Cl_2\underrightarrow{as}2HCl\)
\(2NaOH+Cl_2\rightarrow NaCl+NaClO+H_2O\)
\(Cl_2+H_2O⇌HCl+HClO\)
b)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2\uparrow+H_2O\)
\(HCl+AgNO_3\rightarrow AgCl\downarrow+HNO_3\)
\(Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
Đúng 4
Bình luận (3)
Câu 2:
a: (1): \(2HCl\rightarrow H_2+Cl_2\)(đk: điện phân dung dịch)
(2): \(Cl_2+H_2\rightarrow2HCl\)(đk: as)
(3): \(3Cl_2+2Fe\rightarrow2FeCl_3\)(điều kiện: t độ)
(4): \(2FeCl_3+Fe\rightarrow3FeCl_2\)(đk: đun sôi dung môi)
(5): \(Cl_2+2NaOH\rightarrow NaClO+NaCl+H_2O\)
b:
(1): \(2KMnO_4+16HCl\rightarrow5Cl_2+8H_2O+2KCl+2MnCl_2\)
(2): \(Cl_2+H_2\rightarrow2HCl\)
(3): \(2HCl+Fe\rightarrow FeCl_2+H_2\)
(4): \(2FeCl_2+Cl_2\rightarrow2FeCl_3\)
(5): \(2FeCl_3+Fe\rightarrow3FeCl_2\)
\(\left(6\right):FeCl_3+3AgNO_3\rightarrow3AgCl+Fe\left(NO_3\right)_3\)
Đúng 3
Bình luận (0)
Để đốt cháy hoàn toàn hỗn hợp X gồm 0,1 mol Al và 0,05 mol Mg cần dùng một lượng hỗn hợp khí Y gồm 0,05 mol O2 và x mol khí Cl2. Sau khi phản ứng xong, thu được m gam chất Z. Giá trị của m là
BT e: \(3n_{Al}+2n_{Mg}=4n_{O_2}+2n_{Cl_2}\)
\(\Rightarrow3\cdot0,1+2\cdot0,05=4\cdot0,05+2\cdot x\)
\(\Rightarrow x=0,1mol\)
\(m=m_{Al}+m_{Mg}+m_{O_2}+m_{Cl_2}\)
\(=0,1\cdot27+0,05\cdot24+0,05\cdot2\cdot16+0,1\cdot35,5\cdot2\)
\(=12,6g\)
Đúng 4
Bình luận (0)
Theo bảo toàn electron ta có: \(3\cdot n_{Al}+2\cdot n_{Mg}=2\cdot n_{Cl_2}+4\cdot N_{O_2}\)
\(\Rightarrow3\cdot0,1+2\cdot0,05=4\cdot0,05+2x\Rightarrow x=0,2\)
\(\Rightarrow m_Z=m_X+m_Y=0,1\cdot27+0,05\cdot24+0,05\cdot32+0,2\cdot71=19,7g\)
Đúng 0
Bình luận (0)
\(C+O_2\underrightarrow{t_o}CO_2\)
\(N+O_2\underrightarrow{t_O}NO_2\)
\(4Na+O_2\underrightarrow{t_o}2Na_2O\)
\(2Ca+O_2\underrightarrow{t_O}2CaO\)
\(4Al+3O_2\underrightarrow{t_o}2Al_2O_3\)
\(C_2H_4+3O_2\underrightarrow{t_o}2CO_2+2H_2O\)
\(C_2H_2+\dfrac{5}{2}O_2\underrightarrow{t_o}2CO_2+H_2O\)
Đúng 3
Bình luận (0)
1: \(C+O_2\rightarrow CO_2\)
2: \(4N+O_2\rightarrow2N_2O\)
3: \(4Na+O_2\rightarrow2Na_2O\)
4 \(2Ca+O_2\rightarrow2CaO\)
5 \(4Al+3O_2\rightarrow2Al_2O_3\)
6: \(C_2H_4+O_2\rightarrow CH_3CHO\)
7: \(2C_2H_2+5O_2\rightarrow4CO_2+2H_2O\)
Đúng 3
Bình luận (0)
1.\(CO_2\)
2.\(NO_2\)
3.4Na+\(O_2\)->2\(Na_2O\)
4.CaO
5.\(4Al+3O_2->2Al_2O_3\)
6.\(C_2H_4+3O_2->2H_2O+2CO_2\)
7.\(2C_2H_2+5O_2->4CO_2+2H_2O\)
Đúng 1
Bình luận (0)
cân bằng pthh 2Hg----to--->Hg + o
\(2HgO\rightarrow\left(450^oC-500^oC\right)2Hg+O_2\uparrow\)
Đúng 5
Bình luận (0)
Đốt cháy 4,48 lít khí etilen trong 6,72 lít khí O2. Tính thể tích của các khí còn lại sau phản ứng . Cần gấp ạ, cảm ơn
C2H4+3O2-to>2CO2+2H2O
0,3-------0,2-------0,2
n C2H4=\(\dfrac{4,48}{22,4}\)=0,2 mol
n O2=\(\dfrac{6,72}{22,4}\)=0,3 mol
=>C2H4 dư
=>VCO2=VH2O=0,2.22,4=4,48l
=>VC2H4 dư=0,1.22,4=2,24l
Đúng 4
Bình luận (1)
\(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ n_{C_2H_4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ C_2H_4+3O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\\ Vì:\dfrac{0,2}{1}>\dfrac{0,3}{3}\Rightarrow C_2H_4dư\\ \Rightarrow n_{CO_2}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ n_{C_2H_4\left(dư\right)}=0,2-\dfrac{0,3}{3}=0,1\left(mol\right)\\ \Rightarrow V_{CO_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\\ V_{C_2H_4\left(dư\right)}=0,1.22,4=2,24\left(l\right)\)
Đúng 3
Bình luận (3)
dùng khí H khử 8g đồng oxit . Tính kl kim loại thu dc (giả sử hiệu suất phản ứng đạt 80% )
CuO+H2-to>Cu+H2O
0,1---------------0,1 mol
n CuO=\(\dfrac{8}{80}\)=0,1 mol
H=80%
=>m Cu=0,1.64.\(\dfrac{80}{100}\)=5,12g
Đúng 3
Bình luận (1)
CuO+H2\(CuO+H_2\underrightarrow{t^0}Cu+H_2O\)Cu+H2O
Theo PT: \(n_{H_{2\left(lt\right)}}\)=\(n_{CuO}\)=\(\dfrac{8}{80}\)=0,1(mol)
Vì hiệu suất đạt 80%
⇒\(V_{H_2}\)(thực)=\(\dfrac{0,1.22,4}{80\%}\)=2,8(l)
Đúng 0
Bình luận (1)
nhiệt phân 39,5g KMnO4 thu dc 2,24 lít khí õxi ở dktc tính hiệu suất phản ứng
2KMnO4-to>K2MnO4+MnO2+O2
0,2---------------------------------------0,1 mol
n O2=\(\dfrac{2,24}{22,4}\)=0,1 mol
=>m KMnO4 tt =0,2.158=31,6g
=>H =\(\dfrac{31,6}{39,5}.100\)=80%
Đúng 6
Bình luận (0)
Ta có: \(n_{KMnO_4}=\dfrac{39,5}{158}=0,25\left(mol\right)\)
PT: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
Theo PT: \(n_{O_2\left(LT\right)}=\dfrac{1}{2}n_{KMnO_4}=0,125\left(mol\right)\)
Mà: \(n_{O_2\left(TT\right)}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(\Rightarrow H\%=\dfrac{0,1}{0,125}.100\%=80\%\)
Bạn tham khảo nhé!
Đúng 4
Bình luận (1)
Xem thêm câu trả lời
\(M=27+\left(14+16.3\right).3=213\left(\dfrac{g}{mol}\right)\)
\(m=n.M=0,15.213=31,95\left(g\right)\)
Đúng 5
Bình luận (0)
\(m_{Al\left(NO_3\right)_3}=0,15.213=31,95\left(g\right)\)
\(V_{Al\left(NO_3\right)_3}=0,15.22,4=3,36\left(l\right)\)
mk k bt đề bài hỏi j nên mk làm 2 cách nha
Đúng 6
Bình luận (2)
Xem thêm câu trả lời
Cho 9,2 gam hỗn hợp Fe và Mg phản ứng vừa đủ với 200ml dung dịch axit clohiđric thu được 5,6 lít khí Hiđro ở đktc.
a) Tính thành phần phần trăm các chất có trong hỗn hợp ban đầu.
b) Tính nồng độ mol dung dịch axit clohiđric đã dùng.
c) Tính khối lượng muối thu được sau phản ứng.
mn giúp với ạ
\(a,Đặt:n_{Mg}=g\left(mol\right);n_{Fe}=j\left(mol\right)\left(g,j>0\right)\\ Fe+2HCl\rightarrow FeCl_2+H_2\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ \Rightarrow\left\{{}\begin{matrix}24g=56j=9,2\\22,4g+22,4j=5,6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}g=0,15\\j=0,1\end{matrix}\right.\\ \Rightarrow\%m_{Mg}=\dfrac{0,15.24}{9,2}.100\approx39,13\%\\ \Rightarrow\%m_{Fe}\approx60,87\%\\ b,n_{HCl}=2n_{H_2}=\dfrac{2.5,6}{22,4}=0,5\left(mol\right)\\ \Rightarrow C_{MddHCl}=\dfrac{0,5}{0,2}=2,5\left(M\right)\\ c,m_{muối}=m_{FeCl_2}+m_{MgCl_2}=95g+127j=95.0,15+127.0,1=26,95\left(g\right)\)
Đúng 6
Bình luận (0)
Fe+2HCl->FeCl2+H2
x-----------------------x mol
Mg+2HCl->MgCl2+H2
y-------------------------y mol
ta có\(\left\{{}\begin{matrix}56x+24y=9,2\\x+y=0,25\end{matrix}\right.\)
=>\(\left\{{}\begin{matrix}x=0,1\\y=0,15\end{matrix}\right.\)
=>%mFe=\(\dfrac{0,1.56}{9,2}.100\)=60,87%
=>%m Mg=39,13%
Ta có : n HCl=0,1.2+0,15.2=0,5 mol
=>CMHCl=\(\dfrac{0,5}{0,2}\)=2,5M
=>m muối =0,1.127+0,15.95=26,95g
Đúng 3
Bình luận (0)