cho hỗn hợp X gồm Al,Fe,Cu có khối lượng là 35,8g tác dụng với HCl dư thu đc 12,395lít H2 ở đkc và dd Y chứa 52,1g muối .Xác định khối lượng của các muối trong hỗn hợp ban đầu
Có lẽ đề hỏi khối lượng các KL trong hh đầu chứ bạn nhỉ?
Ta có: 27nAl + 56nFe + 64nCu = 35,8 (1)
BTNT Al, Fe: nAlCl3 = nAl, nFeCl2 = nFe
⇒ 133,5nAl + 127nFe = 52,1 (1)
\(n_{H_2}=\dfrac{12,395}{24,79}=0,5\left(mol\right)\)
BT e, có: 3nAl + 2nFe = 0,5.2 (3)
Từ (1), (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}n_{Al}=0,2\left(mol\right)\\n_{Fe}=0,2\left(mol\right)\\n_{Cu}=0,3\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Al}=0,2.27=5,4\left(g\right)\\m_{Fe}=0,2.56=11,2\left(g\right)\\m_{Cu}=0,3.64=19,2\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Nguyên tử của nguyên tố X có tổng số hạt proton, neutron, electron là 60. Trong hạt nhân, số hạt mang điện bằng số hạt không mang điện. Cho biết số đơn vị điện tích hạt nhân của X... Em cần gấp ạ tối nay nộp rồi!!!!
Theo đề bài ta có:
\(\left\{{}\begin{matrix}p+n+e=60\\p=n\end{matrix}\right.< =>\left\{{}\begin{matrix}3p=60\\p=n\end{matrix}\right.\)
==> \(\left\{{}\begin{matrix}p=e=\dfrac{60}{3}=20\left(hạt\right)\\p=n=20\left(hạt\right)\end{matrix}\right.\)
Số đơn vị điện tích hạt nhân: \(Z=n_P=20\)
Đúng 2
Bình luận (0)
\(\left[{}\begin{matrix}2p+n=60\\p=n\end{matrix}\right.\)
\(\Leftrightarrow2p+p=60\)
\(\Leftrightarrow3p=60\)
\(\Leftrightarrow p=Z=20\)
Đúng 0
Bình luận (0)
 giúp mình câu này vs ạ
giúp mình câu này vs ạ
\(\%^{35}Cl=100\%-24,23\%=75,77\%\)
\(\overline{Cl}=\dfrac{37.24,23+35.75,77}{100}=35,4846\)
\(\%m_{^{37}Cl}=\dfrac{37.0,7577}{1+35,4846+16.4}.100\%\approx26,392\%\)
Đúng 0
Bình luận (0)
Sửa lại (bỏ phần giả sử về sau)
\(1\left(mol\right)HClO_4\rightarrow1\left(mol\right)Cl\)
\(\Rightarrow n\left(^{37}Cl\right)\) trong \(1\left(mol\right)HClO_4\) là \(1.24,23\%=0,2423\left(mol\right)\)
\(m\left(^{37}Cl\right)\) trong \(1\left(mol\right)HClO_4\) là \(0,2423.37=8,9651\left(g\right)\)
\(\Rightarrow\%m\left(^{37}Cl\right)=\dfrac{8,9651}{100,485}.100\%=8,92\%\)
Đúng 1
Bình luận (0)
Co có cấu hình : 1s2 2s2 2p6 3s2 3p6 3d7 4s2 .Vậy để đạt cấu hình bền vừng chúng ta phải làm sao??
GIÚP MÌNH VỚI Ạ
Lớp \(4s\) ngoài cùng có \(2\) electron; phân lớp \(3d\) ngoài cùng có \(7\) electron
\(\Rightarrow\text{ }\)Nguyên tử này có thể :
- Nhường \(2\) electron ở lớp \(4s\): Nguyên tử sẽ trở thành ion dương có cấu hình electron của khí hiếm Argon \(\left(Ar\right)\) \(\rightarrow\) cấu hình bền vững
- Nhận \(1\) electron để lấp đầy phân lớp \(3d\): Nguyên tử sẽ trở thành ion âm (trường hợp này rất hiếm)
Vậy để đạt cấu hình bền vững nguyên tử sẽ nhường \(2\) electron ở lớp \(4s\)
Đúng 0
Bình luận (0)
cứ 1 mol 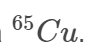 thì sẽ có bao nhiêu
thì sẽ có bao nhiêu 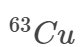
giúp mk vs ạ
Xét 1 mol Cu có x mol 65Cu và (1 – x) mol 63Cu
⟹ MCu = 65x + 63.(1 – x) = 63,546
⟹ x = 27,3%
Bạn tham khảo
Đúng 1
Bình luận (0)
1 nguyên tử có tổng số hạt mang điện nhiều hơn hạt không mang điện là 22 xác định tên nguyên tố và kí hiệu hoá học
Nguyên tử Ý có tổng số các hạt là 36. Số hạt không mang điện bằng một nữa hiệu số giữa tổng số hạt với số hạt mang điện tích âm. Xác định thành phần cấu tạo của nguyên tử Y
Ta có:
\(p+e+n=36\)
\(2p+n=36\)
\(n=\dfrac{1}{2}\left(2p+n-e\right)\)
\(n=\dfrac{1}{2}\left(2p+n-p\right)\)
\(n=\dfrac{1}{2}\left(p+n\right)\)
\(\dfrac{1}{2}n+\dfrac{1}{2}n=\dfrac{1}{2}p+\dfrac{1}{2}n\)
\(\Rightarrow p=n\)
Mà số \(p\) = số \(e\) do nguyên tử trung hòa về điện
\(\Rightarrow p=n=e=\dfrac{1}{3}\left(p+e+n\right)=\dfrac{1}{3}.36=12\) (hạt)
Vậy nguyên tử Y được cấu tạo bởi:
+) 12 proton
+) 12 neutron
+) 12 electron
Đúng 2
Bình luận (0)
tính nguyên tử khối trung bình
\(^{56}_{26}Fe\left(91,72\%\right);^{57}_{26}Fe\left(2,2\%\right);^{58}_{26}Fe\left(0,28\%\right)\)
\(\overline{M}=\dfrac{56.91,72+57.2,2+58.0,28}{100}=52,7796\)
Đúng 2
Bình luận (0)
hoàn thành bảng và cho em hỏi "ĐTHN" là gì ạ?

























