Đốt cháy hoàn toàn m gam hỗn hợp A gồm: C3H6, C2H4 và C4H5 bằng khí O2 . Hấp thụ hết toàn bộ sản phẩm cháy vào bình đựng nước vôi trong dư, thấy tạo thành 30g chất kết tủa trắng. Giá trị của m là
Hóa học
Cân lấy 10,6 Na2co3 cho vào cốc cha độ có dung dịch 500ml. Rót từ từ nước cất vào cốc cho vạch 200ml. Khuấy đều nhẹ cho Na2co3 . Biết 1ml dung dịch cho khối lượng 1,05 g.
Hãy xác định nồng độ phần trăm ( C% ) và nồng độ mol của dung dịch vừa được pha chế ?
Giúp mình với còn câu này mà chưa hoàn thành đc cho lắm.
\(nNa_2CO_3=\dfrac{10,6}{106}=0,1\left(mol\right)\)
Vdd = 200 ml = 0,2(l)
\(Na_2CO_3+H_2O\rightarrow NaHCO_3+NaOH\)
1 1 1 1 (mol)
0,1 0,1 0,1 0,1 (mol)
theo đề ta suy ra : mdd = 1,05 . 200 = 210 (g)
\(mNaHCO_3=0,1.84=8,4\left(g\right)\)
\(mNaOH=0,1.40=4\left(g\right)\)
=> ndd sau pứ = 0,1 + 0,1 = 0,2 (mol)
m dd vừa đc pha chế = m NaHCO3 + mNaOH
= > mdd vừa đc pha chế = \(8,4+4=12,4\left(g\right)\)
\(C\%dd=\dfrac{12,4.100}{210}=5,9\%\)
\(CM_{dd}=\dfrac{n_{dd}}{V_{dd}}=\dfrac{0,2}{0,2}=1M\)
Đúng 2
Bình luận (1)
trình bày phương pháp hóa học nhận biết dung dịch các chất sau đây đựng riêng biệt trong các lọ:
a. Na2SO4, Ba(OH)2, HNO3
B. K2SO4, Ca(oh)2, hcl
a) cho quỳ tím vào các dd
QT hóa xanh => Ba(OH)2
QT hóa đỏ => HNO3
QT không đổi màu => Na2SO4
b) cho QT vào các dd
QT hóa đỏ => HCl
QT hóa xanh => Ca(OH)2
QT không đổi màu => K2SO4
Đúng 4
Bình luận (1)
Hoàn thành chuỗi phản ứng sau, ghi rõ điều kiện phản ứng nếu có:
Fe --> H2 --> H2O --> H2SO4
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\\ 2H_2+O_2\underrightarrow{t^o}2H_2O\\ SO_3+H_2O\rightarrow H_2SO_4\)
Đúng 4
Bình luận (0)
trình bày phương pháp hóa hcoj nhận biết dung dịch các chất sau đây đựng riêng biệt trong các lọ:
a. Na2SO4, Ba(OH)2, HNO3
B. K2SO4, Ca(oh)2, hcl
a) cho quỳ tms vào các dd
QT hóa xanh => Ba(OH)2
QT hóa đỏ => HNO3
QT không đổi màu => Na2SO4
b) cho QT vào các dd
QT hóa đỏ => HCl
QT hóa xanh => Ca(OH)2
QT không đổi màu => K2SO4
Đúng 3
Bình luận (0)
Giải thích hiện tượng trong đời sống -Trái cây chín mùi thơm mùi rượu. -Rượu để lâu bị chua. -Áo len làm từ lông cừu khi giặt bằng xà phòng dễ bị hỏng. -Thịt, trứng nướng quá lửa có mùi khét. -Khi ăn thịt (nấu chín) của các loài động vật khác nhau thì cảm giác mùi vị khác nhau.
- Khi trái cây bị chín sẽ có một phần đường/tinh bột bị phân hủy và oxi hoá thành ancol etylic nên có mùi rượu.
- Để rượu lâu trong không khí sẽ bị oxi hoá chậm bởi oxi không khí tạo thành axit axetic (vị chua)
- Lông cừu được tạo thành từ các hợp chất thuộc loại amit (-CO-NH-) nên dễ bị thuỷ phân trong môi trường kiềm, do đó không nên giặt bằng xà phòng có tính kiềm cao.
Đúng 0
Bình luận (0)
CÂU 1:Hòa tan 13 gam kẽm vào dung dịch chứa 21,9 gam A xit clohidric HCI.C, viết PTHH xảy ra.B, tính thể tích khí hidro thoát ra ở đktc.C,nếu dẫn khí hidro nói trên vào bình chứa 12 gam hỗn hợp gồm CuO và Fe2O3 nung nóng. Tính khối lượng của từng kim loại thu được sau phản ứngCÂU 2: Trình bày phương pháp đơn giản nhất để nhận biết các hóa chất đựng trong các bình bị mất nhãn gồm; HCI; NaOH; NaCI; H2O.MONG ANH CHỊ GIẢI CHO E Ạ, E ĐANG CẦN GẤP TRONG TỐI NAY Ạ. E CẢM ƠN
Đọc tiếp
CÂU 1:Hòa tan 13 gam kẽm vào dung dịch chứa 21,9 gam A xit clohidric HCI.
C, viết PTHH xảy ra.
B, tính thể tích khí hidro thoát ra ở đktc.
C,nếu dẫn khí hidro nói trên vào bình chứa 12 gam hỗn hợp gồm CuO và Fe2O3 nung nóng. Tính khối lượng của từng kim loại thu được sau phản ứng
CÂU 2: Trình bày phương pháp đơn giản nhất để nhận biết các hóa chất đựng trong các bình bị mất nhãn gồm; HCI; NaOH; NaCI; H2O.
MONG ANH CHỊ GIẢI CHO E Ạ, E ĐANG CẦN GẤP TRONG TỐI NAY Ạ. E CẢM ƠN
Câu 2.
a.
\(n_{Zn}=\dfrac{13}{65}=0,2mol\)
\(n_{HCl}=\dfrac{21,9}{36,5}=0,6mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2 < 0,6 ( mol )
0,2 0,2 ( mol )
\(V_{H_2}=0,2.22,4=4,48l\)
b.
Gọi \(\left\{{}\begin{matrix}n_{CuO}=x\\n_{Fe_2O_3}=y\end{matrix}\right.\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
x x x ( mol )
\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
y 3y 2y ( mol )
Ta có:
\(\left\{{}\begin{matrix}80x+160y=12\\x+3y=0,2\end{matrix}\right.\) \(\rightarrow\left\{{}\begin{matrix}x=0,05\\y=0,05\end{matrix}\right.\)
\(\left\{{}\begin{matrix}m_{Cu}=0,05.64=3,2g\\m_{Fe}=0,05.56=2,8g\end{matrix}\right.\)
Câu 2.
Trích một ít mẫu thử và đánh dấu
Đưa quỳ tím vào 4 chất:
-HCl: quỳ hóa đỏ
-NaOH: quỳ hóa xanh
-NaCl,H2O: quỳ ko chuyển màu (1)
Cô cạn (1)
-NaCl : xuất hiện kết tinh
-H2O: bay hơi
Đúng 3
Bình luận (1)
Tổng số hạt proton nowtron electron trong nguyên tử là 26 trong hạt nhân đó số hạt ko mang điện tích >số hạt mang điện là 2 .Tính số hạt mỗi loại 🤨🤔
Ta có: `p + n + e = 26`
Mà `p = e`
`=> 2p + n = 26` `(1)`
Vì số hạt không mang điện lớn hơn số hạt mang điện là `2`
`=> n - 2p = 2` `(2)`
Từ `(1) ; ( 2) =>{(p = 6 = e),(n=14):}`
Đúng 4
Bình luận (1)
có số hạt mang điện tích nhiều hơn số hạt không mạng điện là 2 hạt
=> n- 2p = 2
n=2p + 2 (1)
mà tổng số hạt là 26
=> p + e + n = 26
hay 2p+n = 26 (2)
thay (1) vào (2) ta có
2p + 2p + 2 = 26
4p = 24
p=6
=> p=e = 7
n = 14
Đúng 3
Bình luận (1)
Câu 11: Hoá trị của cacbon, oxi, hiđro trong hợp chất hữu cơ lần lượt là:
A. IV, II, II. B. IV, II, I. C. II, IV, I. D. IV, III, I
Xem thêm câu trả lời
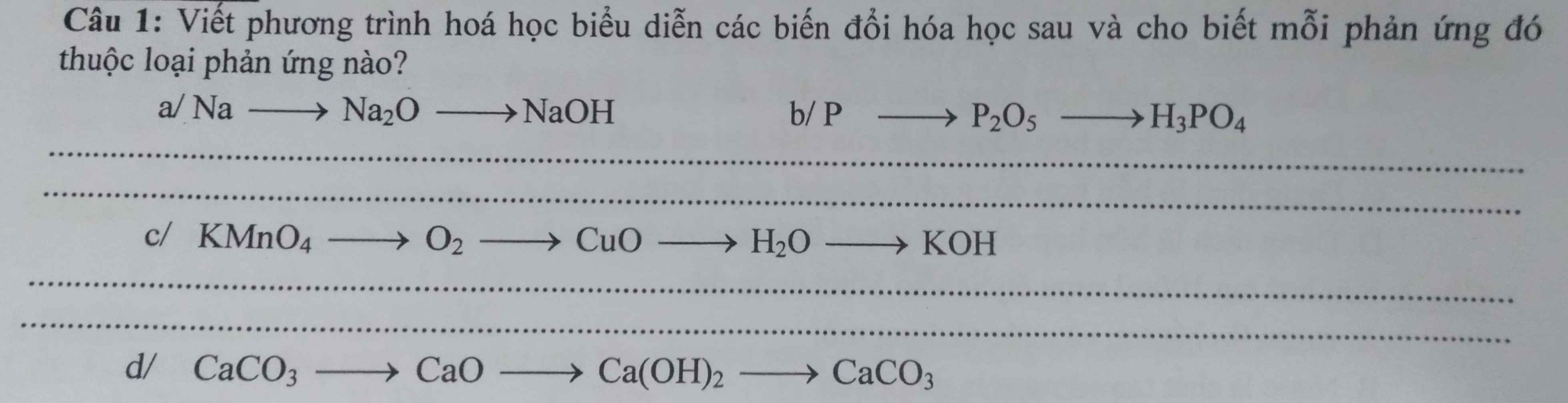
\(a,4Na+O_2\underrightarrow{t^o}2Na_2O\\ Na_2O+H_2O\rightarrow2NaOH\\ b,4P+5O_2\underrightarrow{t^o}2P_2O_5\\ P_2O_5+3H_2O\rightarrow2H_3PO_4\\ c,2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\\ 2Cu+O_2\underrightarrow{t^o}2CuO\\ CuO+H_2\underrightarrow{t^o}Cu+H_2O\\ H_2O+K_2O\rightarrow2KOH\)
Đúng 3
Bình luận (1)
a.
\(4Na+O_2\rightarrow\left(t^o\right)2Na_2O\)
\(Na_2O+H_2O\rightarrow2NaOH\)
b.
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
c.
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
\(2Cu+O_2\rightarrow\left(t^o\right)2CuO\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
\(K_2O+H_2O\rightarrow2KOH\)
d.
\(CaCO_3\rightarrow\left(t^o\right)CaO+CO_2\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
Đúng 2
Bình luận (0)