giúp tôi làm câu này với, nghe nó khó quá
(Mệnh đề nào đúng, mệnh đề nào sai)Câu 5: Nylon-6,6 một loại polymer tổng hợp, được sử dụng phổ biến trong các ngành công nghiệp khác nhau, bởi các đặc tính đặc biệt và phạm vi ứng dụng rộng rãi của nó. Nó được xem là một trong những loại nhựa kỹ thuật được sử dụng phổ biến nhất. Nylon-6,6 là một polymer được tổng hợp từ adipic acid và và hexamethylenediamine.a. Nylon-6,6 được tổng hợp bằng phương pháp trùng ngưng.b. Trong một mắt xích của nylon-6,6, nguyên tố carbon chiếm 31,86% về khối lượng.c...
Đọc tiếp
(Mệnh đề nào đúng, mệnh đề nào sai)
Câu 5: Nylon-6,6 một loại polymer tổng hợp, được sử dụng phổ biến trong các ngành công nghiệp khác nhau, bởi các đặc tính đặc biệt và phạm vi ứng dụng rộng rãi của nó. Nó được xem là một trong những loại nhựa kỹ thuật được sử dụng phổ biến nhất. Nylon-6,6 là một polymer được tổng hợp từ adipic acid và và hexamethylenediamine.
a. Nylon-6,6 được tổng hợp bằng phương pháp trùng ngưng.
b. Trong một mắt xích của nylon-6,6, nguyên tố carbon chiếm 31,86% về khối lượng.
c. Nylon-6,6 thuộc loại poliamide bền với nhiệt nhưng kém bền trong môi trường acid hoặc base.
d. Vải nylon-6,6 có thể giặt chung với xà phòng có độ kiềm cao.
Câu 5: Nylon-6,6 một loại polymer tổng hợp, được sử dụng phổ biến trong các ngành công nghiệp khác nhau, bởi các đặc tính đặc biệt và phạm vi ứng dụng rộng rãi của nó. Nó được xem là một trong những loại nhựa kỹ thuật được sử dụng phổ biến nhất. Nylon-6,6 là một polymer được tổng hợp từ adipic acid và và hexamethylenediamine.
a. Nylon-6,6 được tổng hợp bằng phương pháp trùng ngưng. (Đúng)
b. Trong một mắt xích của nylon-6,6, nguyên tố carbon chiếm 31,86% về khối lượng.
(Sai)=>`(C_12H_22N_2O_2)_n=>%_(mC)=63,72%`
c. Nylon-6,6 thuộc loại poliamide bền với nhiệt nhưng kém bền trong môi trường acid hoặc base. (Đúng)
d. Vải nylon-6,6 có thể giặt chung với xà phòng có độ kiềm cao. (Sai)
Đúng 2
Bình luận (0)
Amoxicillin là thuốc kháng sinh có thể dùng để điều trị nhiễm khuẩn đường hô hấp trên, đường tiết niệu… Nồng độ tối thiểu có thể kháng khuẩn là 0,04 mg/1kg thể trọng. Khi kê đơn cho một bệnh nhân nặng 50kg, bác sĩ kê đơn mỗi lần uống 1 viên thuốc (có hàm lượng Amoxicilin 500 mg/viên). Bệnh nhân cần uống các viên thuốc tiếp theo cách lần đầu bao nhiêu lâu? Biết rằng chu kì bán hủy của Amoxicilin trong cơ thể người là 61 phút. Giả thiết quá trình đào thải thuốc là phản ứng bậc 1.
Đọc tiếp
Amoxicillin là thuốc kháng sinh có thể dùng để điều trị nhiễm khuẩn đường hô hấp trên, đường tiết niệu… Nồng độ tối thiểu có thể kháng khuẩn là 0,04 mg/1kg thể trọng. Khi kê đơn cho một bệnh nhân nặng 50kg, bác sĩ kê đơn mỗi lần uống 1 viên thuốc (có hàm lượng Amoxicilin 500 mg/viên). Bệnh nhân cần uống các viên thuốc tiếp theo cách lần đầu bao nhiêu lâu? Biết rằng chu kì bán hủy của Amoxicilin trong cơ thể người là 61 phút. Giả thiết quá trình đào thải thuốc là phản ứng bậc 1.
Ở nhiệt độ cơ thể người là 370C và dưới áp suất khí nitrogen trong khí quyển là 0,78 bar, độ tan của khí nitrogen trong máu là 15,6 mL. Trong quá trình lặn, áp suất không khí trong buồng phổi tăng, đồng thời độ tan của khí nitrogen trong máu cũng tăng và tỉ lệ thuận với áp suất khí quyển.a) Ở độ sâu 30 m, áp suất khí nitrogen là 3,12 bar thì độ tan của khí nitrogen trong máu là bao nhiêu?b) Tính thể tích khí nitrogen trong máu cần thoát ra khi người thợ lặn đang ở độ sâu 30 m ngoi lên mặt nước....
Đọc tiếp
Ở nhiệt độ cơ thể người là 370C và dưới áp suất khí nitrogen trong khí quyển là 0,78 bar, độ tan của khí nitrogen trong máu là 15,6 mL. Trong quá trình lặn, áp suất không khí trong buồng phổi tăng, đồng thời độ tan của khí nitrogen trong máu cũng tăng và tỉ lệ thuận với áp suất khí quyển.
a) Ở độ sâu 30 m, áp suất khí nitrogen là 3,12 bar thì độ tan của khí nitrogen trong máu là bao nhiêu?
b) Tính thể tích khí nitrogen trong máu cần thoát ra khi người thợ lặn đang ở độ sâu 30 m ngoi lên mặt nước. Biết ở 370C và 1 bar, 1 mol khí chiếm thể tích là 25,4 L và giả thiết tổng lượng máu trong cơ thể người thợ lặn là 5 L.
c) Trường hợp người thợ lặn ngoi lên quá nhanh, khí nitrogen không kịp chuyển ra phổi để thoát ra ngoài, tạo các bọt khí gây tắc nghẽn mạch máu. Đây là bệnh gì? Nó gây tác hại gì?
Thủy phân hoàn toàn 26,1 gam chất béo E trong dung dịch NaOH, thu được glycerol và hỗn hợp Y chứa các muối stearate, oleate và palmitate của sodium với tỉ lệ mol tương ứng là 5: 2: 2. Tính số lodine của chất béo E, biết rằng số lodine là số gam I2 cần thiết để cộng vào 100 gam chất béo.
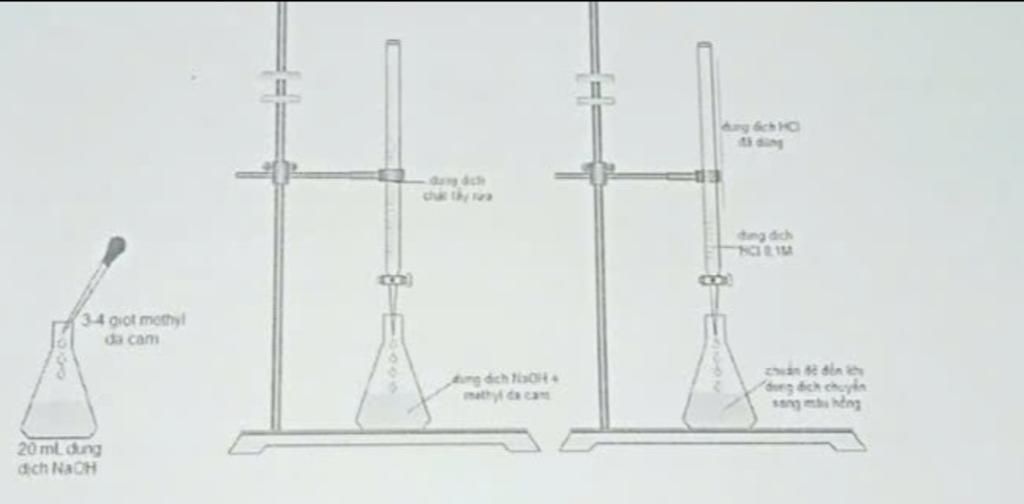
Chất tẩy rửa thông dụng thường có chứa hydrochloric acid. Lấy 25 ml. chất tẩy rửa pha thành 250 mL trong bình định mứcCho 20 ml dung dịch sodium carbonate 0,448M vào bình nón. Thêm chỉ thị methyl da cam vào bình và chuẩn độ bàng dung dịch tẩy rửa đã pha loãng bên trên. Tiến hành chuẩn độ đến khi nào chỉ thị từ màu vàng sang màu hồng, sau 3 lần chuẩn độ thì thể tích chất tẩy rửa trung bình đã dùng là 19,84 mL. Tính nồng độ hydrochloric acid trong chất tẩy rửa
Đọc tiếp
Chất tẩy rửa thông dụng thường có chứa hydrochloric acid. Lấy 25 ml. chất tẩy rửa pha thành 250 mL trong bình định mức
Cho 20 ml dung dịch sodium carbonate 0,448M vào bình nón. Thêm chỉ thị methyl da cam vào bình và chuẩn độ bàng dung dịch tẩy rửa đã pha loãng bên trên. Tiến hành chuẩn độ đến khi nào chỉ thị từ màu vàng sang màu hồng, sau 3 lần chuẩn độ thì thể tích chất tẩy rửa trung bình đã dùng là 19,84 mL. Tính nồng độ hydrochloric acid trong chất tẩy rửa
Mọi người giúp mình giải bài này với, mình cảm ơn nhiều ạ 🤧
Hòa tan 10g CuSO4.5 H20 vào 90 g
nước. Tính C% của dung dịch thu được
Ta có: \(n_{CuSO_4}=n_{CuSO_4.5H_2O}=\dfrac{10}{250}=0,04\left(mol\right)\)
⇒ mCuSO4 = 0,04.160 = 6,4 (g)
m dd CuSO4 = 10 + 90 = 100 (g)
\(\Rightarrow C\%_{CuSO_4}=\dfrac{6,4}{100}.100\%=6,4\%\)
Đúng 2
Bình luận (0)
a) Ở trạng thái \(1:\left\{{}\begin{matrix}P_1=3.10^5\left(Pa\right)\\V_1=8\left(lít\right)=8.10^{-3}\left(m^3\right)\end{matrix}\right.\)
Ở trạng thái \(2:\left\{{}\begin{matrix}P_2=P_1=3.10^5\left(đẳng.áp\right)\\V_2=1,25.V_1=1,25.8.10^{-3}=10^{-2}\left(lít\right)\end{matrix}\right.\)
Công mà khí thực hiện được trong quá trình đẳng áp:
\(A=P\Delta V=P=\left(V_2-V_1\right)=3.10^5\left(10^{-2}-8.10^{-3}\right)=600\left(J\right)\)
b) Áp dụng định luật bảo toàn năng lượng:
\(\Delta U=A+Q\)
\(\Rightarrow Q=\Delta U-A=200-600=-400\left(J\right)< 0\)
\(\Rightarrow\) Khối khí truyền 1 nhiệt lượng bằng \(400\left(J\right)\)
Đúng 2
Bình luận (0)
Chọn Cellulase
Cellulase: Đây là enzyme chuyên biệt để phân hủy cellulose, một thành phần chính cấu tạo nên thành tế bào thực vật. Cellulose là chất xơ mà động vật ăn cỏ thường tiêu thụ nhiều
Amylase: Enzyme này có chức năng phân hủy tinh bột thành đường đơn giản để cơ thể dễ hấp thụ. Tinh bột cũng là một loại carbohydrate, nhưng cấu trúc của nó khác với cellulose
Đúng 1
Bình luận (0)

















