 giúp min
giúp min giúp mình với ạ
giúp mình với ạ
Câu 1: Cấu hình electron của:- Nguyên tử X: 1s22s22p63s23p64s1;- Nguyên tử Y: 1s22s22p63s23p4.Số hạt mang điện trong nguyên tử X nhiều hơn số hạt mang điện trong nguyên tử Y bao nhiêu hạt?
Đọc tiếp
Câu 1: Cấu hình electron của:
- Nguyên tử X: 1s22s22p63s23p64s1;
- Nguyên tử Y: 1s22s22p63s23p4.
Số hạt mang điện trong nguyên tử X nhiều hơn số hạt mang điện trong nguyên tử Y bao nhiêu hạt?
X:38 hạt mang điện
Y:32 hạt mang điện
Hạt mang điện của X nhiều hơn Y là 6
Đúng 1
Bình luận (0)
X:38 hạt mang điện (K) Y:32 hạt mang điện (S)
số hạt mang điện trong nguyên tử X nhiều hơn số hạt mang điện trong nguyên tử Ylà 6 hạt
Đúng 0
Bình luận (0)
Tại sao 3d9 4s1 thuộc nhóm IB
3d8 4s2 thuộc nhóm VIIIB(lớp ngoài cùng đều là 10e)
Bạn xem lại nha, \(3d^94s^1\)là cấu hình ko bền,rất khó tồn tại, nhóm IB có 1 cấu hình gần tương tự của \(Cu:\left[Ar\right]3d^{10}4s^1\):cấu hình này có số e hoá trị là 1 (do phân lớp sát ngoài cùng đã bảo hoà) + với đây là nguyên tố d nên thuộc lớp \(IB\) là hợp lí nè
-Còn \(\left[Ar\right]3d^84s^2\) có số e hoá trị là 10 (2 từ lớp ngoài cùng + 8 từ phân lớp sát ngoài cùng chưa bão hoà) thêm với đây là nguyên tố d
=> NHóm \(VIIIB\) là hoàn toàn hợp lí nhé
Đúng 1
Bình luận (1)
Tổng số hạt p, n, e của hai nguyên tử kim loại X, Y là 142 ,trong đó tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 42. Số hạt mang điện của nguyên tử Y nhiều hơn của X là 12. Tổng số hạt mang điện trong kim loại X là?
Giúp em với ạ
Tổng số hạt trong hai nguyên tử là: \(2p\left(X\right)+n\left(X\right)+2p\left(Y\right)+n\left(Y\right)=142\left(1\right)\)
Tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là
\(2p\left(X\right)+2p\left(Y\right)-n\left(X\right)-n\left(Y\right)=42\left(2\right)\)
Số hạt mang điện của nguyên tử Y nhiều hơn nguyên tử X là
\(2p\left(Y\right)=2p\left(X\right)+12\Leftrightarrow p\left(Y\right)=p\left(X\right)+6\left(3\right)\)
\(\left(1\right);\left(2\right);\left(3\right)\Rightarrow\left\{{}\begin{matrix}2p\left(X\right)+n\left(X\right)+2p\left(Y\right)+n\left(Y\right)=142\\2p\left(X\right)+2p\left(Y\right)-n\left(X\right)-n\left(Y\right)=42\\p\left(Y\right)=p\left(X\right)+6\end{matrix}\right.\)
\(\Leftrightarrow2p\left(X\right)=40\Leftrightarrow p\left(X\right)+e\left(X\right)=40\left(hạt\right)\)
Đúng 1
Bình luận (0)
\(\left[{}\begin{matrix}2p_x+n_x+2p_y+n_y=142\\2p_x+2p_y-n_x-n_y=42\end{matrix}\right.\)
\(\Leftrightarrow4p_x+4p_y=184\left(1\right)\)
\(2p_y-2p_x=12\Leftrightarrow-2p_x+2p_y=12\left(2\right)\)
\(\text{Từ (1) và (2):}\left\{{}\begin{matrix}4p_x+4p_y=184\\-2p_x+2p_y=12\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}p_x=20\\p_y=26\end{matrix}\right.\)
\(\text{Vậy số hạt mang điện trong kim loại X là 40 hạt
}\)
Đúng 0
Bình luận (0)
A,B là 2 nguyên tố thuộc 2 chu kì liên tiếp và cùng nhóm, tổng số proton trong hạt nhân của A, B là 24
a) Xác định vị trí của A,B trong bảng tuần hoàn, cho biết tên của A và B.
b) Cho biết A, B là kim loại hay phi kim? Để đạt cấu hình e của khí hiếm, A và B có khuynh hướng gì? Viết quá trình nhường hay nhận e và viết cấu hình e của ion tạo thành ?
a) \(Z\left(A\right)+Z\left(B\right)=24\); \(A;B\) thuộc 2 chu kỳ liên tiếp và cùng 1 nhóm, dựa vào bảng HTTH ta được :
\(A\) là \(O\left(Z=8\right)\rightarrow Chu.kỳ2;nhómVIA\)
\(B\) là \(S\left(Z=16\right)\rightarrow Chu.kỳ3;nhómVIA\)
b) Cả \(O;S\) đều là phi kim vì thuộc nhóm \(VIA\)
\(\left(O\right):1s^22s^22p^4+2e\rightarrow1s^22s^22p^6\rightarrow O^{2-}\)
\(\left(S\right):1s^22s^22p^63s^23p^4+2e\rightarrow1s^22s^22p^63s^23p^6\rightarrow S^{2-}\)
Vậy để đạt cấu hình electron bền vững (khí hiếm) \(O;S\) đều nhận \(2\) electron và tạo thành ion âm \(O^{2-};S^{2-}\)
Đúng 2
Bình luận (0)
Tổng số hạt proton, neutron và electron tạo nên phân tử M2X là 116, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 36. Số khối của X lớn hơn số khối của M là 9 . Tổng các loại hạt trong X mũ 2- nhiều hơn trong M + là 17 .Số khối của m là?
Giúp em vs ạ 🥹🥹
Do nguyên tử trung hòa về điện nên P = E
- Tổng số hạt trong M2X là 116.
⇒ 2.2PM + 2NM + 2PX + NX = 116 (1)
- Số hạt mang điện nhiều hơn số hạt không mang điện là 36.
⇒ 2.2PM + 2PX - 2NM - NX = 36 (2)
- Số khối của X lớn hơn số khối của M là 9.
⇒ PX + NX - PM - NM = 9 (3)
- Tổng số hạt trong X2- nhiều hơn M+ là 17.
⇒ (2PX + NX + 2) - (2PM + NM - 1) = 17 (4)
Từ (1), (2), (3) và (4) \(\Rightarrow\left\{{}\begin{matrix}P_M=E_M=11\\N_M=12\\P_X=E_X=16\\N_X=16\end{matrix}\right.\)
⇒ AM = 11 + 12 = 23
Đúng 1
Bình luận (0)
A , B là hai nguyên tử của hai nguyên tố. tổng số hạt cơ bản của A và B là 191, hiệu số hạt cơ bản của a và b là 153. Biết số hạt không mang điện trong A gấp 10 lần số hạt không mang điện trong B. Số hạt mang điện trong a là?
Giúp em với ạ 🥺
Do nguyên tử trung hòa về điện nên P = E.
- Tổng số hạt của A và B là 191.
⇒ 2PA + NA + 2PB + NB = 191 (1)
- Hiệu số hạt của A và B là 153.
⇒ 2PA + NA - 2PB - NB = 153 (2)
Từ (1) và (2) ⇒ \(\left\{{}\begin{matrix}2P_A+N_A=172\\2P_B+N_B=19\end{matrix}\right.\)
⇒ NB = 19 - 2PB
Mà: 1 ≤ \(\dfrac{N_B}{P_B}\) ≤ 1,5 ⇒ 1≤ \(\dfrac{19-2P_B}{P_B}\) ≤ 1,5
⇒ 5,4 ≤ PB ≤ 6,3 ⇒ PB = 6
⇒ NB = 19 - 2PB = 7
Mà: Số hạt không mang điện trong A gấp 10 lần B.
⇒ NA = 7.10 = 70
⇒ Số hạt mang điện trong A là: 172 - 70 = 102
Đúng 1
Bình luận (2)
MN cho mình hỏi cách bấm mày tính casio fx 580 4 ẩn phương trình ntn như nào với:
ZX + NX + 2.(2ZM + NM ) = 140
2ZX + 4ZM - NX- 2.NM = 44
ZM + NM - ( ZX + NX) = 23
(2.ZM + NM -1)- (2ZX + NX +2)= 31
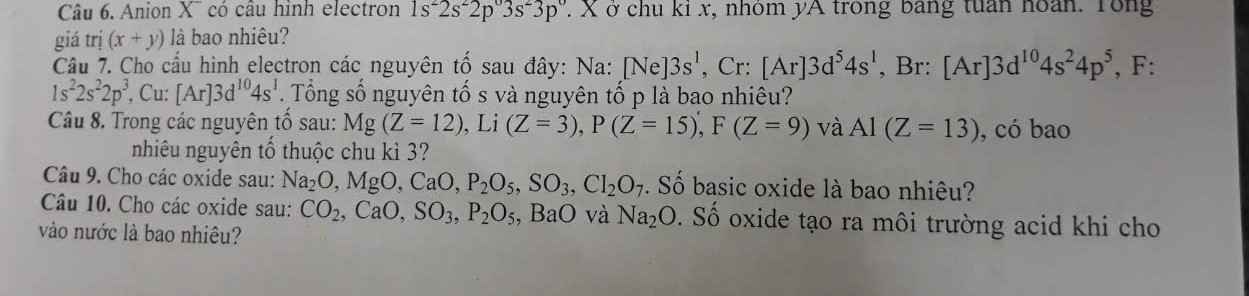 2 coin ạ
2 coin ạ
Câu 7 :
\(Na\) có lớp ngoài cùng là \(3s^1\rightarrow\) nguyên tố \(s\)
\(Cr\) có lớp ngoài cùng là \(4s^1\rightarrow\) nguyên tố \(s\)
\(Br\) có lớp ngoài cùng là \(4p^5\rightarrow\) nguyên tố \(p\)
\(F\) có lớp ngoài cùng là \(2p^5\rightarrow\) nguyên tố \(p\)
\(Cu\) có lớp ngoài cùng là \(4s^1\rightarrow\) nguyên tố \(s\)
\(\Rightarrow\) Nguyên tố \(s:Na;Cr;Cu\)
Nguyên tố \(p:Br;F\)
Tổng số nguyên tố \(s;p:3+2=5\)
Câu 8 : Dựa vào bảng HTTH ta thấy có 3 nguyên tố thuộc chu kỳ 3 là \(Mg;P;Al\)
Câu 9 : Basic oxide là \(Na_2O;MgO;CaO\Rightarrow\) có \(3\) Basic oxide
Câu 10 : Có \(3\) oxide tạo ra môi trường acid khi cho vào nước là \(CO_2;SO_3;P_2O_5\)
Đúng 0
Bình luận (0)
Một phân tử DNA có cấu trúc xoắn kép giả sử phân tử DNA này có tỉ lệ (A+T)/(G+C) = 1/5 thì tỉ lệ nucleptide loại G của phân tử ADN này là bao nhiêu ?

















