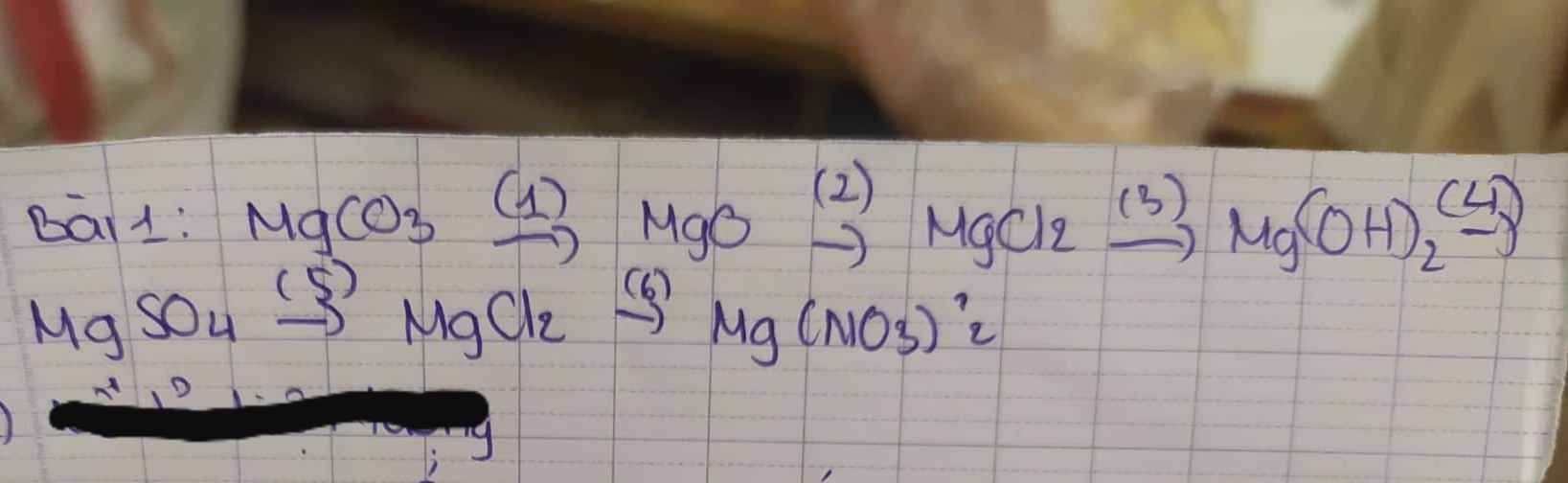al và fe là kim loại vận đụng nhiều trong cuộc sống nhưng nhôm đề ngoài không bị sét còn sắt thì thì bị sét ?
Đề kiểm tra 1 tiết chương I : Các loại hợp chất vô cơ-Đề 2
Khi sắt bị gỉ sẽ tạo nên một lớp oxit sắt xốp, oxy có thể lọt qua lớp sắt oxit mà tiếp xúc với lớp sắt kim loại bên trong lớp sắt oxit và gây gỉ tiếp tục. Nhôm thì không giống như vậy: Khi nhôm tác dụng với oxy sẽ tạo thành một lớp nhôm oxit (Al2O3)
Đúng 0
Bình luận (0)
để có được 2,7 tấn nhôm nguyên chất cần bao nhiêu tấn quặng boxit chứa 80% nhôm oxit. Biết hiệu suất H của quá trình là 90%
2,7 tấn = 2700 kg
$n_{Al} = \dfrac{2700}{27} = 100(kmol)$
$\Rightarrow n_{Al_2O_3} = \dfrac{1}{2}n_{Al} = 50(kmol)$
$m_{Al_2O_3} = 50.102 = 5100(kg)$
$\Rightarrow m_{Al_2O_3\ đã\ dùng} = 5100 : 90\% = 5666,67(kg)$
$\Rightarrow m_{boxit} = 5666,67 : 80\% = 7083,3375(kg)$
Đúng 1
Bình luận (0)
Viết PTHH biểu diễn sự chuyển đổi sau:
\(FeCl_3->FeSO_4->Fe_2O_3->Fe->Fe_3O_4\)
nhiệt phân hoàn toàn m(g) Zn(oh)2 thu đc 4,05g zno a) tính khối lượng m b) trung hoà 200g dd h2so4 9% bằng lượng Zn(oh)2 như trên. Tính C% các chất sau pứ
\(Zn\left(OH\right)_2\xrightarrow[]{t^o}ZnO+H_2O\)
\(ZnO+H_2SO_4\xrightarrow[]{}ZnSO_4+H_2O\)
a) \(n_{Zn\left(OH\right)_2}=n_{ZnO}=\dfrac{4,05}{81}=0,05\left(mol\right)\)
\(m_{Zn\left(OH\right)_2}=0,05.99=4,95\left(g\right)\)
b) \(m_{H_2SO_4}=\dfrac{200.9}{100}=18\left(g\right)\)
\(n_{H_2SO_4}=\dfrac{18}{98}\approx0,18\left(mol\right)\)
Tỉ lệ: \(\dfrac{0,05}{1}< \dfrac{0,18}{1}\)
⇒ \(H_2SO_4\) dư. Dùng số mol \(Zn\left(OH\right)_2\) để tính
\(n_{H_2SO_4pứ}=n_{ZnSO_4}=n_{Zn\left(OH\right)_2}=0,05\left(mol\right)\)
Theo BTKL: \(m_{Zn\left(OH\right)_2}+m_{ddH_2SO_4}=m_{ddsau}\)
⇒ \(m_{ddsau}=4,95+200=204,95\left(g\right)\)
\(C\%_{ZnSO_4}=\dfrac{0,05.161}{204,95}.100=3,98\%\)
\(C\%_{H_2SO_4}=\dfrac{\left(0,18-0,05\right).98}{204,95}.100=6,22\%\)
Đúng 1
Bình luận (0)
cho a gam SO2 vào 100ml dung dịch Ba(OH)2 2M phản ứng xong thu được 19,7 gam kết tủa xác định a
PTHH : SO2 + Ba(OH)2 -> BaSO3 \(\downarrow\)+ H2O
\(\dfrac{197}{2330}\) \(\dfrac{197}{2330}\)
\(n_{Ba\left(OH\right)_2}=2.0,1=0,2\left(mol\right)\)
\(n_{BaSO_4}=\dfrac{19.7}{233}=\dfrac{197}{2330}\left(mol\right)\)
Ta thấy : Ba(OH)2 dư
\(m_{SO_2}=\dfrac{197}{2330}.64=\dfrac{6304}{1165}\left(g\right)\)
Đúng 2
Bình luận (0)
Cho A là oxit, B là muối, C là kim loại, D là phi kim. Hãy chọn chất thích hợp với A, B, C, D và hoàn thành PTHH của các phản ứng sau:
1. A + HCl \(\rightarrow\)2 muối + H2O
2. B + NaOH \(\rightarrow\) 2 muối + H2O
3. C + muối \(\rightarrow\)1 muối
4. D+axit\(\rightarrow\)3oxit
1. Fe3O4 + HCl \(\rightarrow\) 2FeCl3 + FeCl2 + H2O
2. CaHCO3 + NaOH \(\rightarrow\) Na2CO3 + CaCO3 + H2O
3. FeCl2 + Fe \(\rightarrow\) 3FeCl2
4. S + HNO3 \(\rightarrow\) SO2 + NO2 + H2O
Đúng 2
Bình luận (0)
$\rm 1.Fe_3O_4 + 8HCl \rightarrow FeCl_2 + 2FeCl_3 + 4H_2O$
$\rm 2.Ca(HCO_3)_2 + 2NaOH \rightarrow CaCO_3 \downarrow + Na_2CO_3 + 2H_2O$
$\rm 3.2FeCl_3 + Fe \rightarrow 3FeCl_2$
$\rm 4.C + 2H_2SO_{4(đặc)} \rightarrow CO_2 \uparrow + 2SO_2 \uparrow + 2H_2O$
Đúng 2
Bình luận (0)
Nhận biết các lọ mất nhãn chứa dd sau:Cacl2,Ca(No3)2,Ca(Oh)2,Na2So4
GIUP MINH Ạ:((
- Trích một ít các dd làm mẫu thử
- Cho các dd tác dụng với giấy quỳ tím:
+ QT chuyển xanh: Ca(OH)2
+ QT không chuyển màu: CaCl2, Ca(NO3)2, Na2SO4 (1)
- Cho các dd ở (1) tác dụng với dd BaCl2:
+ Không hiện tượng: CaCl2, Ca(NO3)2 (2)
+ Kết tủa trắng: Na2SO4
\(Na_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2NaCl\)
- Cho các dd ở (2) tác dụng với dd AgNO3:
+ Không hiện tượng: Ca(NO3)2
+ Kết tủa trắng: CaCl2
\(CaCl_2+2AgNO_3\rightarrow Ca\left(NO_3\right)_2+2AgCl\downarrow\)
- Dán nhãn
Đúng 2
Bình luận (1)
mgco3---t-->mgo + co2
mgo +2hcl---->mgcl2 + h2o
mgcl2+2naoh---->mg(oh)2+2nacl
mg(oh)2+h2so4---->mgso4 + 2h2o
mgso4 + 2hcl------>mgcl2 + h2so4
mgcl2 + 2hno3----->mg(no3)2 + 2hcl
Đúng 0
Bình luận (0)
Cho 4,8g kim loại magie(Mg) tác dụng với H2SO4 0,5 M a)tính thể tích khí sinh ra ở đktc b)tính thể tích dd axit H2SO4 đã dùng
a) \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PTHH: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
0,2----->0,2------>0,2---->0,2
=> \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b) \(V_{dd.H_2SO_4}=\dfrac{0,2}{0,5}=0,4\left(l\right)\)
Đúng 1
Bình luận (0)
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
Trường hợp 1: Nếu axit sunfuric loãng.
\(Mg+H_2SO_4\text{ (loãng)}\xrightarrow[]{}MgCl_2+H_2\uparrow\)
0,2 → 0,2 → 0,2
a) \(V_{H_2}=0,2\cdot22,4=4,48\left(l\right)\)
b) \(V_{H_2SO_4\text{ (loãng)}}=\dfrac{0,2}{0,5}=0,4\left(l\right)\)
Trường hợp 2: Nếu axit sunfuric đặc.
\(Mg+2H_2SO_4\text{(đặc)}\xrightarrow[]{}MgSO_4+SO_2\uparrow+2H_2O\)
0,2 → 0,4 → 0,2
a) \(V_{SO_2}=0,2\cdot22,4=4,48\left(l\right)\)
b) \(V_{H_2SO_4\text{ (đặc)}}=\dfrac{0,4}{0,5}=0,8\left(M\right)\) (Loại, vì 0,8M là dd loãng)
Đúng 0
Bình luận (0)
3) Trộn 100ml dd CaCl2 0,2 M với 100ml dd AgNO3 0,3ml
a) Cho biết hiện tượng quan sát được và viết PTHH
b) Tính khối lượng chất rắn sinh ra
c ) Tính CM của chất còn lại trong dd sau phản ứng . Biế thể tích dd thay đổi không đáng kể
a) Hiện tượng: Có kết tủa trắng xuất hiện
\(\left\{{}\begin{matrix}n_{CaCl_2}=0,1.0,2=0,02\left(mol\right)\\n_{AgNO_3}=0,3.0,1=0,03\left(mol\right)\end{matrix}\right.\)
PTHH: \(2AgNO_3+CaCl_2\rightarrow2AgCl\downarrow+Ca\left(NO_3\right)_2\)
Ban đầu: 0,03 0,02
Pư: 0,03-------->0,015
Sau pư: 0 0,005 0,03 0,015
b) \(m_{c.rắn}=m_{AgCl}=0,03.143,5=4,305\left(g\right)\)
c) \(\left\{{}\begin{matrix}C_{M\left(CaCl_2.dư\right)}=\dfrac{0,005}{0,1+0,1}=0,025M\\C_{M\left(Ca\left(NO_3\right)_2\right)}=\dfrac{0,015}{0,1+0,1}=0,075M\end{matrix}\right.\)
Đúng 3
Bình luận (0)