Cho a gam hỗn hợp gồm Zn và Al vào dung dịch axit clohiđric (HCl) dư. Sau phản ứng thu được 3,36 lít H2 ở đktc. Tính a?
Hóa học
\(n_{H_2}=\dfrac{3.36}{22.4}=0,15\left(mol\right)\)
PTHH : Zn + 2HCl -> ZnCl2 + H2 ( 1)
0,15 0,15
PTHH : 2Al + 6HCl -> 2AlCl3 + 3H2 ( 2 )
0,1 0,15
\(m_{Zn}=0,15.65=9,75\left(g\right)\)
\(m_{Al}=27.0,1=2,7\left(g\right)\)
\(m_{hh}=9,75+2,7=12,45\left(g\right)\)
Đúng 3
Bình luận (0)
nH2=3,36:22,4=0,15(mol)
có PTHH:
Zn+2HCl--->ZnCl2+H2
0,15 0,15(mol)
2Al+6HCl--->2AlCl3+3H2
0,1 0,15(mol)
mAl=0,1x27=2,7(g)
mZn=0,15x65=9,75(g)
ma=2,7+9,75=12,45(g)
Đúng 3
Bình luận (4)
Câu1: A: hãy viết phương trình điều chế axetilen từ canxi cacbua cac2 B: hãy viết phương trình điều chế axetilen từ metan Câu 2: chi các chất sau: C₄H₁₀, C₄H₈, NaHCO₃, CaCo₃, C₃H₄,HNo₂, CuSo₄, C₂H₄. Hãy chỉ ra chất nào là chất vô cơ, chất nào là chất hữu cơ? Viết công thức cấu tạo của các chất hữu cơ đó Câu 3: A: có hỗn hợp khí gồm Co₂, CH₄. Hãy nêu phương pháp để thu được CH₄ tinh khiết B: có hỗn hợp khí gồm CH₄, C₂H₄. Hãy nêu phương pháp để thu được C₂H₄ tinh khiết Ai biết có thể giúp em được...
Đọc tiếp
Câu1: A: hãy viết phương trình điều chế axetilen từ canxi cacbua cac2 B: hãy viết phương trình điều chế axetilen từ metan Câu 2: chi các chất sau: C₄H₁₀, C₄H₈, NaHCO₃, CaCo₃, C₃H₄,HNo₂, CuSo₄, C₂H₄. Hãy chỉ ra chất nào là chất vô cơ, chất nào là chất hữu cơ? Viết công thức cấu tạo của các chất hữu cơ đó Câu 3: A: có hỗn hợp khí gồm Co₂, CH₄. Hãy nêu phương pháp để thu được CH₄ tinh khiết B: có hỗn hợp khí gồm CH₄, C₂H₄. Hãy nêu phương pháp để thu được C₂H₄ tinh khiết Ai biết có thể giúp em được ko ạ, em cảm ơn ạ. Trưa em bắt đầu thì rồi nên mọi người giúp em với ạ
Câu 1:
\(CaC_2 + 2H_2O \rightarrow Ca(OH)_2 + C_2H_2\\ 2CH_4 \xrightarrow[\text{làm lạnh nhanh}]{t^o} C_2H_2 + 3H_2\)
Câu 2:
HCHC: \(C_4H_{10}, C_4H_8, C_3H_4, C_2H_4\)
HCVC: Còn lại
CTCT:
\(C_4H_{10}:CH_3-CH_2-CH_2-CH_3\\ C_4H_8:CH_2=CH-CH=CH_2\)
\(C_3H_4:CH\equiv C-CH_3\\ C_2H_4:CH_2=CH_2\)
Câu 3:
Dẫn qua dd Ca(OH)2 dư, CO2 bị hấp thụ hết
\(CO_2 + Ca(OH)_2 \rightarrow CaCO_3 + H_2O\)
Đem hh đi đốt rồi làm lạnh nhanh, đun nóng có xúc tác Pd, hh thu được dẫn qua CuO nung nóng rồi dẫn qua dd H2SO4 đặc để làm khô
\(2CH_4 \xrightarrow[\text{làm lạnh nhanh}]{t^o} C_2H_2 + 3H_2\\ C_2H_2 + H_2 \xrightarrow[t^o]{Pd} C_2H_4\\ H_2 + CuO \xrightarrow{t^o} Cu + H_2O\)
Đúng 3
Bình luận (0)
Câu1:
A: hãy viết phương trình điều chế axetilen từ canxi cacbua cac2
B: hãy viết phương trình điều chế axetilen từ metan
Câu 2: chi các chất sau: C₄H₁₀, C₄H₈, NaHCO₃, CaCo₃, C₃H₄,HNo₂, CuSo₄, C₂H₄. Hãy chỉ ra chất nào là chất vô cơ, chất nào là chất hữu cơ? Viết công thức cấu tạo của các chất hữu cơ đó
Câu 3:
A: có hỗn hợp khí gồm Co₂, CH₄. Hãy nêu phương pháp để thu được CH₄ tinh khiết
B: có hỗn hợp khí gồm CH₄, C₂H₄. Hãy nêu phương pháp để thu được C₂H₄ tinh khiết
Ai biết có thể giúp em đ...
Đọc tiếp
Câu1: A: hãy viết phương trình điều chế axetilen từ canxi cacbua cac2 B: hãy viết phương trình điều chế axetilen từ metan Câu 2: chi các chất sau: C₄H₁₀, C₄H₈, NaHCO₃, CaCo₃, C₃H₄,HNo₂, CuSo₄, C₂H₄. Hãy chỉ ra chất nào là chất vô cơ, chất nào là chất hữu cơ? Viết công thức cấu tạo của các chất hữu cơ đó Câu 3: A: có hỗn hợp khí gồm Co₂, CH₄. Hãy nêu phương pháp để thu được CH₄ tinh khiết B: có hỗn hợp khí gồm CH₄, C₂H₄. Hãy nêu phương pháp để thu được C₂H₄ tinh khiết Ai biết có thể giúp em được ko ạ, em cảm ơn ạ
Bài 2:
Viết theo thứ tự bạn nhé :)
H2SO4, H2SO3, NaHCO3, NaOH, FeCl3, Fe2O3, Na2SiO3, CaCO3, Ca(H2PO4)2, Ca(HS)2
Bài 3:
CTHH: R2On
\(\rightarrow\%R=\dfrac{2M_R}{160}.100\%=70\%\\ \rightarrow M_R=56\left(\dfrac{g}{mol}\right)\)
=> R là Fe
=> 2.56 + 16n = 160
=> n = 3
CTHH Fe2O3 (sắt (III) oxit)
Đúng 1
Bình luận (0)
Bài 2.
Axit sunfuric: \(H_2SO_4\)
Axit sunfuro: \(H_2SO_3\)
Natri hidrocacbonat: \(NaHCO_3\)
Sắt (lll) clorua: \(FeCl_3\)
Sắt (ll) oxit: \(FeO\)
Natri silicat: \(Na_2SiO_3\)
Canxi cacbonat: \(CaCO_3\)
Canxi đihofhidrophotphat: \(Ca\left(H_2PO_4\right)_2\)
Đúng 2
Bình luận (0)
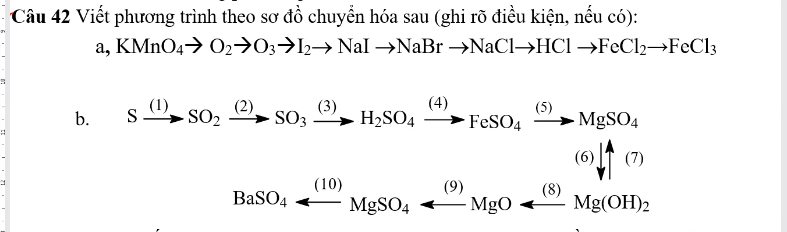
a)
2KMnO4 --to--> K2MnO4 + MnO2 + O2
3O2 --tia tử ngoại--> 2O3
O3 + 2KI + H2O --> 2KOH + I2 + O2
2Na + I2 --to--> 2NaI
Br2 + 2NaI --> 2NaBr + I2
Cl2 + 2NaBr --> 2NaCl + Br2
NaCl + H2SO4(đ) --to--> NaHSO4 + HCl
Fe + 2HCl --> FeCl2 + H2
2FeCl2 + Cl2 --> 2FeCl3
b)
(1) S + O2 --to--> SO2
(2) 2SO2 + O2 <--> 2SO3 (điều kiện chiều thuận: to, V2O5)
(3) SO3 + H2O --> H2SO4
(4) Fe + H2SO4 --> FeSO4 + H2
(5) FeSO4 + Mg --> Fe + MgSO4
(6) MgSO4 + 2NaOH --> Mg(OH)2 + Na2SO4
(7) Mg(OH)2 + H2SO4 --> MgSO4 + 2H2O
(8) Mg(OH)2 --to--> MgO + H2O
(9) MgO + H2SO4 --> MgSO4 + H2O
(10) MgSO4 + BaCl2 --> BaSO4 + MgCl2
Đúng 4
Bình luận (0)
 cau 10 giải chi tiết giúp mình nha
cau 10 giải chi tiết giúp mình nha
Câu 10:
\(a) n_{Zn} = \dfrac{3,25}{65} = 0,05 (mol)\\n_{CuO} = \dfrac{6}{80} = 0,075 (mol)\)
PTHH:
Zn + 2HCl ---> ZnCl2 + H2
0,05------------------------->0,05
CuO + H2 --to--> Cu + H2O
LTL: \(0,075>0,05\rightarrow\) CuO dư
b, Theo pthh: \(n_{CuO\left(pư\right)}=n_{Cu}=n_{H_2}=0,05\left(mol\right)\)
\(\rightarrow m_{Cu}=0,05.64=3,2\left(g\right)\)
\(c) \text{chất dư là CuO}\\ \rightarrow m_{CuO (dư)} = (0,075 - 0,05) . 80 = 2 (g)\)
Đúng 4
Bình luận (0)
10
\(n_{Zn}=\dfrac{3,25}{65}=0,05\left(mol\right)\)
\(n_{CuO}=\dfrac{6}{80}=0,075\left(mol\right)\)
\(pthh:Zn+HCl->ZnCl_2+H_2\)
0,05 0,05
\(pthh:CuO+H_2\underrightarrow{t^o}H_2O+Cu\)
LTL : \(\dfrac{0,075}{1}>\dfrac{0,05}{1}\)
=>> CuO dư
theo pthh : \(n_{Cu}=n_{H_2}=0,05\)(mol)
=> \(m_{Cu}=0,05.64=3,2\left(g\right)\)
=> \(m_{CuO\left(d\right)}=\left(0,075-0,05\right).80=2\left(g\right)\)
Đúng 3
Bình luận (0)
để oxi hóa hỗn hợp kim loại gồm 0,2 mol Al và 0,1 mol Mg cần phải dùng V lít (dktc) hỗn hợp clo và oxi. sau khi phản ứng kết tủa thu được 25,2 gam hh gồm oxit và muối. Vậy thể tích có trong hỗn hợp ban đầu là ( biết Cl= 35,5. O=16, Mg= 24, Al= 27)
A. 6,72 l B. 3,36 lít C. 2,24 lít D. 4,48 lít
help me !!!
\(\left\{{}\begin{matrix}Cl_2:x\left(mol\right)\\O_2:y\left(mol\right)\end{matrix}\right.\)
\(BTe:3n_{Al}+2n_{Mg}=2n_{Cl_2}+4n_{O_2}\)
\(\Rightarrow2x+4y=3\cdot0,2+0,1\cdot2=0,8\left(1\right)\)
\(BTKL:m_{muối}=m_{Al^{3+}}+m_{Mg^{2+}}+m_{Cl^-}+m_{O^{2-}}\)
\(\Rightarrow25,2=0,2\cdot27+0,1\cdot24+35,5\cdot2x+16\cdot2y\)
\(\Rightarrow71x+32y=17,4\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1mol\\y=0,1mol\end{matrix}\right.\)
\(V=V_{Cl_2}+V_{O_2}=0,1\cdot22,4+0,1\cdot22,4=4,48l\)
Chọn D
Đúng 1
Bình luận (0)
... "thể tích có trong hỗn hợp ban đầu" là thể tích của gì thế bn :)
Đúng 0
Bình luận (0)
 Giải giúp mình câu 10 ik giải chi tiết nha
Giải giúp mình câu 10 ik giải chi tiết nha
Đốt cháy hoàn toàn 7,6 gam hỗn hợp E gồm một axit cacboxylic X no, đơn chức, mạch
hở và một ancol Y đơn chức (có số nguyên tử cacbon trong phân tử khác nhau), thu được 0,3 mol
CO2 và 0,4 mol H2O. Thực hiện phản ứng este hóa 7,6 gam hỗn hợp X trên với hiệu suất 80%, thu
được m gam este Z. Xác định công thức của X, Y, Z và tính giá trị của m.
Do nCO2 > nH2O => Ancol Y no, đơn chức, mạch hở
=> E gồm CnH2nO2, CxH2x+2O
Gọi \(\left\{{}\begin{matrix}n_{C_nH_{2n}O_2}=a\left(mol\right)\\n_{C_xH_{2x+2}O}=b\left(mol\right)\end{matrix}\right.\)
Bảo toàn C: an + bx = 0,3 (*)
=> 2an + 2bx = 0,6 (1)
Bảo toàn H: 2an + 2bx + 2b = 0,8 (2)
nC = 0,3 (mol); nH = 0,8 (mol)
=> \(n_O=\dfrac{7,6-0,3.12-0,8.1}{16}=0,2\left(mol\right)\)
=> 2a + b = 0,2
(2) - (1) => 2b = 0,2 => b = 0,1 (mol)
=> a = 0,05 (mol)
Thay vào (*) => 0,05n + 0,1x = 0,3
=> n + 2x = 6
- Xét x = 1 => n = 4 (TM)
=> E chứa C4H8O2, CH3OH
=> Z là C3H7COOCH3
- Xét x = 2 => n = 2 (Loại do có số C khác nhau)
PTHH: C3H7COOH + CH3OH -H+,to-> C3H7COOCH3 + H2O
Xét tỉ lệ: \(\dfrac{0,05}{1}< \dfrac{0,1}{1}\) => Hiệu suất tính theo C3H7COOH
\(n_{C_3H_7COOH\left(pư\right)}=0,05.80\%=0,04\left(mol\right)\)
=> \(n_{C_3H_7COOCH_3}=0,04\left(mol\right)\)
=> m = 0,04.102 = 4,08 (g)
Đúng 2
Bình luận (0)
Oxi hóa m gam ancol (rượu) etylic một thời gian thu được hỗn hợp X. Chia X thành 3phần bằng nhau. Phần 1 tác dụng vừa đủ với dung dịch NaHCO3 thoát ra 4,48 lít khí. Phần 2 tácdụng với Na dư thoát ra 8,96 lít khí. Phần 3 tác dụng với dung dịch AgNO3/NH3 dư tạo thành 21,6gam Ag. Các phản ứng của hỗn hợp X xảy ra hoàn toàn. Xác định giá trị của m và hiệu suất phảnứng oxi hóa ancol etylic.
Đọc tiếp
Oxi hóa m gam ancol (rượu) etylic một thời gian thu được hỗn hợp X. Chia X thành 3
phần bằng nhau. Phần 1 tác dụng vừa đủ với dung dịch NaHCO3 thoát ra 4,48 lít khí. Phần 2 tác
dụng với Na dư thoát ra 8,96 lít khí. Phần 3 tác dụng với dung dịch AgNO3/NH3 dư tạo thành 21,6
gam Ag. Các phản ứng của hỗn hợp X xảy ra hoàn toàn. Xác định giá trị của m và hiệu suất phản
ứng oxi hóa ancol etylic.
X chứa CH3COOH, CH3CHO, C2H5OH, H2O
Giả sử trong mỗi phần chứa \(\left\{{}\begin{matrix}CH_3COOH:a\left(mol\right)\\CH_3CHO:b\left(mol\right)\\C_2H_5OH:c\left(mol\right)\\H_2O:d\left(mol\right)\end{matrix}\right.\)
- Phần 1:
\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: CH3COOH + NaHCO3 --> CH3COONa + CO2 + H2O
0,2<--------------------------------0,2
=> a = 0,2 (mol)
- Phần 2: \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: 2CH3COOH + 2Na --> 2CH3COONa + H2
0,2----------------------------->0,1
2C2H5OH + 2Na --> 2C2H5ONa + H2
c----------------------------->0,5c
2H2O + 2Na --> 2NaOH + H2
d--------------------->0,5d
=> 0,5c + 0,5d = 0,3
- Phần 3:
\(n_{Ag}=\dfrac{21,6}{108}=0,2\left(mol\right)\)
CH3CHO --> 2Ag
0,1<-------0,2
=> b = 0,1 (mol)
Mặt khác, ta có: nH2O(X) = nCH3CHO(tạo thành khi oxh C2H5OH bđ)
=> nH2O(X) = nCH3CHO(X) + nCH3COOH(X)
=> 3d = 3b + 3a
=> d = 0,3 (mol)
=> c = 0,3 (mol)
X chứa \(\left\{{}\begin{matrix}CH_3COOH:0,6\left(mol\right)\\CH_3CHO:0,3\left(mol\right)\\C_2H_5OH:0,9\left(mol\right)\\H_2O:0,9\left(mol\right)\end{matrix}\right.\)
Bảo toàn C: \(n_{C_2H_5OH\left(bđ\right)}=\dfrac{0,6.2+0,3.2+0,9.2}{2}=1,8\left(mol\right)\)
=> m = 1,8.46 = 82,8 (g)
\(H=\dfrac{1,8-0,9}{1,8}.100\%=50\%\)
Đúng 1
Bình luận (0)