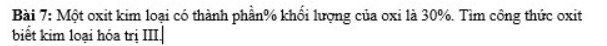Thêm 150 ml H2O ( D= 1g/ml) vào 50 gam NaCl 60%. Tính nồng độ dung dịch thu được sau phản ứng.
Hóa học
\(m_{NaCl}=50.60\%=30\left(g\right)\)
\(m_{H_2O\left(thêm\right)}=150.1=150\left(g\right)\)
=> mdd(sau khi thêm) = 150 + 50 = 200 (g)
=> \(C\%_{dd.sau.khi.thêm}=\dfrac{30}{200}.100\%=15\%\)
Đúng 1
Bình luận (0)
Cho 18,2 g hỗn hợp X gồm Al203 và CuO phản ứng với CO dư, sau phản ứng thu được 16,6 g rắn và V(l) CO2 (đktc)
a) Viết ptpư xảy ra
b) Tính V
c) Sục V(l) CO2 vào 70ml dung dịch Ba(OH)2 1M thu được bao nhiêu (g) kết tủa
a) \(CuO+CO\underrightarrow{t^o}Cu+CO_2\)
b) Gọi số mol Al2O3, CuO là a, b (mol)
=> 102a + 80b = 18,2 (1)
PTHH: \(CuO+CO\underrightarrow{t^o}Cu+CO_2\)
b------------->b---->b
=> 102a + 64b = 16,6 (2)
(1)(2) => a= 0,1 (mol); b = 0,1 (mol)
=> V = 0,1.22,4 = 2,24 (l)
c) \(n_{Ba\left(OH\right)_2}=1.0,07=0,07\left(mol\right)\)
PTHH: \(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
0,07----->0,07----->0,07
\(BaCO_3+CO_2+H_2O\rightarrow Ba\left(HCO_3\right)_2\)
0,03<---0,03
=> \(m_{BaCO_3}=\left(0,07-0,03\right).197=7,88\left(g\right)\)
Đúng 2
Bình luận (0)
a) \(CuO+CO\xrightarrow[]{t^o}Cu+CO_2\)
b) \(m_{giảm}=m_O=18,2-16,6=1,6\left(g\right)\)
\(n_{CO_2}=n_O=\dfrac{1,6}{16}=0,1\left(mol\right) \)
=> V = 0,1.22,4 = 2,24 (l)
c) \(n_{Ba\left(OH\right)_2}=1.0,07=0,07\left(mol\right)\)
Xét \(T=\dfrac{n_{Ba\left(OH\right)_2}}{n_{CO_2}}=\dfrac{0,07}{0,1}=0,7\) => Tạo cả 2 muối
\(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
0,07--------->0,07------>0,07
\(BaCO_3+CO_2+H_2O\rightarrow Ba\left(HCO_3\right)_2\)
0,03<-----0,03
=> mkt = (0,07 - 0,03).197 = 7,88 (g)
Đúng 1
Bình luận (0)
\(a.CuO+CO-^{t^o}\rightarrow Cu+CO_2\\ b.m_{giảm}=m_{O\left(trongCuO\right)}=18,2-16,6=1,6\left(g\right)\\ \Rightarrow n_{CO_2}=n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\\ \Rightarrow V_{CO_2}=0,1.22,4=2,24\left(l\right)\\ c.n_{Ba\left(OH\right)_2}=0,07\left(mol\right)\\ LTL:\dfrac{n_{CO_2}}{n_{Ba\left(OH\right)_2}}=\dfrac{0,1}{0,07}=1,42\Rightarrow Xảyra2phảnứng\\ PTHH:Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\\ Ba\left(OH\right)_2+2CO_2\rightarrow Ba\left(HCO_3\right)_2\\Đặt:\left\{{}\begin{matrix}n_{BaCO_3}=x\left(mol\right)\\n_{Ba\left(HCO_3\right)_2}=y\left(mol\right)\end{matrix}\right.\\ Tacó:\left\{{}\begin{matrix}x+y=0,07\\x+2y=0,1\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}x=0,04\\y=0,03\end{matrix}\right.\\ \Rightarrow m_{BaCO_3}=0,04.197=7,88\left(g\right)\)
Đúng 0
Bình luận (0)
Cho 8,12g Oxit sắt FexOy phản ứng hoàn toàn với CO dư. Sau phản ứng thu được m(g) rắn và 3,136 (l) CO2 (đktc) a) Viết phương trình phản ứng b) Tính m c) Tìm công thức và tên của oxit FexOy
a) \(Fe_xO_y+yCO\xrightarrow[]{t^o}xFe+yCO_2\)
b) \(n_O=n_{CO_2}=\dfrac{3,136}{22,4}=0,14\left(mol\right)\)
\(BTNT:m_{Fe}=8,12-0,14.16=5,88\left(g\right)\\ d,n_{Fe}=\dfrac{5,88}{56}=0,105\left(mol\right)\\ \Rightarrow\dfrac{x}{y}=\dfrac{n_{Fe}}{n_O}=\dfrac{0,105}{0,14}=\dfrac{3}{4}\)
=> CTHH: `Fe_3O_4` sắt từ oxit
Đúng 5
Bình luận (1)
a) FexOy+yCOto→xFe+yCO2FexOy+yCO→toxFe+yCO2
b) BTNT:mFe=8,12−0,14.16=5,88(g)d,nFe=5,8856=0,105(mol)⇒xy=nFenO=0,1050,14=34BTNT:mFe=8,12−0,14.16=5,88(g)d,nFe=5,8856=0,105(mol)⇒xy=nFenO=0,1050,14=34
=> CTHH: Fe3O4Fe3O4 sắt từ oxit
Đúng 0
Bình luận (0)
Oxit nào sau đây có % về khối lượng oxi trong phân tử là 50% A.SO2 B.SO3 C.CO2 D.NO2
\(\%O_{\left(SO_2\right)}=\dfrac{32}{64}.100\%=50\%\\ \%O_{\left(SO_3\right)}=\dfrac{48}{80}.100\%=60\%\\ \%O_{\left(CO_2\right)}=\dfrac{32}{44}.100\%=72,73\%\\ \%O_{\left(NO_2\right)}=\dfrac{32}{46}.100\%=69,57\%\)
=> A
Đúng 6
Bình luận (0)
Cho 200ml dung dịch NaOH 2M tác dụng với CuCl2 20% a. Viết phương trình b. Tính klg muối sinh ra c. Tính klg kết tủa thu được d. Tính mdd CuCl2 đã phản ứng ( cần gấp ạ)
\(n_{NaOH}=0,2.2=0,4\left(mol\right)\)
`a)`\(2NaOH+CuCl_2\rightarrow2NaCl+Cu\left(OH\right)_2\downarrow\)
0,4 0,2 0,4 0,2 ( mol )
`b)`\(m_{NaCl}=0,4.58,5=23,4\left(g\right)\)
`c)`\(m_{Cu\left(OH\right)_2}=0,2.98=19,6\left(g\right)\)
`d)`\(m_{dd_{CuCl_2}}=\dfrac{0,2.135}{20\%}=135\left(g\right)\)
Đúng 3
Bình luận (0)
a) `n_{NaOH} = 0,2.2 = 0,4 (mol)`
PTHH: `2NaOH + CuCl_2 -> Cu(OH)_2 + 2NaCl`
0,4------>0,2--------->0,2--------->0,4
b) `m_{NaCl} = 0,4.58,5 = 23,4 (g)`
c) `m_{Cu(OH)_2} = 0,2.98 = 19,6 (g)`
d) `m_{ddCuCl_2} = {0,2.135}{20%} = 135 (g)`
Đúng 3
Bình luận (0)
CTHH của oxit là: `R_2O_3`
Ta có: \(\dfrac{16.3}{16.3+2M_R}.100\%=30\%\)
=> MR = 56 => R là Fe
CTHH: `Fe_2O_3`
Đúng 2
Bình luận (0)
Ta có: \(\%O=\dfrac{16x}{32+16x}.100\%=60\%\)
=> x = 3
=> CTHH: SO3
Đúng 0
Bình luận (0)
ài 16: Trộn lẫn 150ml dung dịch H2SO4 2M vào 200g dd H2SO4 5M( D = 1,29g/ml ). Tính nồng độ mol/l của dung dịch H2SO4 nhận được.
200 gam dung dịch $H_2SO_4$ 5M có :
$V_{dd\ H_2SO_4} = 200 : 1,29 = 155(ml)$
Sau khi trộn :
$n_{H_2SO_4} = 0,15.2 + 0,155.5 = 1,075(mol)$
$V_{dd} = 0,15 + 0,155 = 0,305(lít)$
$C_{M_{H_2SO_4}} = \dfrac{1,075}{0,305} = 3,52M$
Đúng 3
Bình luận (0)
hấp thụ hoàn toàn 15.68 l CO2 (dktc) và 500ml dung dịch NaOH a(mol/l) sau phản ứng thu được dung dịch chứa 65.4g muối> Tính A
- Gọi số mol NaHCO3 và Na2CO3 là x,y
PT : CO2 + NaOH ----> NaHCO3 (1)
x x x
CO2 + 2NaOH ----> Na2CO3 + H2O (2)
y 2y y
- n_{CO_2}=\frac{15,68}{22,4}=0,7\left(n\right)nCO2=22,415,68=0,7(n)
- Ta có : x + y = 0,7 ( mol ) => y = 0,7 - x (1)
84x + 106y = 65,4 (2)
- Thay (1) vào (2) , ta có :
84x + 106(0,7 - x ) = 65,4
<=> 84x + 74,2 - 106x = 65,4
<=> -22x = 65,4 - 74,2
<=> -22x = -8,8
<=> 22x = 8,8
<=> x = 0,4 => y = 0,3
- n_{NaOH}=0,4+2\times0,3=1\left(n\right)nNaOH=0,4+2×0,3=1(n)
\Rightarrow C_{M_{NaOH}}=\frac{1}{0,5}=2\left(M\right)⇒AMNaOH=0,51=2(M)
Nếu sai ko chửi tui nha
Đúng 1
Bình luận (0)
cho 5,6 l khí CO2 ở dktc hấp thụ và 164ml dung dịch NaOH 20%(d=1.22g/ml)sau phản ứng thu được dung dịch x.Tính khối lượng các chất trong x
\(n_{CO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\); \(m_{dd.NaOH}=164.1,22=200\left(g\right)\)
\(n_{NaOH}=\dfrac{200.20\%}{40}=1\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{n_{NaOH}}{n_{CO_2}}=\dfrac{1}{0,25}=4\) => Tạo muối Na2CO3
PTHH: \(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
0,5<----0,25------>0,25
=> \(\left\{{}\begin{matrix}m_{Na_2CO_3}=0,25.106=26,5\left(g\right)\\m_{NaOH\left(dư\right)}=\left(1-0,5\right).40=20\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)