Một mẫu cellulose nitrate có %N (theo khối lượng) là 14,14%. Cho biết số nhóm -OH trong một mắt xích phân từ cellulose đã bị nitrate hóa. Giả thiết phản ứng chỉ tạo một loại cellulose nitrate duy nhất
CH2 = CH-CN
+ Trùng hợp CH2=CH–CN sẽ tạo thành poliacrilonitrin – một loại tơ sợi (tơ olon hay nitron), dai, bền với nhiệt, giữ nhiệt tốt, thường dùng để bện thành sợi “len” đan áo rét.
Đúng 1
Bình luận (0)
BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC(SUS)Tên nguyên tố kí hiệu nguyên tố số hiệu nguyên tử khối lượng nguyên tửHydrogen H 1 1Helium He 2 4Lithium Li 3 7Beryllium Be 4 9Boron B 5 11Carbon C 6 12Nitrogen N 7 14Oxygen ...
Đọc tiếp
BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
(SUS)
Tên nguyên tố kí hiệu nguyên tố số hiệu nguyên tử khối lượng nguyên tử
Hydrogen H 1 1
Helium He 2 4
Lithium Li 3 7
Beryllium Be 4 9
Boron B 5 11
Carbon C 6 12
Nitrogen N 7 14
Oxygen O 8 16
Fluorine F 9 19
Neon Ne 10 20
Sodium Na 11 23
Magnesium Mg 12 24
Aluminium Al 13 27
Silicon Si 14 28
Phosphorus P 15 31
Sulfur S 16 32
Chlorine Cl 17 35,5
Argon Ar 18 40
Potassium K 19 39
Calcium Ca 20 40
Chromium Cr 24 52
Manganese Mn 25 55
Iron Fe 26 56
Nickel Ni 28 59
Copper Cu 29 64
Zinc Zn 30 65
Bromine Br 35 80
Silver Ag 47 108
Barium Ba 56 137
Platinum Pt 78 195
Gold Au 79 197
Mercury Hg 80 201
Lead Pb 82 207
tìm lỗi sai
Thực hiện phản ứng (theo tỉ lệ số mol phản ứng) đối với hai ester E (C3H6O2) và ester F (C7H6O2) như sau:(1) E + NaOH → X + Y(2) F + 2NaOH → X + Z + H2O(3) X + HCl → T + NaClCho các phát biểu sau:(a) E và F là các ester mạch hở(b) E và F đều tham gia phản ứng tráng bạc(c) T được sử dụng để điều chế Co trong phòng thí nghiệm(d) Dẫn khí CO2 vào dung dịch Z thu được kết tủa(e) Nhiệt độ sôi của Y lớn hơn của T(g) Có thể điều chế E và F từ carboxylic acid và alcohol tương ứng
Đọc tiếp
Thực hiện phản ứng (theo tỉ lệ số mol phản ứng) đối với hai ester E (C3H6O2) và ester F (C7H6O2) như sau:
(1) E + NaOH → X + Y
(2) F + 2NaOH → X + Z + H2O
(3) X + HCl → T + NaCl
Cho các phát biểu sau:
(a) E và F là các ester mạch hở
(b) E và F đều tham gia phản ứng tráng bạc
(c) T được sử dụng để điều chế Co trong phòng thí nghiệm
(d) Dẫn khí CO2 vào dung dịch Z thu được kết tủa
(e) Nhiệt độ sôi của Y lớn hơn của T
(g) Có thể điều chế E và F từ carboxylic acid và alcohol tương ứng
Xem thêm câu trả lời
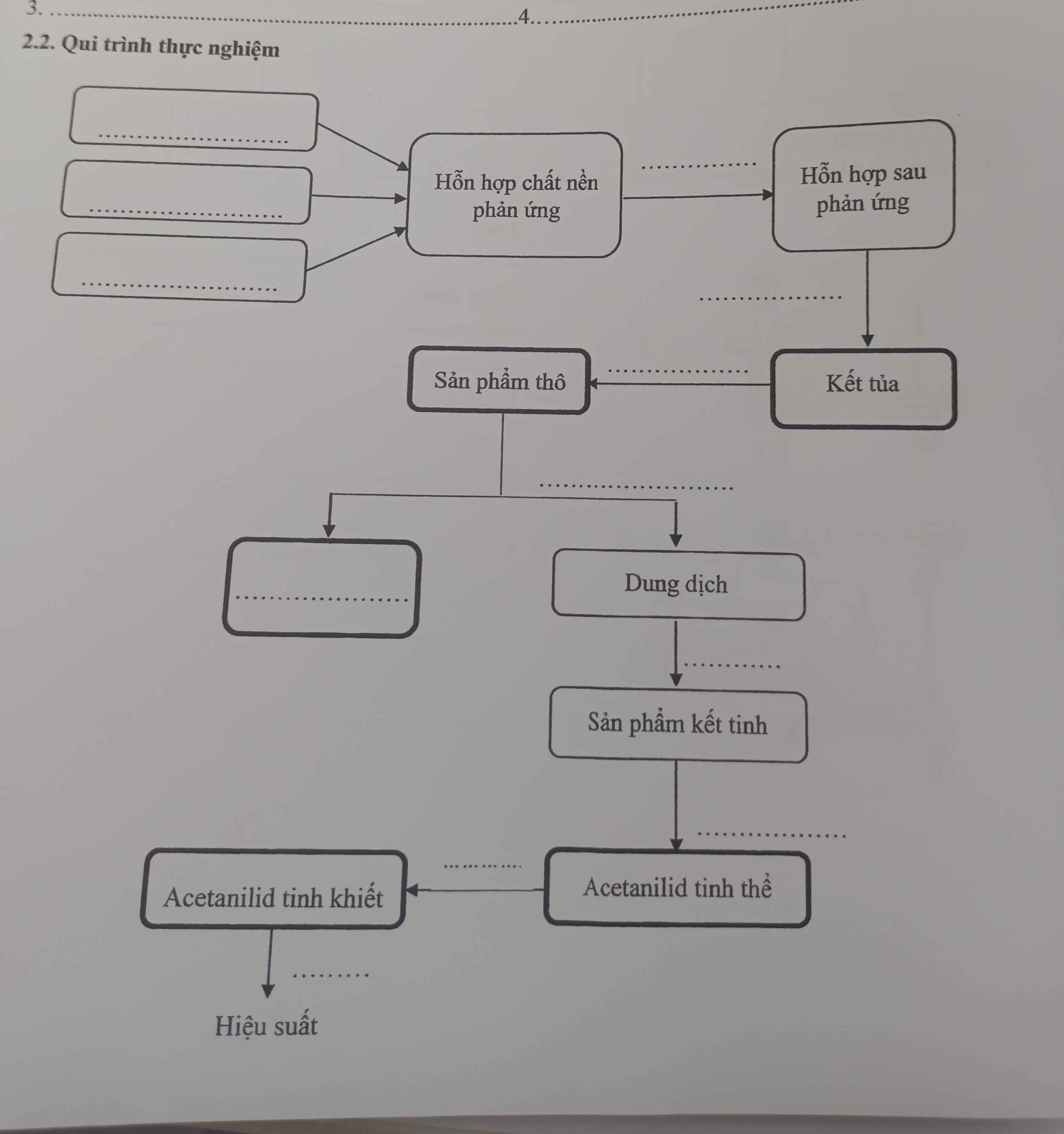 giúp mk giải bài này với ạ mk cảm ơn
giúp mk giải bài này với ạ mk cảm ơn
3 ô phía trên:
- Mục tiêu của thí nghiệm
- Phương pháp tổng hợp
- Các thiết bị, dụng cụ và biện pháp an toàn
Ô dưới sản phẩm thô :
Lọc, kết tinh, chưng cất, chiết suất
Đúng 1
Bình luận (0)
Thành phần carbohydrate chính trong kẹo mạch nha là Fructose.
Giải thích:
- Fructose là một loại đường đơn giản, có vị ngọt hơn glucose và được tìm thấy tự nhiên trong nhiều loại trái cây, mật ong và đặc biệt là trong kẹo mạch nha.
- Kẹo mạch nha được sản xuất từ quá trình lên men và đường hóa ngũ cốc, trong đó fructose là một trong những sản phẩm cuối cùng.
- Glucose cũng là một loại đường đơn giản, nhưng hàm lượng của nó trong kẹo mạch nha thường thấp hơn so với fructose.
Đúng 1
Bình luận (0)
Kẹo mạch nha không có 2 thành phần trên vì trong kẹo mạch nha chủ yếu là đường Maltose.
Đúng 1
Bình luận (0)
thế điên cực chuẩn là gì mối liên hệ giữa thế điện cực chuẩn và dãy điện hoá
Cả giấm và đường đều khử mùi tanh của cá
- Giấm có axit axetic giúp trung hòa các hợp chất amin gây mùi tanh, đồng thời làm săn chắc thịt của cá, nhưng nếu dùng giấm nhiều sẽ làm thịt cá bị chua.
- Đường sẽ phản ứng các protein trong cá, tạo ra hợp chất mới át mùi tanh của cá và tăng thêm vị ngọt tự nhiên của cá, về hiệu quả giảm mùi tanh của cá thì đường sẽ không bằng dùng giấm.
Đúng 1
Bình luận (0)
Giấm
Vì khi ta rửa cá bằng giấm, acetic acid phản ứng với trimethylamine trong cá tạo thành muối tan, dễ rửa trôi do đó có thể khử bớt mùi tanh của cá.
Đúng 0
Bình luận (0)
Trong công nghiệp, saccharose là nguyên liệu để thủy phân thành glucose và fructose dùng trong kĩ thuật tráng, tráng ruột phích. Thủy phân 3,42 gam saccharose với hiệu suất H% trong môi trường acid thu được dung dịch X. Tiến hành xư lý dung dịch X với lượng vừa đủ dung dịch NaHCO3 thu được dung dịch Y, sau đó cho toàn bộ dung dịch tham gia hoàn toàn phản ứng tráng gương thu được 3,456 gam Ag. Gia trị H% bằng bao nhiêu
Đọc tiếp
Trong công nghiệp, saccharose là nguyên liệu để thủy phân thành glucose và fructose dùng trong kĩ thuật tráng, tráng ruột phích. Thủy phân 3,42 gam saccharose với hiệu suất H% trong môi trường acid thu được dung dịch X. Tiến hành xư lý dung dịch X với lượng vừa đủ dung dịch NaHCO3 thu được dung dịch Y, sau đó cho toàn bộ dung dịch tham gia hoàn toàn phản ứng tráng gương thu được 3,456 gam Ag. Gia trị H% bằng bao nhiêu
Phản ứng thủy phân saccarozơ:
\(C_{12}H_{22}O_{11}+H_2O\rightarrow C_6H_{12}O_6+C_6H_{12}O_6\left(1\right)\)
Phản ứng tráng gương:
\(RCHO+2AgNO_3+2NH_3+H_2O\rightarrow RCOOH+2Ag\downarrow+2NH_4NO_3\left(2\right)\)
Số mol \(Ag\) thu được theo thực tế :
\(n\left(\text{Ag}\right)=\dfrac{3,456}{108}=0,032\left(mol\right)\)
Số mol saccarozơ thủy phân cần thiết để tạo ra số mol \(Ag\) này:
\(n_{\left(\text{saccarozơ}\right)}\left(lý.thuyết\right)=\dfrac{n_{Ag}}{2}=0,016\left(mol\right)\)
Khối lượng saccarozơ lý thuyết :
\(m_{\left(\text{saccarozơ}\right)}\left(lý.thuyết\right)=0,016.342=5,472\left(g\right)\)
Hiệu suất phản ứng :
\(H\%=\dfrac{m_{\left(\text{saccarozơ}\right)}\left(thực.tế\right)}{m_{\left(\text{saccarozơ}\right)}\left(lý.thuyết\right)}.100\%=\dfrac{3,42}{5,472}.100\%=62,34\%\)
Đúng 1
Bình luận (0)
khái niệm và chức năng nhóm hemiacetal
Hemiacetal là một nhóm chức năng trong hóa học hữu cơ hình thành khi một phân tử aldehyde hoặc ketone phản ứng với một phân tử alcohol. Cụ thể, hemiacetal được tạo ra thông qua phản ứng cộng nucleophilic, khi nhóm hydroxyl (-OH) của alcohol tấn công nhóm carbonyl (C=O) của aldehyde hoặc ketone.
Cấu trúc của hemiacetal:Nhóm chức năng hemiacetal có công thức tổng quát là:R1−CH(OH)−OR2R_1 - CH(OH) - OR_2R1−CH(OH)−OR2 Trong đó:R1R_1R1 là một nhóm hydrocarbon hoặc hydro (trong trường hợp của aldehyde),R2R_2R2 là một nhóm hydrocarbon (từ alcohol),−OH-OH−OH là nhóm hydroxyl,−OR2-OR_2−OR2 là nhóm alkoxy (từ alcohol).
Đúng 1
Bình luận (1)





















