Có 1lít dd hcl 2M cần thêm vào 1 lít dd trên bao nhiêu lít dd naoh 1,8M để thu đc dd có ph=13
Hóa học
Có 1 lít dung dịch HCL 2M .Cần thêm vào 1 lít dung dịch axit trên bao nhiêu lít NAOH 1,8M để thu được dung dịch có ph= 1 ( giúp mk với ạ cảm ơn nhiều ạ )
Sau phản ứng, $V_{dd} = 1 + 1 = 2(lít)$
$n_{H^+\ dư} = 2.10^{-pH} = 0,2(mol)$
$n_{H^+\ ban\ đầu} = n_{HCl} = 1.2 = 2(mol)$
$\Rightarrow n_{NaOH} = n_{OH^-} = n_{H^+\ pư} = 2 - 0,2 = 1,8(mol)$
$\Rightarrow V_{dd\ NaOH} = \dfrac{1,8}{1,8} = 1(lít)$
Đúng 1
Bình luận (1)
Câu 1: Viết các PTHH xảy ra khi: a. Cho khí H2 lần lượt tác dụng với: PbO; O2; MgO; Fe3O4 ở nhiệt độ cao? b. Cho H2O tác dụng lần lượt với: K; CaO; Cu; SO3; N2O5. Gọi tên các hợp chất thu được?
Đọc tiếp
Câu 1: Viết các PTHH xảy ra khi:
a. Cho khí H2 lần lượt tác dụng với: PbO; O2; MgO; Fe3O4 ở nhiệt độ cao?
b. Cho H2O tác dụng lần lượt với: K; CaO; Cu; SO3; N2O5. Gọi tên các hợp chất thu được?
a)
$PbO + H_2 \xrightarrow{t^o} Pb + H_2O$
$2H_2 + O_2 \xrightarrow{t^o} 2H_2O$
$Fe_3O_4 + 4H_2 \xrightarrow{t^o} 3Fe + 4H_2O$
b)
$2K + 2H_2O \to 2KOH$( Kali hidroxit) $+ H_2$
$CaO + H_2O \to Ca(OH)_2$ (Canxi hidroxit)
$SO_3 + H_2O \to H_2SO_4 $ (Axit sunfuric)
$N_2O_5 + H_2O \to 2HNO_3$ (Axit nitric)
Đúng 1
Bình luận (0)
Câu 7: Đốt cháy 5,6 g chất hữu cơ A, thu được 13,2 g CO2 và 3,6 g H2O
a. Lập CTPT của A biết tỉ khối của A so với khí nitơ bằng 2
b. Viết CTCT của A
Câu 7:
a, Đốt cháy A thu CO2 và H2O nên A chứa C và H, có thể có O.
Ta có: \(n_{CO_2}=\dfrac{13,2}{44}=0,3\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\Rightarrow n_H=0,2.2=0,4\left(mol\right)\)
⇒ mC + mH = 0,3.12 + 0,4.1 = 4 (g) < 5,6 (g)
→ A chứa C, H và O.
⇒ mO = 5,6 - 4 = 1,6 (g) \(\Rightarrow n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\)
Gọi CTPT của A là CxHyOz.
\(\Rightarrow x:y:z=0,3:0,4:0,1=3:4:1\)
→ CTĐGN của A là (C3H4O)n
Có: MA = 2.28 = 56 (g/mol)
\(\Rightarrow n=\dfrac{56}{12.3+4+16}=1\)
Vậy: CTPT của A là C3H4O.
b, CTCT: \(CH_2=CH-CHO\)
\(CH\equiv C-CH_2-OH\)
\(CH\equiv C-O-CH_3\)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn 11,2 lít khí metan cần phải dùng: a/ Bao nhiêu lít khí oxi? b/ Bao nhiêu lít không khí chứa 20% thể tích oxi? (Thể tích các khí đo ở đktc)
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
Ta có: \(n_{CH_4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
a, Theo PT: \(n_{O_2}=2n_{CH_4}=1\left(mol\right)\)
\(\Rightarrow V_{O_2}=1.22,4=22,4\left(l\right)\)
b, \(V_{kk}=\dfrac{22,4}{20\%}=112\left(l\right)\)
Đúng 2
Bình luận (0)
Câu 6: Oxi tác dụng được với dãy chất nào sau đây?A. Fe, S, CH4 B. Na2O, Fe, SC. H2O, FeO, H2 D. H2O, Na2O, S
Đọc tiếp
Câu 6: Oxi tác dụng được với dãy chất nào sau đây?
A. Fe, S, CH4 B. Na2O, Fe, S
C. H2O, FeO, H2 D. H2O, Na2O, S
Câu 6: Oxi tác dụng được với dãy chất nào sau đây?
A. Fe, S, CH4
B. Na2O, Fe, S
C. H2O, FeO, H2
D. H2O, Na2O, S
Đúng 0
Bình luận (0)
Cho 24g hỗn hợp gồm sắt (III) ôxít và đồng (II) oxit dùng hiđrô hứa sau phản ứng thu được 17,6 gam hỗn hợp hai kim loại ở nhiệt độ cao A viết các phương trình phản ứng xảy ra b.tính thể tích hiđrô cần dùng ở điều kiện tiêu chuẩn c.tính khối lượng mỗi ôxít đã phản ứng D.tính phần trăm theo khối lượng mỗi ôxít
a, PT: \(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
b, Theo PT: \(n_{H_2}=n_{H_2O}=a\left(mol\right)\)
Theo ĐLBT KL, có: m oxit + mH2 = mKL + mH2O
⇒ 24 + 2a = 17,6 + 18a ⇒ a = 0,4 (mol)
\(\Rightarrow V_{H_2}=0,4.22,4=8,96\left(l\right)\)
c, Gọi: \(\left\{{}\begin{matrix}n_{Fe_2O_3}=x\left(mol\right)\\n_{CuO}=y\left(mol\right)\end{matrix}\right.\) ⇒ 160x + 80y = 24 (1)
Theo PT: \(\left\{{}\begin{matrix}n_{Fe}=n_{Fe_2O_3}=2x\left(mol\right)\\n_{Cu}=n_{CuO}=y\left(mol\right)\end{matrix}\right.\) ⇒ 56.2x + 64y = 17,6 (2)
Từ (1) và (2) ⇒ x = y = 0,1 (mol)
\(\Rightarrow\left\{{}\begin{matrix}m_{Fe_2O_3}=0,1.160=16\left(g\right)\\m_{CuO}=0,1.80=8\left(g\right)\end{matrix}\right.\)
d, \(\left\{{}\begin{matrix}\%m_{Fe_2O_3}=\dfrac{16}{24}.100\%\approx66,67\%\\\%m_{CuO}\approx33,33\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
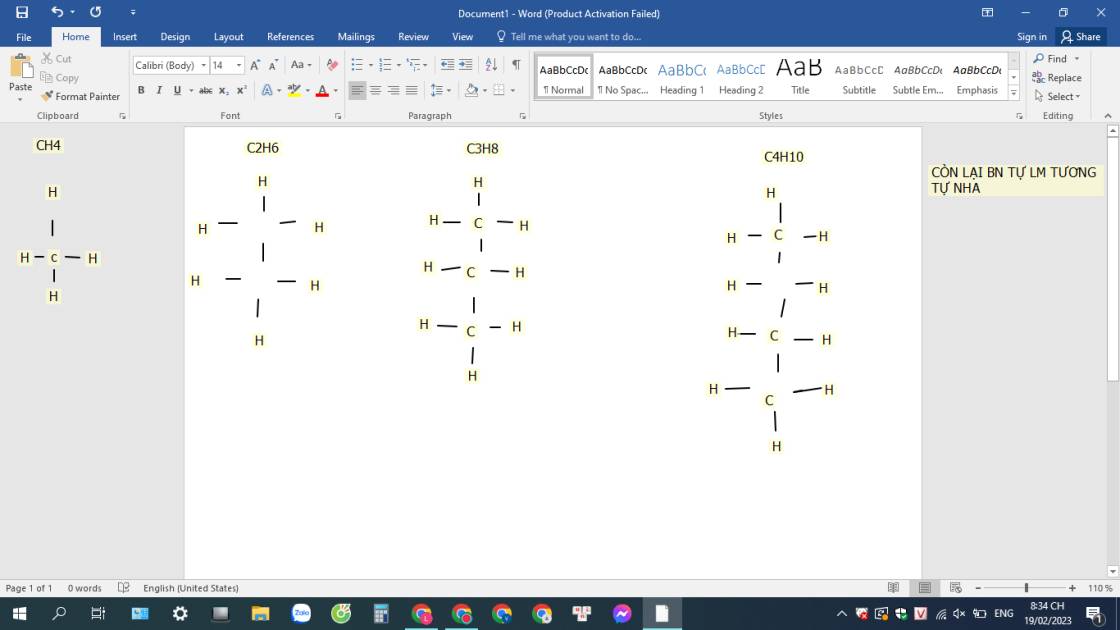
viết công thức cấu tạo phân tử của
CH4
C2H6
C3H8
C4H10
C5H12
C6H14
C7H16
C8H18
hình như thứ bạn cần là cấu tạo phân tử, chứ ko phải công thức hóa học nhỉ:?))
Đúng 1
Bình luận (1)
hòa tan hoàn toàn a g So3 vào dd H2So4 15% thì thu được 200g đ h2so4 20% tính a
Các chất SO2, Na2O,MgO,N2O5,P2O5,Al2O3 hãy phân loại hai oxit
- Oxit axit: SO2 , P2O5 và N2O5
- Oxit bazo: Na2O, MgO
- Oxit lưỡng tính: Al2O3
Đúng 0
Bình luận (0)