Đốt cháy 12,4 gam photpho trong không khí thu được điphotpho pentaoxit.
a/ Viết phương trình phản ứng.
b/ Tính khối lượng điphotpho pentaoxit tạo thành.
c/ Tính thể tích khí oxi cần dùng (ở điều kiện tiêu chuẩn)
Hóa học
a)
$4P + 5O_2 \xrightarrow{t^o} 2P_2O_5$
b) $n_P = \dfrac{12,4}{31} = 0,4(mol)$
Theo PTHH : $n_{P_2O_5} = \dfrac{1}{2}n_P = 0,2(mol)$
$m_{P_2O_5} = 0,2.142 = 28,4(gam)$
c) $n_{O_2} = \dfrac{5}{4}n_P = 0,5(mol)$
$V_{O_2} = 0,5.22,4 = 11,2(lít)$
Đúng 1
Bình luận (0)
1) Na+ O2 --->
2) Cu + O2 --->
3) Ba+ O2 --->
4) Al + O2 --->
5) Zn + O2 --->
6) K + O2 --->
\(1,4Na+O_2\underrightarrow{t^o}2Na_2O\)
\(2,2Cu+O_2\underrightarrow{t^o}2CuO\)
\(3,2Ba+O_2\underrightarrow{t^o}2BaO\)
\(4,4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(5,2Zn+O_2\underrightarrow{t^o}2ZnO\)
\(6,4K+O_2\underrightarrow{t^o}2K_2O\)
Đúng 3
Bình luận (0)
$1) 4Na + O_2 \xrightarrow{t^o} 2Na_2O$
$2) 2Cu + O_2 \xrightarrow{t^o} 2CuO$
$3) 2Ba + O_2 \xrightarrow{t^o} 2BaO$
$4) 4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
$5) 2Zn + O_2 \xrightarrow{t^o} 2ZnO$
$6) 4K + O_2 \xrightarrow{t^o} 2K_2O$
Đúng 0
Bình luận (0)
Viết các phương trình phản ứng khi cho khí oxi tác dụng với lưu huỳnh, sắt,
cacbon, photpho, nhôm, kẽm, kali, CH4, CaH10, C2H6O.
$S + O_2 \xrightarrow{t^o} SO_2$
$3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4$
$C + O_2 \xrightarrow{t^o} CO_2$
$4P + 5O_2 \xrightarrow{t^o} 2P_2O_5$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
$2Zn + O_2 \xrightarrow{t^o} 2ZnO$
$4K + O_2 \xrightarrow{t^o} 2K_2O$
$CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O$
$C_2H_6O + 3O_2 \xrightarrow{t^o} 2CO_2 + 3H_2O$
Đúng 1
Bình luận (0)
Đốt cháy 12,4 gam photpho trong không khí thu được điphotpho pentaoxit.
a/ Viết phương trình phản ứng.
b/ Tính khối lượng điphotpho pentaoxit tạo thành.
c/ Tính thể tích khí oxi cần dùng (ở điều kiện tiêu chuẩn)
a)
$4P + 5O_2 \xrightarrow{t^o} 2P_2O_5$
b) $n_P = \dfrac{12,4}{31} = 0,4(mol)$
Theo PTHH : $n_{P_2O_5} = \dfrac{1}{2}n_P = 0,2(mol)$
$m_{P_2O_5} = 0,2.142 = 28,4(gam)$
c) $n_{O_2} = \dfrac{5}{4}n_P = 0,5(mol)$
$V_{O_2} = 0,5.22,4 = 11,2(lít)$
Đúng 1
Bình luận (0)
Có hai lọ đựng hai chất khí không màu: khí oxi Oz, khí cacbonic CO,. Bằng phương
pháp hóa học hãy nhận biết hai chất khí trên. Viết phương trình phản ứng minh họa.
Trích mẫu thử
Sục các mẫu thử vào dung dịch nước vôi trong :
- mẫu thử nào tạo vẩn đục trắng là $CO_2$
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
- mẫu thử nào không hiện tượng là $O_2$
Đúng 1
Bình luận (0)
Lập phương trình hóa học biểu diễn phản ứng hóa hợp của lưu huỳnh với các kim
loại magie Mg, kẽm Zn, sắt Fe, nhôm Al, biết rằng công thức hóa học các hợp chất được
tạo thành kà MgS, ZnS, FeS, AlzS3.
Phương trình hóa học:
\(Mg+S\rightarrow MgS\)
\(Fe+S\rightarrow FeS\)
\(Zn+S\rightarrow ZnS\)
\(2Al+3S\rightarrow Al_2S_3\)
Đúng 0
Bình luận (1)
Hòa tan hoàn toàn 52 gam hỗn hợp X gồm Al, Fe, Zn trong dung dịch HCl vừa đủ, sau phản ứng kết thúc thu được dung dịch Y chứa 119,45 gam muối và V lít H2 (đktc). Giá trị của V là: A. 17,92 lít. B. 22,4 lit. C. 21,28 lít. D. 26,28 lít.
\(n_{HCl}=n_{Cl}=\dfrac{119,45-52}{35,5}=1,9\left(mol\right)\\ \Rightarrow n_{H_2}=\dfrac{1}{2}n_{HCl}=0,95\left(mol\right)\\ \Rightarrow V=V_{H_2}=0,95.22,4=21,28\left(l\right)\)
Chọn C
Đúng 2
Bình luận (0)
Giups em a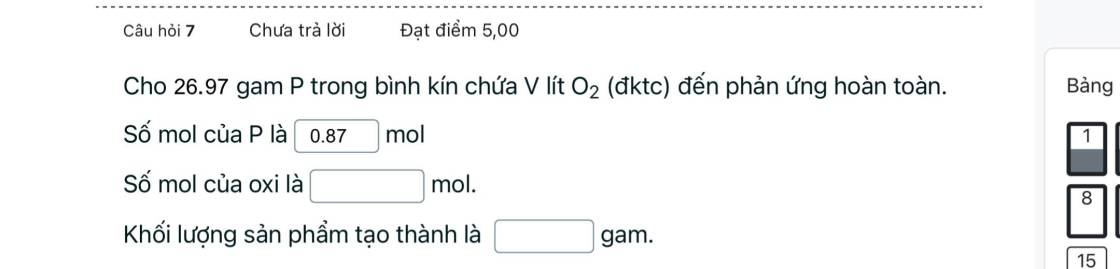
Trong 1 bình trộn khí SO2 và SO3 khi phân tích thấy có 0.4gam S và 2.8 gam O. Hãy xác định tỉ lệ số mô của SO2 và SO3
\(n_S=\dfrac{0,4}{32}=0,0125\left(mol\right);n_O=\dfrac{2,8}{16}=0,175\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{SO_2}=a\left(mol\right)\\n_{SO_3}=b\left(mol\right)\end{matrix}\right.\left(a,b>0\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_S=n_{SO_2}+n_{SO_3}=a+b=0,0125\\n_O=2n_{SO_2}+3n_{SO_3}=2a+3b=0,175\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=-0,1375\left(mol\right)\\b=0,15\left(mol\right)\end{matrix}\right.\)
Đề sai à bạn?
Đúng 0
Bình luận (1)












