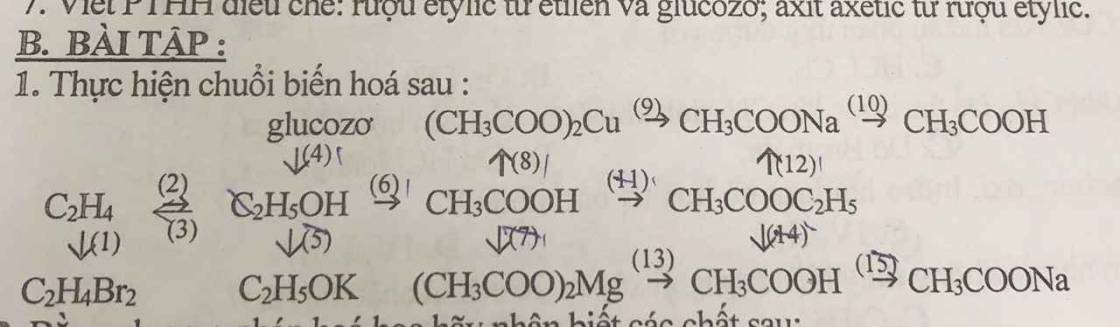Cô mới giao mà ko b lm ::) HELPP

Hóa học
Cho 2,4g kim loại Mg tác dụng hoàn toàn với dung dịch axit axetic 0,5M. a/ Viết PTHH xảy ra. b/ Tính thể tích dung dịch axit đã phản ứng. c/ Nếu cho lượng axit 0,5M ở trên thực hiện phản ứng este hoá. Tính khối lượng rượu etylic cần dùng để phản ứng với dung dịch axit nói trên. Biết hiệu suất phản ứng đạt 80%
Cho kim loại kẽm tác dụng vừa đủ với dung dịch HCI 1,5M. Tính khối lượng muối kẽm clorua thu được? Biết rằng nếu thay dung dịch HCl trong phản ứng bằng dung dịch H2SO4 loãng có nồng độ mol gấp đôi thì dùng vừa đủ 100 ml. ( mọi người giúp mình với ạ)
\(n_{H_2SO_4}=0,1.3=0,3\left(mol\right)\)
PT: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
Theo PT: \(n_{Zn}=n_{H_2SO_4}=0,3\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Theo PT: \(n_{ZnCl_2}=n_{Zn}=0,3\left(mol\right)\Rightarrow m_{ZnCl_2}=0,3.136=40,8\left(g\right)\)
Đúng 1
Bình luận (0)
Đốt cháy lưu huỳnh trong bình chứa 6,72 lit O2 (đktc) thu đươc một thể tích khí SO2 : A. 2,24 lít B. 4,48 lít C. 1,12 lít D. 3,36 lít
Đọc tiếp
Đốt cháy lưu huỳnh trong bình chứa 6,72 lit O2 (đktc) thu đươc một thể tích khí SO2 :
A. 2,24 lít B. 4,48 lít C. 1,12 lít D. 3,36 lít
\(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PT: \(S+O_2\underrightarrow{t^o}SO_2\)
Theo PT: \(n_{SO_2}=n_{O_2}=0,3\left(mol\right)\Rightarrow V_{SO_2}=0,3.22,4=6,72\left(l\right)\)
Đúng 1
Bình luận (0)
Cho 0,5 lít dung dịch axit axetic tác dụng hoàn toàn với kim loại sắt. Sau phản ứng đem cô cạn dung dịch thu được 34,8g muối. a/Tính nồng độ mol/lít của dung dịch axit đã dùng? b/Nếu cho 0,5 lít dung dịch axit axetic trên đun nóng với rượu etylic, có axit sunfuric đặc làm chất xúc tác, sau phản ứng thu được bao nhiêu gam etylaxetat. Biết hiệu suất của phản ứng đạt 75%.
Cho 5,4 gam bột nhôm tác dụng vừa đủ với 400 ml dung dịch HCL A:tính nồng độ mol/lít dung dịch đã dùng B: khí hiđrô thu được ở trên cho qua bình đựng CuO dư nung nóng thu được m gam Đồng tính m
a, \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Theo PT: \(n_{HCl}=3n_{Al}=0,6\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,6}{0,4}=1,5\left(M\right)\)
b, \(n_{H_2}=\dfrac{3}{2}n_{Al}=0,3\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Theo PT: \(n_{Cu}=n_{H_2}=0,3\left(mol\right)\Rightarrow m_{Cu}=0,3.64=19,2\left(g\right)\)
Đúng 2
Bình luận (0)
Hoà tan kẽm Zn vào 400ml dung dịch axit Clohiđric HCL 1M a tính lượng muối thu được b tính thể tích khí hiđro thu được
\(a,n_{HCl}=1.0,4=0,4\left(mol\right)\\ PTHH:Zn+2HCl\xrightarrow[]{}ZnCl_2+H_2\\ n_{ZnCl_2}=\dfrac{0,4}{2}=0,2\left(mol\right)\\ m_{ZnCl_2}=0,2.136=27,2\left(g\right)\\ b,n_{H_2}=\dfrac{0,4}{2}=0,2\left(mol\right) \\ V_{H_2}=0,2.22.4=4,48\left(l\right)\)
Đúng 0
Bình luận (0)
Hoàn thành các phản ứng hóa học sau và cho biết phản ứng nào là phản ứng hóa hợp , phản ứng cháy , phản ứng phân hủy , phản ứng thế.a/.........+.........------ ZnOb/.........+........------- H³PO⁴c/......+........------- CO² + H²Od/......+........------ K²Se/H²O -----......+........f/KClO³ ------ ......+.......g/.......+.......---- CuCl²h/KMnO⁴ ------ ........+.......+.....i/Zn +HCl ------- ......+......j/Al + H²SO⁴ ------ .......+........k/H² +......------ O² +.....l/CaO + H²O ------ .............
Đọc tiếp
Hoàn thành các phản ứng hóa học sau và cho biết phản ứng nào là phản ứng hóa hợp , phản ứng cháy , phản ứng phân hủy , phản ứng thế.
a/.........+.........------> ZnO
b/.........+........-------> H³PO⁴
c/......+........-------> CO² + H²O
d/......+........------> K²S
e/H²O ----->......+........
f/KClO³ ------> ......+.......
g/.......+.......----> CuCl²
h/KMnO⁴ ------> ........+.......+.....
i/Zn +HCl -------> ......+......
j/Al + H²SO⁴ ------> .......+........
k/H² +......------> O² +.....
l/CaO + H²O ------> ...........
\(a/2Zn+O_2\xrightarrow[t^0]{}2ZnO\\ b/P_2O_5+3H_2O\xrightarrow[]{}2H_3PO_4\left(pư.hoá.hợp\right)\\ c/C_2H_4+3O_2\xrightarrow[t^0]{}2CO_2+2H_2O\left(pư.thế\right)\\ d/2K+S\xrightarrow[]{}K_2S\left(pư.hoá.hợp\right)\\ e/2H_2O\xrightarrow[đp]{}2H_2+O_2\left(pư.phân.huỷ\right)\\ f/2KClO_3\xrightarrow[t^0]{}2KCl+3O_2\left(pư.phân.huỷ\right)\\ g/Cu+Cl_2\xrightarrow[]{}CuCl_2\left(pư.hoá.hợp\right)\\ h/2KMnO_4\xrightarrow[t^0]{}K_2MnO_4+MnO_2+O_2\left(pư.phân.huỷ\right)\\ i/Zn+2HCl\xrightarrow[]{}ZnCl_2+H_2\left(pư.thế\right)\\ j/2Al+3H_2SO_4\xrightarrow[]{}Al_2\left(SO_4\right)_3+3H_2\left(pư.thế\right)\\ k/Sai.đề\\ l/CaO+H_2O\xrightarrow[]{}Ca\left(OH\right)_2\left(pư.hoá.hợp\right)\)
Đúng 0
Bình luận (0)
Hoà tan mg kẽm vào dd chứa 200ml HCL 1mol. a)viết Phương trình phản ứng b)Tính khối lượng m c)Tính thể tích hiđro.(cho O=16 ,H=1 ,Cl=35,5; Zn=65)
a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, \(n_{HCl}=0,2.1=0,2\left(mol\right)\)
Theo PT: \(n_{Zn}=\dfrac{1}{2}n_{HCl}=0,1\left(mol\right)\Rightarrow m_{Zn}=0,1.65=6,5\left(g\right)\)
c, \(n_{H_2}=\dfrac{1}{2}n_{HCl}=0,1\left(mol\right)\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Đúng 1
Bình luận (0)