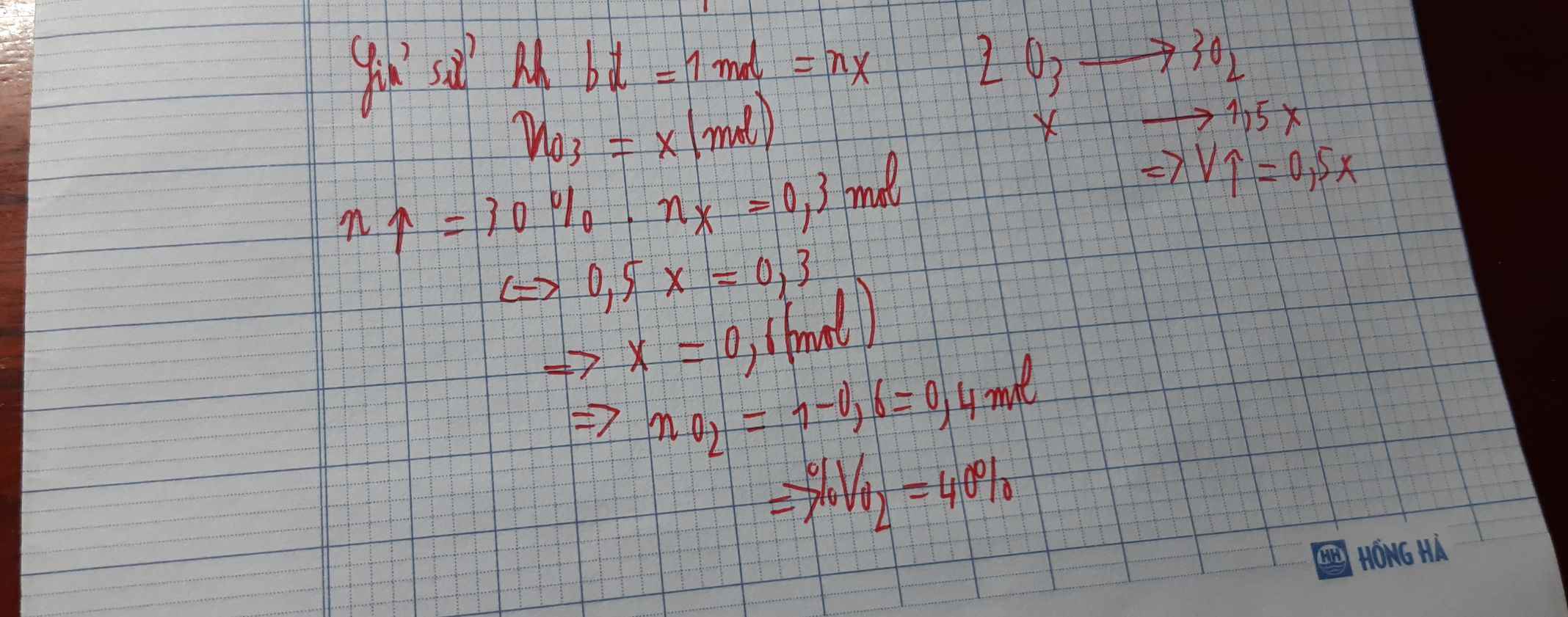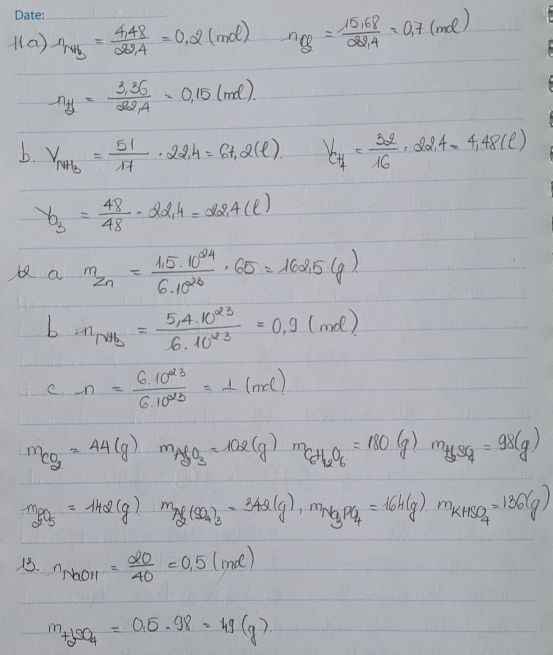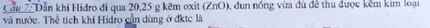
Hóa học
nZnO = 20,25/81 = 0,25 (mol)
PTHH: ZnO + H2 -> (t°) Zn + H2O
Mol: 0,25 ---> 0,25
VH2 = 0,25 . 22,4 = 5,6 (l)
Đúng 3
Bình luận (0)
C13: bạn tự học SGK
C14:
3Fe + 2O2 -> (t°) Fe3O4
4P + 5O2 -> (t°) 2P2O5
MgCO3 -> (t°) MgO + CO2
C2H4 + 3O2 -> (t°) 2CO2 + 2H2O
C15:
nCuO = 48/80 = 0,6 (mol)
PTHH: 2Cu + O2 -> 2CuO
Mol: 0,6 <--- 0,3 <--- 0,6
VO2 = 0,3 . 22,4 = 6,72 (l)
PTHH: 2KClO3 -> (t°, MnO2) 2KCl + 3O2
Mol: 0,2 <--- 0,2 <--- 0,3
mKClO3 = 0,2 . 122,5 = 24,5 (g)
Đúng 2
Bình luận (0)
Bài toán so sánh Hết-dư
Câu 12:
\(nZn=\dfrac{2,6}{65}=0,04\left(mol\right)\)
\(nCuCl_2=0,75.0,1=0,075\left(mol\right)\)
có pthh:
\(Zn+CuCl_2\rightarrow ZnCl_2+Cu\)
Trong dung dịch thu được ta có:
\(nZnCl_2=0,04\left(mol\right)\)
\(nCuCl_2=0,075-0,04=0,035\left(mol\right)\)
Đúng 3
Bình luận (0)
B12:
nZn = 2,6/65 = 0,04 (mol)
nCuCl2 = 0,1 . 0,75 = 0,075 (mol)
PTHH: Zn + CuCl2 -> ZnCl2 + Cu
LTL: 0,04 < 0,075 => CuCl2 dư
nZnCl2 = nCu = nCuCl2 (p/ư) = nZn = 0,04 (mol)
nCuCl2 (dư) = 0,075 - 0,04 = 0,035 (mol)
B13:
nNaCl = 5,85/58,5 = 0,1 (mol)
nAgNO3 = 34/170 = 0,2 (mol)
PTHH: NaCl + AgNO3 -> NaNO3 + AgCl
LTL: 0,1 < 0,2 => AgNO3 dư
nNaNO3 = nAgCl = 0,1 (mol)
mNaNO3 = 0,1 . 85 = 8,5 (g)
mAgCl = 0,1 . 143,5 = 14,35 (g)
Đúng 3
Bình luận (2)
câu 13:
\(nNaCl=0,1\left(mol\right)\)
\(nAgNO_3=0,2\left(mol\right)\)
có pthh:
\(NaCl+AgNO_3\rightarrow AgCl\downarrow+NaNO_3\)
0,1<-----0,2---------->0,1
\(mAgCl=0,1.\left(108+35,5\right)=14,35\left(g\right)\)
Đúng 0
Bình luận (2)
Khi đốt 1 lít chất X cần 5 lít oxi thu được 3 lít CO2 , 4 lít hơi nước (thể tích các khí đo ở cùng điều kiện nhiệt độ, áp suất). Xác định CTPT của X.
VC = 3 lit; V H = 8
→ V O = 0 vì VO ban đầu = 5.2 = 10 lit = VO sau phản ứng = 2*VC+ V H
Công thức tổng quát : CxHy ta có x:y = 3:8 → công thức của X là C3H8.
Đúng 5
Bình luận (0)
VC = VCO2 = 3 (l)
VH = 2 . VH2O = 2 . 4 = 8 (l)
VO (trong oxi) = 5 . 2 = 10 (l)
VO (sau p/ư) = 4 . 2 + 3 = 10 (l)
So sánh: 10 = 10 => trong X chỉ có H và C
CTPT: CxHy
=> x : y = 3 : 8
Vậy X là C3H8
Đúng 2
Bình luận (0)
VC = 3 lit; V H = 8
→ V O = 0 vì VO ban đầu = 5.2 = 10 lit = VO sau phản ứng = 2*VC+ V H
Công thức tổng quát : CxHy ta có x:y = 3:8 → công thức của X là C3H8.
Đúng 0
Bình luận (0)
làm hết 3 câu hộ mình nha
mình cảm ơn nhiều lắm

Tham khảo:
a) nNH3NH3=4,48/22,4=0,2 (mol)
nCl2Cl2=15,68/22,4=0,7 (mol)
nH2H2=3,36/22,4=0,15 (mol)
b) nNH3NH3=51/17=3 (mol)
=>VNH3NH3=3.22,4=67,2 (l)
nCH4CH4=32/16=2 (mol)
=>VCH4CH4=2.22,4=44,8 (l)
nO3O3=48/48=1 (mol)
=>VO3O3=1.22,4=22,4 (l)
Đúng 2
Bình luận (0)
C1 viết phương trình hóa học biểu diễn sự chảy của sắt,photpho,lưu hình ,nhôm trong khí oxi
C2 dẫn 2,24 lít khí hidro(đktc) vào một ống chứa 12g CuO đã nung nóng đến một nhiệt độ thích hợp.Khối lượng nước tạo thành là:
C3 Cho chất Fe2O3
a) hợp chất Fe2O3 gồm mấy nguyên tố ? đó là nguyên tố nào?
b) Tính phần trăm về khối lượng của oxi
C1:
3Fe + 2O2 -> (t°) Fe3O4
4P + 5O2 -> (t°) 2P2O5
S + O2 -> (t°) SO2
C2:
nH2 = 2,24/22,4 = 0,1 (mol)
nCuO = 12/80 = = 0,15 (mol)
PTHH: CuO + H2 -> (t°) Cu + H2O
LTL 0,15 > 0,1 => CuO dư
nH2O = 0,1 (mol)
mH2O = 0,1 . 18 = 1,8 (g)
C3:
Fe2O3 gồm 2 nguyên tố: Fe và O
%Fe = 112/160 = 70%
%O = 100% - 70% = 30%
Đúng 3
Bình luận (2)
Câu 1: Photpho: 4P + 5O2 (to)-> 2P2O5
Lưu huỳnh: S + O2 (to)-> SO2
Nhôm: 4Al + 3O2 (to)-> Al2O3
Câu 2:
PTHH: \(CuO+H_2=>Cu+H_2O\)
\(nH_2=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(nCuO=\dfrac{12}{80}=0,15\left(mol\right)\)
\(=>CuOdư\)
\(nH_2O=nH_2=0,1\left(mol\right)\)
\(mH_2=0,1\text{×}18=1,8\left(gam\right)\)
Đúng 3
Bình luận (0)
Cho 9,2 g Kl R ( hóa trị 1) tác dụng H2O dư 4,48 (l) H2 đktc.Xác định R
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: 2R + 2H2O --> 2ROH + H2
0,4<------------------0,2
=> \(M_R=\dfrac{9,2}{0,4}=23\left(g/mol\right)\)
=> R là Na
Đúng 3
Bình luận (0)
Bài 3: Tính khối lượng KMnO4 cần điều chế được lượng oxi đủ phản ứng cho 36 g kim loại sắt. (sp Fe3O4)Bài 4: Khi đốt cháy nhôm trong khí oxi thu được nhôm oxit Al2O3. a) Tính khối lượng Nhôm và thể tích khí oxi (đktc) cần dùng để điều chế 51 gam nhôm oxit. b) Tính khối lượng kali pemanganat cần dùng để điều chế lượng khí oxi nói trên. c) Tính khối lượng kali clorat cần dùng để điều chế lượng khí oxi nói trên.Bài 5: Khi đốt cháy hoàn toàn 14,4 gam Mg trong bình chứa 4,48 lít O2 (đk...
Đọc tiếp
Bài 3: Tính khối lượng KMnO4 cần điều chế được lượng oxi đủ phản ứng cho 36 g kim loại sắt. (sp Fe3O4)
Bài 4: Khi đốt cháy nhôm trong khí oxi thu được nhôm oxit Al2O3.
a) Tính khối lượng Nhôm và thể tích khí oxi (đktc) cần dùng để điều chế 51 gam nhôm oxit.
b) Tính khối lượng kali pemanganat cần dùng để điều chế lượng khí oxi nói trên.
c) Tính khối lượng kali clorat cần dùng để điều chế lượng khí oxi nói trên.
Bài 5: Khi đốt cháy hoàn toàn 14,4 gam Mg trong bình chứa 4,48 lít O2 (đktc) thu được m gam hỗn hợp chất rắn. Giá trị của là ?
Bài 6: Đốt cháy hoàn toàn 12,8 gam Cu cần vừa đủ V lít không khí (đktc) thu được m gam CuO. Tính giá trị của m và V. Biết trong không khí oxi chiếm 20% thể tích.
Bài 7: Nung 79 gam KMnO4 thu được V lít khí O2 đo ở đktc. Biết hiệu suất phản ứng nhiệt phân là 80%, hãy tính giá trị của V ?
Bài 8: Nung 24,5 gam KClO3 thu được V lít khí O2 đo ở đktc. Biết hiệu suất phản ứng nhiệt phân là 50%, hãy tính giá trị của V ?
Bài 9: Nung m gam KClO3 thu được 6,72 lít khí O2 đo ở đktc. Biết hiệu suất phản ứng nhiệt phân là 70%, hãy tính giá trị của m ?
Mọi người giúp mình được câu nào thì cứ giúp nhé. Mình cảm ơn nhiều ạ
Bài 8: PTHH: 2KClO₃ (t°)-> 2KCl + 3O₂
mKClO3=24,5x70%=17,15 (g)
nKClO3=\(\dfrac{mKClO_3}{MKClO_3}=\dfrac{17,15}{122,5}=0,14\left(mol\right)\)
Theo PTHH ta có \(nO_2=\dfrac{0,14\text{×}3}{2}=0,21\left(mol\right)\)
\(=>VO_2=nO_2\text{×}22,4=0,21\text{×}22,4=4,704\left(l\right)\)
Đúng 2
Bình luận (0)
Nêu hiện tượng và viết phương trình khi cho HCl dư vào ống nghiệm chứa thanh sắt
- Thanh sắt tan vào dung dịch, có khí không màu thoát ra:
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
Đúng 4
Bình luận (1)
- Một phần thanh sắt tan vào dd, có khí không màu thoát ra:
Fe+2HCl→FeCl2+H2↑
Đúng 2
Bình luận (1)
-Hiện tượng : thanh sắt tan dần, dd tạo thành có màu lục nhạt, có hiện tượng sủi bọt khí.
-Phương trình:
2HCl + Fe → FeCl2 + H2 ↑
Đúng 0
Bình luận (0)