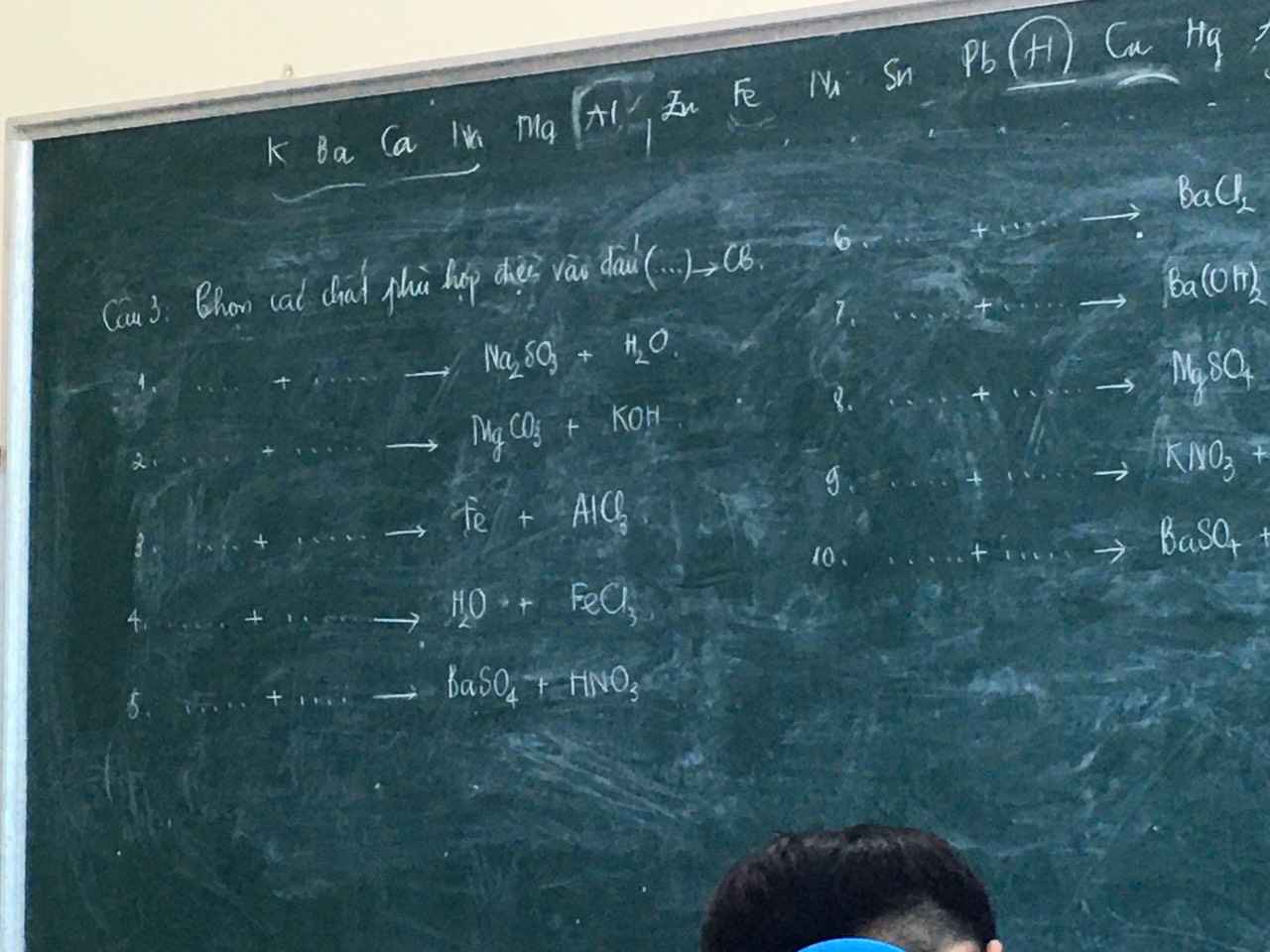
Hóa học
\(Na_2O+H_2SO_3\rightarrow Na_2SO_3+H_2O\\ Mg\left(OH\right)_2+K_2CO_3\rightarrow MgCO_3+2KOH\\ FeCl_3+Al\underrightarrow{t^o}Fe+AlCl_3\\ Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\\ Ba\left(NO_3\right)_2+H_2SO_4\rightarrow BaSO_4+2HNO_3\)
Đúng 1
Bình luận (0)
Lượng hoá chất thêm vào 100ml dung dịch NaOH 0.75N để được dung dịch NaOH coa nồng độ chianh xác 1,00N
Cho 8,64 gam một axit đơn chức phản ứng với 144 ml dd KOH 1M. Cô cạn dd sau phản ứng được 14,544 gam chất rắn. Công thức của axit là:
nKOH = 0,144 mol
Áp dụng định luật bảo toàn khối lượng ta có:
8,64 + 0,144.56 = 14,544 + mnước
mnước = 2,16 g ⇒ nnước = 0,12 mol = naxit
⇒ Maxit = 8,64 : 0,12 = 72 (g/mol)
Vậy axit là C2H3COOH (axit acrylic).
Đúng 0
Bình luận (0)
Giúp mình với mình đang cần gấp ạ. Cảm ơn rấc nhìu !!!
Đọc tiếp







Giúp mình với mình đang cần gấp ạ. Cảm ơn rấc nhìu !!!
Câu 4: C
Câu 1: D
Câu 2: 2,3,1,3
Câu 3: C
Câu 5: B
Đúng 0
Bình luận (0)
Câu 3: Dung dịch X chứa hỗn hợp HCl và H2SO4 theo tỉ lệ mol 1:2. Trung hoà 100 gam dung dịch X cần 100 gam dd NaOH 10%.
a/ Tính C% các chất trong dung dịch X và trong dung dịch thu được sau phản ứng.
b/ Nếu thay dung dịch NaOH bằng dung dịch Ba(OH)2 8,55% để thực hiện phản ứng trung hòa thì nồng độ chất tan trong dung dịch sau trung hoà bằng bao nhiêu?
a)
Gọi \(\left\{{}\begin{matrix}n_{HCl}=a\left(mol\right)\\n_{H_2SO_4}=2a\left(mol\right)\end{matrix}\right.\)
\(m_{NaOH}=100.10\%=10\left(g\right)\\ n_{NaOH}=\dfrac{10}{40}=0,25\left(mol\right)\)
PTHH:
\(NaOH+HCl\rightarrow NaCl+H_2O\)
a<--------a
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
a<----------2a
=> a + a = 0,25
=> a = 0,125
=> \(\left\{{}\begin{matrix}C\%_{HCl}=\dfrac{0,125.36,5}{100}.100\%=4,5625\%\\C\%_{H_2SO_4}=\dfrac{0,125.2.98}{100}.100\%=24,5\%\end{matrix}\right.\)
b)
PTHH:
\(Ba\left(OH\right)_2+H_2SO_4\rightarrow BaSO_4\downarrow+2H_2O\)
0,25<-------0,25---------->0,25
\(Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\)
0,0625<---0,125------->0,0625
\(m_{dd.Ba\left(OH\right)_2}=\dfrac{\left(0,25+0,0625\right).171}{8,55\%}=625\left(g\right)\\ m_{dd.sau.pư}=625+100-0,25.233=666,75\left(g\right)\\ \Rightarrow C\%_{BaCl_2}=\dfrac{0,0625.208}{666,75}.100\%=1,95\%\)
Đúng 2
Bình luận (0)
Lấy 1 lượng vừa đủ nhôm oxit tác dụng với 300ml H2SO4 0,5M
a)Khối lượng nhôm oxit đã phản ứng
b)Khối lượng muối đã tạo thành
c) Cũng lượng oxit nhôm trên cần bao nhiêu ml 3M
\(n_{H_2SO_4}=0,5.0,3=0,15\left(mol\right)\\
pthh:Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
0,05 0,15 0,05
\(m_{Al_2O_3}=102.0,05=5,1\left(g\right)\\
m_{Al_2\left(SO_4\right)_3}=342.0,05=17,1\left(g\right)\\
n_{H_2SO_4}=n_{Al_2O_3}=0,15\left(mol\right)\\
C_{M\left(H_2SO_4\right)}=\dfrac{0,15}{3}=0,05\left(l\right)hay50\left(ml\right)\)
Đúng 1
Bình luận (1)
\(n_{H_2SO_4}=0,5.0,3=0,15\left(mol\right)\\ pthh:Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
0,05 0,15 0,05
\(m_{Al_2O_3}=102.0,05=5,1\left(g\right)\\
m_{Al_2\left(SO_4\right)_3}=342.0,05=17,1\left(g\right)\)
\(n_{HCl}=3n_{Al}=0,15\left(mol\right)\\
C_{M\left(HCl\right)}=\dfrac{0,15}{3}=0,05\left(l\right)hay50ml\)
Đúng 0
Bình luận (4)
Cho em hỏi bài này làm như nào ạ? Em cảm ơn nhiều!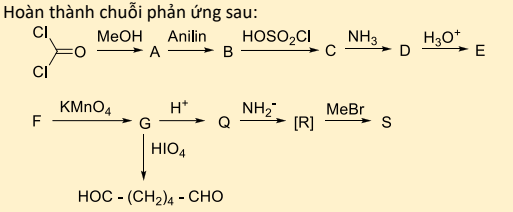
Bài 3: Cho V lít HCl 2M tác dụng V lít dung dịch AgNO3 1M sau phản ứng thu được 14,35g kết tủa. a, xác định V HCl, V AgNO3 b, xác định CM dung dịch thu đc sau p/ung
a)
\(n_{AgCl}=\dfrac{14,35}{143,5}=0,1\left(mol\right)\)
PTHH: \(AgNO_3+HCl\rightarrow AgCl\downarrow+HNO_3\)
0,1<------0,1<------0,1------->0,1
\(\left\{{}\begin{matrix}V_{dd.HCl}=\dfrac{0,1}{2}=0,05\left(l\right)\\V_{dd.AgNO_3}=\dfrac{0,1}{1}=0,1\left(l\right)\end{matrix}\right.\)
b) \(C_{M\left(HNO_3\right)}=\dfrac{0,1}{0,1+0,05}=\dfrac{2}{3}M\)
Đúng 1
Bình luận (0)
PTHH:
\(AgNO_3+HCl->AgCl+HNO_3\)
--> kết tủa là AgCl
\(n_{AgCl}=\dfrac{m}{M}=\dfrac{14,35}{108+35,5}=0,1\left(mol\right)\)
Dựa theo PTHH:
--> \(n_{HCl}=n_{AgNO_3}=n_{HNO_3}=n_{AgCl}=0,1\left(mol\right)\)
\(V_{HCl}=\dfrac{n}{C_M}=\dfrac{0,1}{2}=0,05\left(lít\right)\)
\(V_{AgNO_3}=\dfrac{n}{C_M}=\dfrac{0,1}{1}=0,1\left(lít\right)\)
b) Dung dịch thu được sau phản ứng là \(HNO_3\)
\(V_{ddsau}=V_{HCl}+V_{AgNO_3}=0,05+0,1=0,15\left(lít\right)\)
\(C_{M\left(HNO_3\right)}=\dfrac{n}{V}=\dfrac{0,1}{0,15}=\dfrac{2}{3}M\)
Đúng 0
Bình luận (0)
\(m_{hh}=\dfrac{110g}{mol}\)
\(=>M_{O2}=\dfrac{110.43,46\%}{100}=48g\)
=>\(M_P=62\)g
\(m_{O2}=\dfrac{48}{16}=3mol\)
\(m_P=\dfrac{62}{31}=2mol\)
\(=>CTHH:P_2O_3\)
Đúng 1
Bình luận (0)
c2 :
\(m_O=\dfrac{110.43,46}{100}=48\left(g\right)\\
m_P=110-48=62\left(g\right)\\
n_O=\dfrac{48}{16}=3\left(mol\right)\\
n_P=\dfrac{62}{31}=2\left(mol\right)\)
-> CTHH là P2O3
Đúng 0
Bình luận (0)
gọi cthh có dạng chung là PxOy (x,y>0)
theo bài ra ta có
\(\dfrac{31x}{56,54\%}=\dfrac{16y}{43,46\%}=\dfrac{110}{100\%}\)
-> \(\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\)(tm)
-> CTHH : P2O3
Đúng 1
Bình luận (0)























