
Hóa học
Trung hòa 100ml dung dịch C cần dùng 35ml dung dịch gì thế bn ?
Đúng 0
Bình luận (3)
Các bạn cân bằng phương trình hóa học này cho mình nha
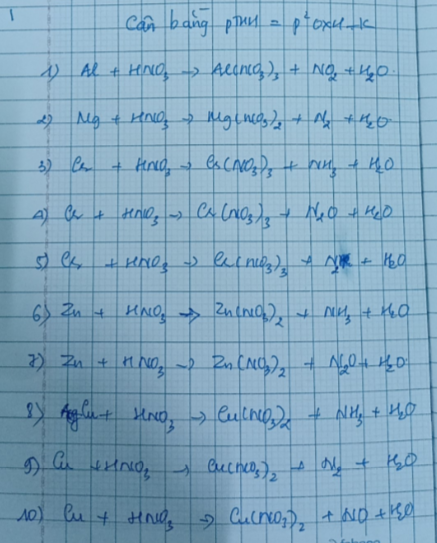
1) \(Al+6HNO_3\rightarrow Al\left(NO_3\right)_3+3NO_2+3H_2O\)
2) \(5Mg+12HNO_3\rightarrow5Mg\left(NO_3\right)_2+N_2+6H_2O\)
3) \(3Cr+27HNO_3\rightarrow8Cr\left(NO_3\right)_3+3NH_3+9H_2O\)
4) \(8Cr+30HNO_3\rightarrow8Cr\left(NO_3\right)_3+3N_2O+15H_2O\)
5) \(10Cr+36HNO_3\rightarrow10Cr\left(NO_3\right)_3+3N_2+18H_2O\)
6) \(4Zn+9HNO_3\rightarrow4Zn\left(NO_3\right)_2+NH_3+3H_2O\)
7) \(4Zn+10HNO_3\rightarrow4Zn\left(NO_3\right)_2+N_2O+5H_2O\)
8) \(8Cu+18HNO_3\rightarrow8Cu\left(NO_3\right)_2+2NH_3+6H_2O\)
9) \(5Cu+12HNO_3\rightarrow5Cu\left(NO_3\right)_2+N_2+6H_2O\)
10) \(3Cu+8HNO_3\rightarrow3Cu\left(NO_3\right)_2+2NO+4H_2O\)
Đúng 4
Bình luận (1)
một oxit biết kim loại có hóa trị III và chiếm 70% khối lượng là:
CTHH: `R_2O_3`
Ta có: \(\dfrac{2M_R}{2M_R+16.3}.100\%=70\%\)
=> MR = 56 (g/mol)
=> R là Fe
Đúng 3
Bình luận (0)
- Gọi CTHH của oxit kim loại đó là \(A_2O_3\) (do kim loại đó có hóa trị III).
-Vì kim loại đó chiếm 70% KL oxit.
\(\Rightarrow\)Oxi chiếm 30% KL oxit.
\(m_O=16.3=48\)
\(\Rightarrow m_{A_2O_3}=\dfrac{100.48}{30}=160\)
\(\Rightarrow2M_A+16.3=160\)
\(\Rightarrow M_A=56\).
\(\Rightarrow\)A là Fe (hóa trị III).
Đúng 2
Bình luận (0)
100g dd HCl phản ứng vừa đủ với 19g hh Na2CO3 và NaHCO3, sinh ra 4,48 lít khí ở đktc a) viết các ptpư xảy ra? b) tính khối lượng mỗi muối có trong hh? c) tính C% của dd HCl đã dùng? d) tính C% của dd chất thu được sau phản ứng?
a)
\(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2+H_2O\)
\(NaHCO_3+HCl\rightarrow NaCl+CO_2+H_2O\)
b)
Gọi số mol Na2CO3, NaHCO3 là a, b (mol)
=> 106a + 84b = 19 (1)
Thep PTHH: \(n_{CO_2}=a+b=\dfrac{4,48}{22,4}=0,2\left(mol\right)\) (2)
(1)(2) => a = 0,1 (mol); b = 0,1 (mol)
\(\left\{{}\begin{matrix}m_{Na_2CO_3}=0,1.106=10,6\left(g\right)\\m_{NaHCO_3}=0,1.84=8,4\left(g\right)\end{matrix}\right.\)
c) nHCl = 2a + b = 0,3 (mol)
=> mHCl = 0,3.36,5 = 10,95 (g)
=> \(C\%_{dd.HCl}=\dfrac{10,95}{100}.100\%=10,95\%\)
c) nNaCl = 2a + b = 0,3 (mol)
=> mNaCl = 0,3.58,5 = 17,55 (g)
mdd sau pư = 100 + 19 - 0,2.44 = 110,2 (g)
=> \(C\%_{NaCl}=\dfrac{17,55}{110,2}.100\%=15,9\%\)
Đúng 2
Bình luận (0)
a)
`Na_2CO_3 + 2HCl -> 2NaCl + CO_2 + H_2O`
`NaHCO_3 + HCl -> NaCl + CO_2 + H_2O`
b)
`n_{CO_2} = [4,48]/[22,4] = 0,2 (mol)`
Gọi `n_{Na_2CO_3} = a (mol); n_{NaHCO_3} = b (mol)`
`=> 106a + 84b = 19(1)`
Theo PT: `=> a + b = 0,2(2)`
`(1),(2) => a = b = 0,1`
`m_{Na_2CO_3} = 0,1.106 = 10,6 (g)`
`m_{NaHCO_3} = 0,1.84 = 8,4 (g)`
c)
Theo PT: `n_{HCl} = 2n_{CO_2} = 0,4 (mol)`
`=> C%_{HCl} = [0,4.36,5][100] .100% = 14,6%`
d)
`m_{dd.sau.pư} = 100 + 19 - 0,2.44 = 110,2 (g)`
Theo PT:`n_{NaCl} = 2n_{Na_2CO_3} + n_{NaHCO_3} = 0,3 (mol)`
`=> C%_{NaCl} = [0,3.58,5][110,2] .100% = 15,93%`
Đúng 1
Bình luận (0)
Nung x gam một hỗn hợp gồm KClO3 và KMnO4 ta thu được chất rắn A và khí O2. Biết KClO3 bị phân hủy hoàn toàn, KMnO4 phân hủy một phần. Trong A có 0,894 gam KCl chiếm 8,132% về khối lượng. Trộn O2 ở trên với không khí theo tỉ lệ 1:3 trong một bình kín ta thu được hỗn hợp khí B. Cho vào bình 0,528 gam cacbon rồi đốt cháy hết cacbonthu được hỗn hợp khí C gồm 3 khí. Trong đó CO2 chiếm 22,92% thể tích.1. Tìm x.2. Tính % theo khối lượng của các chất trong hỗn hợp ban đầu. Giả sử không khí có chứa 80%...
Đọc tiếp
Nung x gam một hỗn hợp gồm KClO3 và KMnO4 ta thu được chất rắn A và khí O2. Biết KClO3 bị phân hủy hoàn toàn, KMnO4 phân hủy một phần. Trong A có 0,894 gam KCl chiếm 8,132% về khối lượng. Trộn O2 ở trên với không khí theo tỉ lệ 1:3 trong một bình kín ta thu được hỗn hợp khí B. Cho vào bình 0,528 gam cacbon rồi đốt cháy hết cacbonthu được hỗn hợp khí C gồm 3 khí. Trong đó CO2 chiếm 22,92% thể tích.
1. Tìm x.
2. Tính % theo khối lượng của các chất trong hỗn hợp ban đầu. Giả sử không khí có chứa 80% N2 và 20% O2 về thể tích.
1)
Gọi số mol O2 sinh ra là a (mol)
=> nKK = 3a (mol)
\(\left\{{}\begin{matrix}n_{O_2\left(tổng\right)}=a+3a.20\%=1,6a\left(mol\right)\\n_{N_2}=3a.80\%=2,4a\left(mol\right)\end{matrix}\right.\)
\(n_C=\dfrac{0,528}{12}=0,044\left(mol\right)\)
\(m_A=\dfrac{0,894.100}{8,132}=11\left(g\right)\)
TH1: C gồm CO2, N2, O2
Bảo toàn C: \(n_{CO_2}=0,044\left(mol\right)\)
=> \(n_C=\dfrac{0,044.100}{22,92}=\dfrac{110}{573}\left(mol\right)\)
Bảo toàn O: \(n_{O_2\left(C\right)}=1,6a-0,044\left(mol\right)\)
C chứa \(\left\{{}\begin{matrix}CO_2:0,044\left(mol\right)\\O_2:1,6a-0,044\left(mol\right)\\N_2:2,4a\left(mol\right)\end{matrix}\right.\)
=> \(0,044+1,6a-0,044+2,4a=\dfrac{110}{573}\)
=> a = 0,048 (mol)
=> x = \(m_A+m_{O_2}=11+0,048.32=11,536\left(g\right)\)
TH2: C gồm CO2, CO, N2
Bảo toàn C: \(n_{CO_2}+n_{CO}=0,044\left(mol\right)\)
Bảo toàn O: \(2.n_{CO_2}+n_{CO}=3,2a\left(mol\right)\)
=> \(n_{CO_2}=3,2a-0,044\left(mol\right)\)
=> \(n_{hh.C}=\dfrac{\left(3,2a-0,044\right).100}{22,92}=\dfrac{8000}{573}a-\dfrac{110}{573}\left(mol\right)\)
Ta có: \(n_{hh.C}=n_{CO_2}+n_{CO}+n_{N_2}=0,044+2,4a=\dfrac{8000}{573}a-\dfrac{110}{573}\)
=> a = 0,02 (mol)
=> x = 11 + 0,02.32 = 11,64 (g)
2) \(n_{KCl}=\dfrac{0,894}{74,5}=0,012\left(mol\right)\)
PTHH: \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
0,008<-------0,012
- Với TH1: \(\%m_{KClO_3}=\dfrac{0,008.122,5}{11,536}.100\%=8,5\%\Rightarrow\%m_{KMnO_4}=100\%-8,5\%=91,5\%\)
- Với TH2:
\(\%m_{KClO_3}=\dfrac{0,008.122,5}{11,64}.100\%=8,42\%\Rightarrow\%m_{KMnO_4}=100\%-8,42\%=91,58\%\)
Đúng 1
Bình luận (0)
Hỗn hợp M gồm kim loại X (hóa trị II) và kim loại Y ( hóa trị III), có tỉ lệ mol là 1:2. Hòa tan hoàn toàn 11,7g hỗn hợp M bằng một lượng H2SO4 loãng dư thu được dd A và 13,44 lít H2 (đkc). Hỏi X và Y là 2 kim loại nào?
Giúp mình với, please!!
Gọi \(\left\{{}\begin{matrix}n_X=a\left(mol\right)\\n_Y=2a\left(mol\right)\end{matrix}\right.\)
=> a.MX +2a.MY = 11,7 (1)
\(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: \(X+H_2SO_4\rightarrow XSO_4+H_2\)
\(2Y+3H_2SO_4\rightarrow Y_2\left(SO_4\right)_3+3H_2\)
Theo PTHH: \(n_{H_2}=n_X+1,5.n_Y=a+3a=0,6\left(mol\right)\)
=> a = 0,15 (mol)
(1) => MX + 2.MY = 78
Chỉ có MX = 24 (g/mol) ; MY = 27 (g/mol)
=> X là Mg, Y là Al
Đúng 2
Bình luận (0)
Cho 200 g dd NaOH có chứa 0,1 mol chất tan (Biết ddd = 1,2 g/ml). Tính CM và C% của dd này.
\(m_{NaOH}=0,1.40=4\left(g\right)\)
=> \(C\%=\dfrac{4}{200}.100\%=2\%\)
\(V_{dd}=\dfrac{200}{1,2}=\dfrac{500}{3}\left(ml\right)=\dfrac{1}{6}\left(l\right)\)
=> \(C_M=\dfrac{0,1}{\dfrac{1}{6}}=0,6M\)
Đúng 2
Bình luận (0)
Lấy bao nhiêu ml dd NaOH 25% (d = 1,28 g/ml) để pha thành 200 g dd NaOH 16%.
\(m_{NaOH}=\dfrac{200.16}{100}=32\left(g\right)\)
=> \(m_{dd.NaOH.25\%}=\dfrac{32.100}{25}=128\left(g\right)\)
=> \(V_{dd.NaOH.25\%}=\dfrac{128}{1,18}=100\left(ml\right)\)
Đúng 2
Bình luận (0)
cho ba nguyên tử của 3 nguyên tố A B C có tổng số hạt mang điện trong chúng tương ứng với tỷ lệ 3: 4 :5 a) xác định số lượng từng loại hạt a,b,c biết hiệu của số giữa hạt mang điện trong nguyên tử A và số hạt mang điện trong hạt nhân nguyên tử C bằng 3 , khôi lượng p bằng khối lượng n bằng 1 đvC , khối lượng e không đáng kể . b) tính khối lượng tuyệt đối của mỗi nguyên tử a,b,cgiúp mình với ạ
Đọc tiếp
cho ba nguyên tử của 3 nguyên tố A B C có tổng số hạt mang điện trong chúng tương ứng với tỷ lệ 3: 4 :5 a) xác định số lượng từng loại hạt a,b,c biết hiệu của số giữa hạt mang điện trong nguyên tử A và số hạt mang điện trong hạt nhân nguyên tử C bằng 3 , khôi lượng p bằng khối lượng n bằng 1 đvC , khối lượng e không đáng kể . b) tính khối lượng tuyệt đối của mỗi nguyên tử a,b,c
giúp mình với ạ
a) Ta có: \(\left\{{}\begin{matrix}\dfrac{p_A}{3}=\dfrac{p_B}{4}=\dfrac{p_C}{5}\\2p_A-p_C=3\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}p_A=9\\p_B=12\\p_C=15\end{matrix}\right.\)
=> A là F, B là Mg, C là P
F chứa 9 hạt proton, 9 hạt electron, 10 hạt nơtron
Mg chứa 12 hạt proton, 12 hạt electron, 12 hạt nơtron
P chứa 15 hạt proton, 15 hạt electron, 16 hạt nơtron
b)
NTKA = 9.1 + 10.1 = 19 (đvC)
NTKB = 12.1 + 12.1 = 24 (đvC)
NTKC = 15.1 + 16.1 = 31 (đvC)
Đúng 1
Bình luận (2)
Cho y (g) K3PO4 vào nước vừa đủ đc 500 g dd K3PO4 0,5M (d = 1,25 g/ml). Tính giá trị của y.
\(V_{dd.K_3PO_4}=\dfrac{500}{1,25}=400\left(ml\right)=0,4\left(l\right)\\ \Rightarrow n_{K_3PO_4}=0,4.0,5=0,2\left(mol\right)\\ \Rightarrow y=0,2.212=42,4\left(g\right)\)
Đúng 2
Bình luận (0)
Vdd. K3 PO4 = 500/1,25 = 400 ml = 0,4 (l)
==> nK3 PO4 = 0,4.0,5 = 0,2 mol
==> y = 0,2.212 = 42,4 g
Đúng 1
Bình luận (0)
















