Câu 5 Hòa tan hoàn toàn một oxít kim loại hóa trị 2 (MO) vào một lượng dung dịch HCl 14,6% (vừa đủ) ta được dung dịch Y chứa có nồng độ 17,59%. Xác định nguyên tử khối của M
Hóa học
Giả sử có 1 mol MO
PTHH: \(MO+2HCl\rightarrow MCl_2+H_2O\)
1------>2-------->1
=> \(\left\{{}\begin{matrix}m_{MO}=M_M+16\left(g\right)\\m_{HCl}=36,5.2=73\left(g\right)\\m_{MCl_2}=M_M+71\left(g\right)\end{matrix}\right.\)
=> \(m_{ddHCl}=\dfrac{73}{14,6\%}=500\left(g\right)\)
=> \(m_{dd\text{ }sau\text{ }pư}=500+M_M+16=516+M_M\left(g\right)\)
=> \(C\%_{MCl_2}=\dfrac{M_M+71}{M_M+516}.100\%=17,59\%\)
=> MM = 24 (g/mol)
=> M là Mg
NTK của Mg là 24 đvC
Đúng 0
Bình luận (0)
Ba(HCO3)2 khi tác dụng với quỳ tím hó đổ hay xanh?
Dd \(Ba\left(HCO_3\right)_2\) làm quỳ hoá xanh, vì Ba là kim loại mạnh, \(-HCO_3\) là gốc axit yếu.
Đúng 0
Bình luận (0)
Câu 4.(Đề chuyên LHP) Hòa tan hoàn toàn a gam CuO vào 420gam dung dịch H2SO4 40% ta được dung dịch X chứa H2SO4 dư có nồng độ 14% và CuSO4 có nồng độ C%. Tính a và C.
Câu 3.(Đề chuyên LHP) Cho 44,8 lít khí HCl (ở điều kiện tiêu chuẩn) hòa tan hoàn toàn vào 327 gam nước được dung dịch A
a) Tính nồng độ % của dung dịch A
b) Cho 50gam CaCO3 vào 250gam dung dịch A, đun nhẹ đến khi phản ứng xảy ra hoàn toàn ta được dung dịch B. Tính nồng độ % các chất có trong dung dịch B.
Câu 2. Dẫn CO đến dư đi qua 26,2 gam hỗn hợp X gồm Fe2O3, Al2O3, CuO nung nóng cho đến khi phản ứng xảy ra hoàn toàn. Sau phản ứng thu được 22,2 gam chất rắn Y. Cho hỗn hợp Y tác dụng vừa đủ với 350ml dung dịch HCl 2M. Hãy viết các phương trình phản ứng xảy ra và tính % số mol của mỗi chất trong hỗn hợp X.
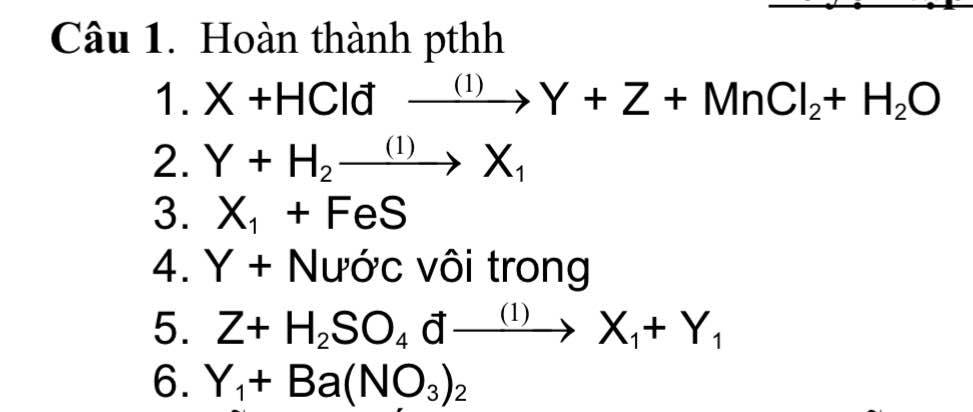
1) \(2KMnO_4+16HCl\text{ đặc}\rightarrow5Cl_2+2KCl+2MnCl_2+8H_2O\)
⇒ Y là Cl2, Z là KCl.
2) \(Cl_2+H_2\rightarrow2HCl\) (ĐK: đưa ra ánh sáng)
⇒ X1 là HCl.
3) \(2HCl+FeS\rightarrow FeCl_2+H_2S\)
4) \(2Cl_2+2Ca\left(OH\right)_2\rightarrow CaCl_2+Ca\left(OCl\right)_2+2H_2O\)
5) \(2KCl+H_2SO_4\text{ đặc}\rightarrow2HCl+K_2SO_4\)
⇒ Y1 là K2SO4.
6) \(K_2SO_4+Ba\left(NO_3\right)_2\rightarrow BaSO_4\downarrow+2KNO_3\)
Đúng 1
Bình luận (0)
feco3 + hno3 đặc nóng ->
\(3FeCO_3+10HNO_3\rightarrow5H_2O+NO+3Fe\left(NO_3\right)_3+3CO_2\)
Đúng 1
Bình luận (0)
Để pha được 500ml dd nước muối sinh lý(C%=0,9%) cần lấy bao nhiêu ml dd NaCl 3%
Biết độ tan của MgSO4 ở 80 độ C là 64,2g và ở 20 độ C là 44,5g, xác định khối lượng tinh thể MgSO4 . 6H2O tách khỏi dd khi hạ nhiệt độ 1642g dd bão hòa MgSO4 ở 80=>20 độ C
Ở $80^oC$, $S_{MgSO_4} = 64,2(gam)$
$\Rightarrow m_{MgSO_4} = 1642. \dfrac{64,2}{100 + 64,2} = 642(gam)$
$m_{H_2O} = 1642 - 642 = 1000(gam)$
Gọi $n_{MgSO_4.6H_2O} = a(mol)$
Sau khi tách tinh thể :
$m_{MgSO_4} = 642 - 120a(gam)$
$m_{H_2O} = 1000 - 18.6a = 1000 - 108a(gam)$
Ở $20^oC$, $S_{MgSO_4} = \dfrac{642-120a}{1000 - 108a}.100 = 44,5(gam)$
$\Rightarrow a = 2,74$
$m_{MgSO_4.6H_2O} = 2,74.228 = 624,72(gam)$
Đúng 2
Bình luận (0)
Hoàn thành sơ đồ phương trình sau:a)CaO + H2O ---b)BaO + CO2 ---c)Al2O3 + HCl ---d)KOH +H2SO4 ---e)K2O + CO2 ---f)Fe2O3 + HNO3 ---g)SO3 + H2O ---h)BaO + H2O ---i)Fe2O3 + CO2 ---k)CaO + H2O ---
Đọc tiếp
Hoàn thành sơ đồ phương trình sau:
a)CaO + H2O --->
b)BaO + CO2 --->
c)Al2O3 + HCl --->
d)KOH +H2SO4 --->
e)K2O + CO2 --->
f)Fe2O3 + HNO3 --->
g)SO3 + H2O --->
h)BaO + H2O --->
i)Fe2O3 + CO2 --->
k)CaO + H2O --->
\(a) CaO + H_2O \to Ca(OH)_2\\ b) BaO + CO_2 \xrightarrow{t^o} BaCO_3\\ c) Al_2O_3 + 6HCl \to 2AlCl_3 + 3H_2O\\ d) 2KOH + H_2SO_4 \to K_2SO_4 + 2H_2O\\ e) K_2O + CO_2 \xrightarrow{t^o} K_2CO_3\\ f) Fe_2O_3 + 6HNO_3 \to 2Fe(NO_3)_3 + 3H_2O\\ g) SO_3 + H_2O \to H_2SO_4\\ h) BaO + H_2O\to Ba(OH)_2\\ i) Fe_2O_3 + 3CO \xrightarrow{t^o} 2Fe +3CO_2\\ k) CaO + H_2O \to Ca(OH)_2\)
Đúng 1
Bình luận (0)
a)CaO+H2O→Ca(OH)2
b)BaO+CO2to→BaCO3
c)Al2O3+6HCl→2AlCl3+3H2O
d)2KOH+H2SO4→K2SO4+2H2O
e)K2O+CO2to→K2CO3
f)Fe2O3+6HNO3→2Fe(NO3)3+3H2O
g)SO3+H2O→H2SO4
h)BaO+H2O→Ba(OH)2
i)Fe2O3+3COto→2Fe+3CO2
k)CaO+H2O→Ca(OH)2
Đúng 0
Bình luận (0)
a) CaO + H2O → Ca(OH)2
b) BaO +CO2 to → BaCO3
c) Al2O3 + 6HCl → 2AlCl3 + 3H2O
d) 2KOH + H2SO4→ K2SO4 + 2H2O
e) K2O + CO2 to → K2CO3
f) Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O
g) SO3 +H2O → H2SO4
h) BaO + H2O → Ba(OH)2
i) Fe2O3 + 3CO to→ 2Fe + 3CO2
k) CaO + H2O → Ca(OH)2
Đúng 0
Bình luận (0)