trong một nguyên tử có tổng số hạt là 95 số hạt không mang điện bằng 0,5833 số hạt mang điện. Số proton của nguyên tử đó là
Hóa học
Tổng số hạt của nguyên tử là 95, nên:
\(P+E+N=95\left(1\right)\)
Nguyên tử này trung hoà về điện nên:
\(P=E=Z\left(2\right)\)
Theo đề bài, số hạt không mang điện bằng 0,5833 số hạt mang điện:
\(N=0,5833.\left(P+E\right)\\ \Leftrightarrow N-1,1666P=0\left(3\right)\)
Từ (1), (2), (3) ta lập hệ pt:
\(\left\{{}\begin{matrix}P+E+N=95\\P=E=Z\\N-1,1666P=0\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P=E=Z=30\\N=35\end{matrix}\right.\)
Vậy nguyên tử đó có 30 proton
Đúng 2
Bình luận (0)
cho nguyên tử x có tổng số hạt là 48 trong đó tổng số hạt mang điện gấp đôi số hạt không mang điện.Số electron lớp ngoài cùng của nguyên tử x là
Vì tổng số hạt cơ bản của nguyên tử X là 48 => P+E+N=48 (1)
Mặt khác, X là nguyên tử nên nó trung hoà về điện: P=E=Z (2)
Theo đề bài, số hạt mang điện gấp đôi số hạt không mang điện: (P+E)= 2N (3)
Thế (2) vào (1) và (3) ta được: 2P + N= 48 ; P=E=N=Z
=> 3P=48 => P=E=N=Z=16
Nguyên tử X (Z=16) cấu hình: 1s22s22p63s23p4 => Có 6e lớp ngoài cùng (Lớp M)
Đúng 3
Bình luận (0)
nguyên tử x có tổng là hạt trong nguyên tử là 36.biết số hạt mang điện nhiều hơn hạt ko mang điện là 12 .số electron lớp ngoài cùng của nguyên tử x là
Nguyên tử X có tổng số hạt cơ bản là 36: P+E+N=36 (1)
Mà nguyên tử X trung hoà về điện, nên: P=E=Z (2)
Mặt khác, số hạt mang điện nhiều hơn số hạt không mang điện là 12: (P+E) - N = 12 (3)
Thế (2) vào (1) và (3) ta được:
2P + N=36 (4) ; 2P - N= 12 (5)
Lấy (4) cộng (5) , ta được: 4P = 48 <=>P=E=Z=12 và N=12
Cấu hình electron: 1s22s22p63s2 => Lớp ngoài cùng (Lớp M) của nguyên tử X có 2 electron
Đúng 2
Bình luận (0)
nguyên tử y có tổng các hạt cơ bản là 93.Hạt mang điện nhiều hơn hạt không mang điện là 23 số hạt electron là
Vì tổng số hạt cơ bản của Y là 93 => P+E+N=93 (1)
Mà nguyên tử Y trung hoà về điện nên có : P=E=Z (2)
Tổng số hạt mang điện nhiều hơn số hạt không mang điện là 23 hạt, nên:
(P+E) - N=23 (3)
Từ (1), (2), (3) => P=E=Z=29; N=35
Đúng 3
Bình luận (0)
Nguyên tử Al có tổng số hạt là 52 trong đó có điện tích hạt nhân là+17 . Tìm số hạt nhân mỗi loại
\(\left\{{}\begin{matrix}P=E=Z=17\\N=52-2P=52-2.17=18\end{matrix}\right.\)
Đúng 2
Bình luận (0)
đốt cháy khí metan (CH4) trong không khí được 3,36 lít khí cacbonic .hãy tìm thể tích khí oxi (đktc) đã tham gia phản ứng
\(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
0,3 0,15
\(VO_2=0,3.22,4=6,72\left(l\right)\)
Đúng 2
Bình luận (0)
Nêu hiện tượng khi nhỏ \(H_2SO_4\)đặc vào bông gòn
Xuất hiện khí không màu mùi hắc và chất rắn màu đen
$C_n(H_2O)_m \xrightarrow{H_2SO_{4_{đặc}}} nC + mH_2O$
$C + 2H_2SO_4 \to CO_2 + SO_2 + 2H_2O$
Đúng 1
Bình luận (0)
xuất hiện chất rắn màu đen và có khí thoát ra?
Đúng 1
Bình luận (0)
Để xác định hàm lượng của FeCO3 trong quặng xiđerit, người ta làm như sau: Cân 0,600 gam mẫu quặng , chế hóa nó theo một quy trình hợp lý , thu dung dịch FeSO4 trong môi trường H2SO4 loãng. Chuẩn độ dung dịch thu được bằng dung dịch chuẩn KMnO4 0,025M thì dùng vừa hết 25,2 ml dung dịch chuẩn. Thành phần phần trăm theo khối lượng của FeCO3 trong quặng là.
Đọc tiếp
Để xác định hàm lượng của FeCO3 trong quặng xiđerit, người ta làm như sau: Cân 0,600 gam mẫu quặng , chế hóa nó theo một quy trình hợp lý , thu dung dịch FeSO4 trong môi trường H2SO4 loãng. Chuẩn độ dung dịch thu được bằng dung dịch chuẩn KMnO4 0,025M thì dùng vừa hết 25,2 ml dung dịch chuẩn. Thành phần phần trăm theo khối lượng của FeCO3 trong quặng là.
Đáp án:60,9%
GT
\(n_{KMnO_4}=CM.V=0,025.0,0252=0,0063mol\)
\(FeCO_3+H_2SO_{4loãng}\rightarrow FeSO_4+CO_2\uparrow+H_2O.\left(1\right)\)
\(0,00315\leftarrow\) \(0,00315\)
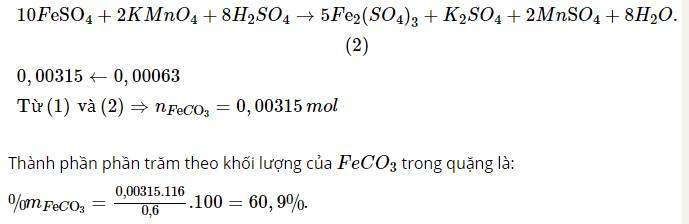
Đúng 1
Bình luận (0)
giúp mik với mai nộp r
r
Câu 16:
\(Đặt:\%n_{^{37}Cl}=a;\%n_{^{35}Cl}=100\%-a\left(a>0\right)\\ \overline{NTK}_{Cl}=35,5\\ \Leftrightarrow37.a+35.\left(100\%-a\right)=35,5\\ \Leftrightarrow a=25\%\Rightarrow\%m_{\dfrac{^{37}Cl}{MgCl_2}}=\dfrac{71}{95}.25\%.100\%=\dfrac{71}{380}\\ \Rightarrow m=m_{MgCl_2}=1,11:\dfrac{71}{380}\approx5,94\left(g\right)\)
Đúng 3
Bình luận (0)
Em ơi mình chụp rõ hơn được không em?
Đúng 1
Bình luận (2)
Cho 40g hỗn hợp Na2O và CuO tác dụng hết với 6,72l SO2 (đktc). Sau phản ứng thấy thu được 1 chất rắn không tan. Thành phần % theo khối lượng của 2 oxit trong hỗn hợp lần lượt là
\(Na_2O+SO_2\rightarrow Na_2SO_3\\ n_{Na_2O}=n_{SO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ \%m_{\dfrac{Na_2O}{hh}}=\dfrac{0,3.62}{40}.100\%=46,5\%\\ \Rightarrow\%m_{\dfrac{CuO}{hh}}=100\%-46,5\%=53,5\%\)
Đúng 2
Bình luận (0)
$Na_2O + SO_2 \xrightarrow{t^o} Na_2SO_3$
$n_{Na_2O} = n_{SO_2} = \dfrac{6,72}{22,4} = 0,3(mol)$
$\%m_{Na_2O} = \dfrac{0,3.62}{40}.100\% = 93\%$
$\%m_{CuO} = 100\% = 93\% = 7\%$
Đúng 1
Bình luận (1)

















