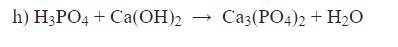Một học sinh viết 1 số CTHH như sau: C2O,CuO2,AL2SO4,KNO3,CaO,NO2,Na3O,Fe2O3 hãy cho biết CTHH nào viết sai và sữa lại cho đúng
Hóa học
C2O ⇒ Sai, sửa: CO2
CuO2 ⇒ Sai, sửa: CuO
Al2SO4 ⇒ Sai, sửa: Al2(SO4)3
KNO3 ⇒ Đúng
CaO ⇒ Đúng
NO2 ⇒ Đúng
Na3O ⇒ Sai, sửa: Na2O
Fe2O3 ⇒ Đúng
Đúng 2
Bình luận (0)
\(2H_3PO_4+3Ca\left(OH\right)_2\xrightarrow[]{}Ca_3\left(PO_4\right)_2\downarrow+6H_2O\)
Đúng 2
Bình luận (0)
cho 13g zn vào trong dd hcl có nồng độ 1M hãy tính thể tích hcl và khối lượng của oxi để đốt hết lượng khí vừa sinh ra
\(Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\ n_{HCl}=2n_{Zn}=0,4\left(mol\right)\\ V_{HCl}=\dfrac{0,4}{1}=0,4\left(l\right)\\ n_{H_2}=n_{Zn}=0,2\left(mol\right)\\ O_2+2H_2-^{t^o}\rightarrow2H_2O\\ n_{O_2}=\dfrac{1}{2}n_{H_2}=0,1\left(mol\right)\\ \Rightarrow V_{O_2}=0,1.32=3,2\left(g\right)\)
Đúng 0
Bình luận (0)
Hòa tan 17,4 gam hỗn hợp Al, Fe, Cu trong dung dịch HCl dư, thấy còn 6,4 gam chất rắn. Khí sinh ra đốt hoàn toàn thu được 7,2 gam hơi nước.
a) Viết các PTHH của phản ứng xảy ra.
b) Tính phần trăm khối lượng mỗi kim loại.
Có một hỗn hợp dạng bột gồm Al và Fe. Hãy nêu cách tiến hành thí nghiệm để xác định phần trăm khối lượng của mỗi kim loại trong hỗn hợp?
a) Phương pháp vật lý.
b) Phương pháp hóa học
Hòa tan 8 gam hỗn hợp A gồm Mg, Cu vào trong dung dịch H2SO4 loãng, sau phản ứng hoàn toàn thì thấy có 4,48 lít (đktc) khí không màu thoát ra. Tính % khối lượng mỗi kim loại trong hỗn hợp A
Giải thích vì sao nguyên tử(kim loại,phi kim) có giá trị như phân tử
CTHH dùng để biểu diễn....... ,gồm .........và..........ghi ở chân .CTHH của..........chỉ gồm một............., còn của .............gồm từ hai.............. trở lên
CTHH dùng để biểu diễn chất, gồm một kí hiệu hóa học (đơn chất) hay hai,ba kí hiệu (hợp chất ) và chỉ số ghi ở chân . CTHH của đơn chất chỉ gồm một kí hiệu , còn của hợp chất gồm từ hai kí hiệu trở lên
Đúng 0
Bình luận (0)
Bài 3:
a)
Gọi số mol ZnO, Fe2O3 là a, b (mol)
=> 81a + 160b = 24,1 (1)
\(n_{H_2SO_4}=0,4.1=0,4\left(mol\right)\)
PTHH: \(ZnO+H_2SO_4\rightarrow ZnSO_4+H_2O\)
a------->a----------->a
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
b--------->3b----------->b
=> a + 3b = 0,4 (2)
(1)(2) => a = 0,1 (mol); b = 0,1 (mol)
=> \(\left\{{}\begin{matrix}\%ZnO=\dfrac{0,1.81}{24,1}.100\%=33,61\%\\\%Fe_2O_3=\dfrac{0,1.160}{24,1}.100\%=66,39\%\end{matrix}\right.\)
b)
\(\left\{{}\begin{matrix}C_{M\left(ZnSO_4\right)}=\dfrac{0,1}{0,4}=0,25M\\C_{M\left(Fe_2\left(SO_4\right)_3\right)}=\dfrac{0,1}{0,4}=0,25M\end{matrix}\right.\)
\(m_{dd.H_2SO_4}=400.1,2=480\left(g\right)\)
\(m_{dd.sau.pư}=480+24,1=504,1\left(g\right)\)
\(\left\{{}\begin{matrix}C\%_{ZnSO_4}=\dfrac{0,1.161}{504,1}.100\%=3,2\%\\C\%_{Fe_2\left(SO_4\right)_3}=\dfrac{0,1.400}{504,1}.100\%=7,935\%\end{matrix}\right.\)
c)
\(n_{NaOH}=0,85.1=0,85\left(mol\right)\)
PTHH: \(ZnSO_4+2NaOH\rightarrow Zn\left(OH\right)_2\downarrow+Na_2SO_4\)
0,1-------->0,2---------->0,1
\(Fe_2\left(SO_4\right)_3+6NaOH\rightarrow2Fe\left(OH\right)_3\downarrow+3Na_2SO_4\)
0,1--------->0,6----------->0,2
\(Zn\left(OH\right)_2+2NaOH\rightarrow Na_2ZnO_2+2H_2O\)
0,025<-------0,05
Kết tủa gồm \(\left\{{}\begin{matrix}Zn\left(OH\right)_2:0,1-0,025=0,075\left(mol\right)\\Fe\left(OH\right)_3:0,2\left(mol\right)\end{matrix}\right.\)
=> mkết tủa = 0,075.99 + 0,2.107 = 28,825 (g)
d)
- Nếu nung đến 100%:
PTHH: \(Zn\left(OH\right)_2\underrightarrow{t^o}ZnO+H_2O\)
0,075----->0,075
\(2Fe\left(OH\right)_3\underrightarrow{t^o}Fe_2O_3+3H_2O\)
0,2------->0,1
=> mrắn = 0,075.81 + 0,1.160 = 22,075 (g)
Vậy khi nung đến 90% thì mT = 22,075.90% = 19,8675 (g)
Đúng 2
Bình luận (0)