cho hỗn hợp khí A gồm Co2 và O2 có tỉ lệ thể tích tương ứng là 5:1
a) tính tỉ khối của hỗn hợp khí a với không khí
b)tính thể tích(ĐKTC) của 10,5 g khí A
cho hỗn hợp khí A gồm Co2 và O2 có tỉ lệ thể tích tương ứng là 5:1
a) tính tỉ khối của hỗn hợp khí a với không khí
b)tính thể tích(ĐKTC) của 10,5 g khí A
a, \(\dfrac{V_{CO_2}}{V_{O_2}}=\dfrac{n_{CO_2}}{n_{O_2}}=\dfrac{5}{1}\)
→ Gọi: nO2 = a (mol) ⇒ nCO2 = 5a (mol)
\(\Rightarrow M_A=\dfrac{32a+44.5a}{a+5a}=42\left(g/mol\right)\)
\(\Rightarrow d_{A/kk}=\dfrac{42}{29}\approx1,45\)
b, Ta có: \(n_A=\dfrac{10,5}{42}=0,25\left(mol\right)\Rightarrow V_A=0,25.22,4=5,6\left(l\right)\)
Đốt cháy 8g khí methane trong không khí ( phản ứng xảy ra hoàn toàn ), sinh ra hỗn hợp khí gồm CO2 và nước. Dẫn hỗn hợp trên vào nước vôi trong, sinh ra m(g) kết tủa. Tính m.
6.
\(n_{CH_4}=\dfrac{8}{16}=0,5\left(mol\right)\)
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
_____0,5_________0,5 (mol)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,5___________________0,5 (mol)
⇒ mCaCO3 = 0,5.100 = 50 (g)
Đốt cháy 8g khí methane trong không khí ( phản ứng xảy ra hoàn toàn ), sinh ra hỗn hợp khí gồm CO2 và nước. Dẫn hỗn hợp trên vào nước vôi trong, sinh ra m(g) kết tủa. Tính m.
\(CH_4+2O_2\rightarrow CO_2+2H_2O\left(1\right)\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\left(2\right)\)
\(n_{CH_4}=\dfrac{m}{M}=\dfrac{8}{16}=0,5\left(mol\right)\)
Từ \(\left(1\right)\Rightarrow n_{CO_2}=n_{CH_4}=0,5\left(mol\right)\)
\(\left(2\right)\Rightarrow n_{CaCO_3}=n_{CO_2}=0,5\left(mol\right)\)
\(m_{CaCO_3}=n.M=0,5.\left(40+12+3.16\right)=50\left(g\right)\)
Vậy kết tủa \(CaCO_3\) có \(m=50\left(g\right)\)
1) Phenolphtalein sẽ làm mẫu chuyển sang màu hồng nhạt
\(\rightarrow NaOH\)
Phenolphtalein sẽ làm mẫu chuyển sang không màu
\(\rightarrow H_2SO_4\)
Còn lại 2 mẫu \(MgCl_2;NaNO_3\)
\(2NaOH+MgCl_2\rightarrow Mg\left(OH\right)_2\downarrow+2NaCl\)
\(\Rightarrow\) Phản ứng cho ra kết tủa trắng \(\rightarrow MgCl_2\)
Còn lại là \(NaNO_3\)
Bài 1: Viết phương trình phản sứng xảy ra nếu có khi cho các kim loại Mg , Al , Fe vào dung dịch ZnSO4
Bài 2: Cho 2,4g Mg tác dụng với dung dịch HCL . Tính khối lượng các chất thu được sau phản ứng .
Do 2 bài trùng lặp nên mình làm tiện thể nhé.
`Mg+ZnSO_4->MgSO_4+Zn`
`2Al+3ZnSO_4->Al_2(SO_4)_3+3Zn`
Bài 2
PTHH:
`Mg+2HCl->MgCl_2+H_2`
0,1------------0,1---------0,1 mol
`n Mg=(2,4)/24=0,1 mol
=>`m_(MgCl_2)=0,1.95=9,5g`
=>`m_(H_2)=0,1.2=0,2g`
Viết phương trình phản ứng xảy ra nếu có khi cho các kim loại Mg , Al , Fe vào dung dịch ZnSO4
+, Trong 3 kim loại Mg, Al, Fe chỉ có duy nhất Fe không phản ứng với dung dịch ZnSO4.
+, PTPU: Mg + ZnSO4 -> MgSO4 + Zn
2Al + 3ZnSO4 -> Al2(SO4)3 + 3Zn
viết phương trình phản ứng xảy ra nếu có khi cho các kim loại sau : Ba , K , Mg , Fe , Al , Cu , Ag :
a) tác dụng với O2 ;
b) tác dụng với Cl2 ;
c) tác dụng với H2SO4 ;
d) tác dụng với H2O
a)
`2Ba+O_2->2BaO`
`4K+O_2->2K_2O`
`2Mg+O_2->2MgO`
`3Fe+2O_2->Fe_3O_4` (to)
`4Al+3O_2->2Al2_O3`
`2Cu+O_2->2CuO`(to)
b)
`Ba+Cl_2->BaCl_2`
`2K+Cl_2->2KCl`
`Mg+Cl_2->MgCl_2`
`Fe+Cl_2->FeCl_3`(to)
`Al+Cl_2->AlCl_3`(to)
c)
`Ba+H_2SO_4->BaSO_4+H_2`
`K+H_2SO_4->K_2SO_4+H_2`
`Mg+H_2SO_4->MgSO_4+H_2`
`Fe+H_2SO_4->FeSO_4+H_2`
`2Al+3H_2SO_4->Al2(SO_4)_3+3H_2`
d)
`Ba+2H_2O->Ba(OH)_2+H_2`
`2K+2H_2O->2KOH+H_2`
Tham khảo.
đọ tan của CUSO4 ở nhiệt độ t1 laaf 20g t2 là 34.2g người ta lấy 134.2 dd bh ở nhiệt đọ t2 hạ xuống nhiết độ t1 tách ra 25g tinh thể CUSO4.nH2Otìm ct
Tính khối lượng nước trong 134.2g dung dịch:
Đặt khối lượng nước là x, khối lượng CUSO4 là y. Ta có:
Khi đó:
y=134.2g−100g=34.2gy=134.2g−100g=34.2gTính khối lượng nước trong 25g tinh thể CUSO4·nH2O:
Khi hạ nhiệt độ xuống t1, CUSO4 sẽ kết tinh:
Tính số mol CUSO4:
Khối lượng mol CUSO4 = 159.61g/mol.
Ta tính ra được n:
25g=25g+n⋅18g/mol ⟹ n≈525g=25g+n⋅18g/mol⟹n≈5Vậy, công thức phân tử của CUSO4·nH2O là CUSO4·5H2O.
1. PT: \(CuCl_2+2NaOH\rightarrow Cu\left(OH\right)_2+2NaCl\)
2. \(n_{CuCl_2}=\dfrac{270.5\%}{135}=0,1\left(mol\right)\)
Theo PT: \(n_{Cu\left(OH\right)_2}=n_{CuCl_2}=0,1\left(mol\right)\)
⇒ mCu(OH)2 = 0,1.98 = 9,8 (g)
3. \(n_{NaOH}=2n_{CuCl_2}=0,2\left(mol\right)\)
\(\Rightarrow C\%_{NaOH}=\dfrac{0,2.40}{80}.100\%=10\%\)
4. \(n_{NaCl}=2n_{CuCl_2}=0,2\left(mol\right)\)
Ta có: m dd sau pư = 270 + 80 - 9,8 = 340,2 (g)
\(\Rightarrow C\%_{NaCl}=\dfrac{0,2.58,5}{340,2}.100\%\approx3,4\%\)
Hoàn thiện các PTHH sau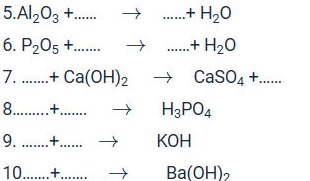
5. \(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
6. \(P_2O_5+6NaOH\rightarrow2Na_3PO_4+3H_2O\)
7. \(H_2SO_4+Ca\left(OH\right)_2\rightarrow CaSO_4+2H_2O\)
8. \(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
9. \(K_2O+H_2O\rightarrow2KOH\)
10. \(BaO+H_2O\rightarrow Ba\left(OH\right)_2\)