Có 3 lọ hóa chất không nhãn chứa lần lượt một trong ba đúng dịch Cả(OH)2 H2SO4 và Na2SO4 . Trình bày phương pháp hóa học nhận biết ba lọ hóa chất trên ? ( Viết phản ứng xảy ra nếu có )
Đề kiểm tra 1 tiết chương I: Các loại hợp chất vô cơ-Đề 1
| \(Ca\left(OH\right)_2\) | \(H_2SO_4\) | \(Na_2SO_4\) | |
| quỳ tím | xanh | đỏ | _ |
Đúng 0
Bình luận (0)
Cho a gam Zn vào 200g đ HCl thoát ra 3,36l khí H2(dktc) A) tìm m gam Zn B)Tìm m zncl2 C) Tính C% đ hcl
\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,15<---0,3<-----0,15<-----0,15
a) \(m_{Zn}=0,15.65=9,75\left(g\right)\)
b) \(m_{ZnCl2}=0,15.136=20,4\)
c) \(C\%_{ddHCl}=\dfrac{0,3.36,5}{200}.100\%=5,475\%\)
Đúng 2
Bình luận (0)
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
a, \(n_{Zn}=n_{H_2}=0,15\left(mol\right)\Rightarrow m_{Zn}=0,15.65=9,75\left(g\right)\)
b, \(n_{ZnCl_2}=n_{H_2}=0,15\left(mol\right)\Rightarrow m_{ZnCl_2}=0,15.136=20,4\left(g\right)\)
c, \(n_{HCl}=2n_{H_2}=0,3\left(mol\right)\Rightarrow C\%_{HCl}=\dfrac{0,3.36,5}{200}.100\%=5,475\%\)
Đúng 1
Bình luận (0)
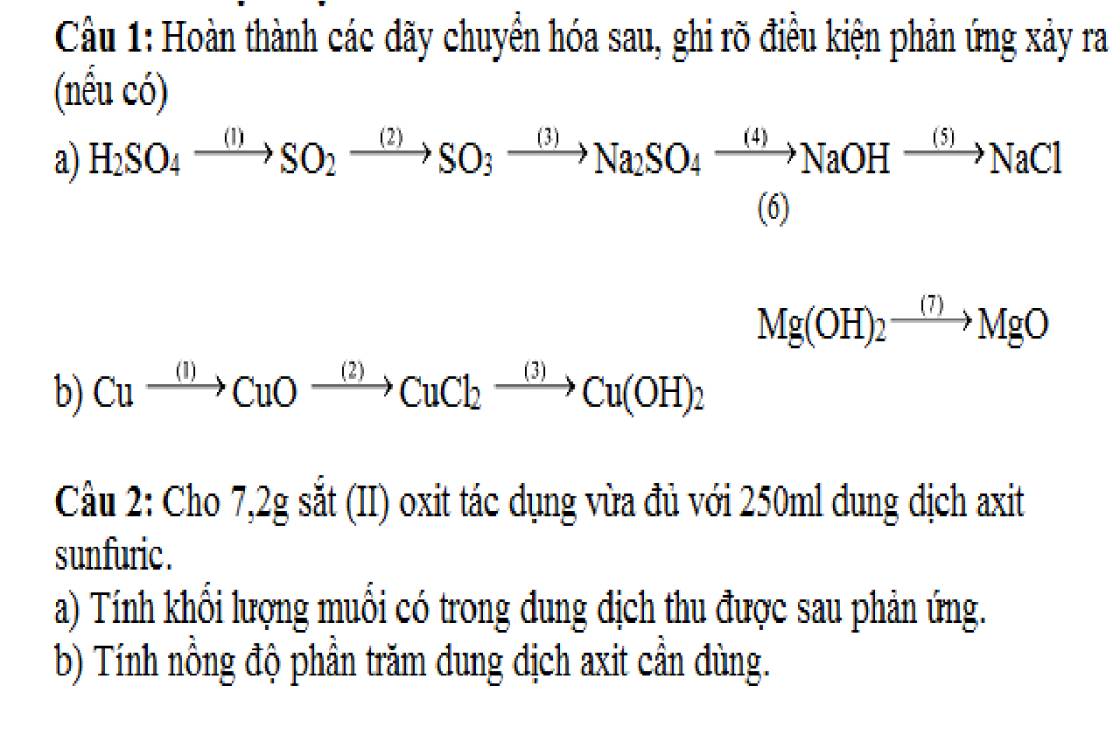
Câu 1:
a, (1) \(2H_2SO_{4\left(đ\right)}+Cu\underrightarrow{t^o}CuSO_4+SO_2+2H_2O\)
(2) \(SO_2+\dfrac{1}{2}O_2\underrightarrow{t^o}SO_3\)
(3) \(SO_3+Na_2O\rightarrow Na_2SO_4\)
(4) \(Na_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4+2NaOH\)
(5) \(NaOH+HCl\rightarrow NaCl+H_2O\)
(6) \(2NaOH+MgCl_2\rightarrow2NaCl+Mg\left(OH\right)_2\)
(7) \(Mg\left(OH\right)_2\underrightarrow{t^o}MgO+H_2O\)
b, (1) \(2Cu+O_2\underrightarrow{t^o}2CuO\)
(2) \(CuO+2HCl\rightarrow CuCl_2+H_2O\)
(3) \(CuCl_2+2NaOH\rightarrow Cu\left(OH\right)_2+2NaCl\)
Đúng 3
Bình luận (0)
Sửa đề: 250 ml → 250 gam
Câu 2:
a, \(n_{FeO}=\dfrac{7,2}{72}=0,1\left(mol\right)\)
PT: \(FeO+H_2SO_4\rightarrow FeSO_4+H_2O\)
Theo PT: \(n_{FeSO_4}=n_{FeO}=0,1\left(mol\right)\)
\(\Rightarrow m_{FeSO_4}=0,1.152=15,2\left(g\right)\)
b, \(n_{H_2SO_4}=n_{FeO}=0,1\left(mol\right)\)
\(\Rightarrow C\%_{H_2SO_4}=\dfrac{0,1.98}{250}.100\%=3,92\%\)
Đúng 3
Bình luận (0)
tai sao khi luộc rau muống, người ta thường cho muối vao?tai sao khi tưới nước tiểu đa pha loang vao cay thì cay lai trở nên tươi tốt ?bột nở la chat gì ma có thể lam cho banh to ra va xốp?giai thích có liên quan tới hoa học
Đọc tiếp
tai sao khi luộc rau muống, người ta thường cho muối vao?
tai sao khi tưới nước tiểu đa pha loang vao cay thì cay lai trở nên tươi tốt ?
bột nở la chat gì ma có thể lam cho banh to ra va xốp?
giai thích có liên quan tới hoa học
Cho 21,2 g dung dịch Na2CO3 tác dụng với dung dịch axit HCL sau phản ứng thu được khi thoát ra (điều kiện tiêu chuẩn ) a. Viết phương trình hóa học b. Tính khối lượng axit HCL cần dùng c. Tính thể tích khí thoát ra
a, \(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2+H_2O\)
b,\(n_{Na_2CO_3}=\dfrac{21,2}{106}=0,2\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{Na_2CO_3}=0,4\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
c, \(n_{CO_2}=n_{Na_2CO_3}=0,2\left(mol\right)\)
\(\Rightarrow V_{CO_2}=0,2.22,4=4,48\left(l\right)\)
Đúng 2
Bình luận (0)
F e SO 4 -->Fe(OH) 2 -> FeO -> Fe -> Fec*l_{2}
\(FeSO_4+2NaOH\rightarrow Fe\left(OH\right)_2+Na_2SO_4\)
\(Fe\left(OH\right)_2\underrightarrow{^{t^0}}FeO+H_2O\)
\(FeO+H_2\underrightarrow{^{t^o}}Fe+H_2O\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Đúng 3
Bình luận (0)
\(FeSO_4+2NaOH\rightarrow Fe\left(OH\right)_2+Na_2SO_4\\ Fe\left(OH\right)_2\xrightarrow[]{t^0}FeO+H_2O\\ FeO+H_2\xrightarrow[]{t^0}Fe+H_2O\\ Fe+2HCl\rightarrow FeCl_2+H_2\)
Đúng 1
Bình luận (0)
Câu 14: (1,5đ) Bằng phương pháp hoá học, hãy nhận biết mỗi lọ mất nhãn đựng một dung dịch sau: Ba(OH)2; K2SO4; NaCl. Viết PTHH xảy ra (nếu có). Giúp E với ạ😿
| \(Ba\left(OH\right)_2\) | \(K_2SO_4\) | \(NaCl\) | |
| Quỳ tím | Xanh | _ | _ |
| \(BaCl_2\) | _ | ↓trắng | _ |
\(BaCl_2+K_2SO_4\rightarrow BaSO_4+2KCl\)
Đúng 1
Bình luận (0)
hòa tan hoàn toàn 7.2g FeO vào dd H2SO4 20%.Viết pthh.Tính khối lượng dd H2SO4 đã dùng.Tính Kluong muối khan thu được
\(n_{FeO}=\dfrac{7,2}{72}=0,1\left(mol\right)\)
PTHH: \(FeO+H_2SO_4\rightarrow FeSO_4+H_2O\)
0,1----->0,1------>0,1
=> \(m_{H_2SO_4}=0,1.98=9,8\left(g\right)\Rightarrow m_{dd.H_2SO_4}=\dfrac{9,8.100}{20}=49\left(g\right)\)
\(m_{FeSO_4}=0,1.152=15,2\left(g\right)\)
Đúng 1
Bình luận (0)
Dẫn 3,7185 lít khí CO2 (Đkc) qua 150 ml dd nước vôi trong Ca(OH)2 phản ứng xảy ra là hoàn toàn có kết tủa trắng A a) Tính khối lượng kết tủa A b) Tíng nồng độ mol nước vôi trong
Mình trả lời ở câu hỏi này rồi bạn nhé.
Đúng 1
Bình luận (1)
neu phuong phap hoa hoc nhan biet cac chat sau
a ) hai chat ran mau trang na2o,mgo
b) hai khi co2,o2
c)hai dung dich ko mau naoh,nacl
d) cac dung dich nacl,na2so4,h2so4
- Trích một ít các chất làm mẫu thử
a)
- Hòa tan các chất rắn vào nước:
+ Chất rắn tan, tạo thành dung dịch trong suốt: Na2O
\(Na_2O+H_2O\rightarrow2NaOH\)
+ Chất rắn không tan: MgO
- Dán nhãn
b)
- Dẫn các chất khí qua dung dịch Ca(OH)2 dư:
+ Xuất hiện kết tủa trắng: CO2
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
+ Không hiện tượng: O2
- Dán nhãn
c)
- Cho các dung dịch tác dụng với giấy quỳ tím:
+ QT chuyển thành màu xanh: NaOH
+ QT không chuyển màu: NaCl
- Dán nhãn
d)
- Cho các dung dịch tác dụng với giấy quỳ tím:
+ QT chuyển thành màu đỏ: H2SO4
+ QT không chuyển màu: NaCl, Na2SO4 (1)
- Cho các dung dịch ở (1) tác dụng với dung dịch BaCl2
+ Không hiện tượng: NaCl
+ Xuất hiện kết tủa trắng: Na2SO4
\(Na_2SO_4+BaCl_2\rightarrow2NaCl+BaSO_4\downarrow\)
- Dán nhãn
Đúng 3
Bình luận (0)