
ko cần làm hết đâu làm câu nào bt thôi thanks!

ko cần làm hết đâu làm câu nào bt thôi thanks!
Câu 1:
a, Dẫn từng khí qua dd Ca(OH)2.
+ Xuất hiện kết tủa trắng: CO2
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
+ Không hiện tượng: C2H4 và CH4. (1)
- Dẫn khí nhóm (1) qua dd Brom dư.
+ Dd Brom nhạt màu dần: C2H4.
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
+ Không hiện tượng: CH4.
b, - Dẫn từng khí qua dd Ca(OH)2 dư.
+ Xuất hiện kết tủa trắng: SO2
PT: \(SO_2+Ca\left(OH\right)_2\rightarrow CaSO_{3\downarrow}+H_2O\)
+ Không hiện tượng: C2H2 và CO. (1)
- Dẫn khí nhóm (1) qua dd Brom dư.
+ Dd Brom nhạt màu dần: C2H2.
PT: \(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
+ Không hiện tượng: CO.
c, - Dẫn từng khí qua quỳ tím ẩm.
+ Quỳ tím hóa đỏ rồi mất màu: Cl2
PT: \(Cl_2+H_2O⇌HCl+HClO\)
+ Quỳ tím hóa đỏ: HCl
+ Quỳ tím hóa hồng: CO2
PT: \(CO_2+H_2O⇌H_2CO_3\)
+ Quỳ tím không đổi màu: CO2
Câu 2:
a, Dẫn hh khí qua dd Brom dư, C2H4 và C2H2 được giữ lại, ta thu được CH4.
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
b, - Dẫn hh khí qua dd Ca(OH)2 dư, CO2 bị giữ lại.
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
- Tiếp tục dẫn hh khí qua dd Brom dư, C2H4 bị giữ lại, khí thoát ra sau pư là CH4.
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
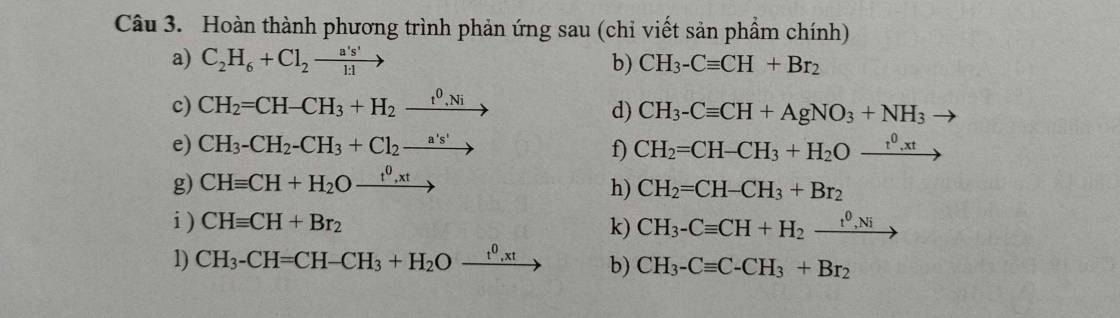 Giúp mình các phương trình này với
Giúp mình các phương trình này với
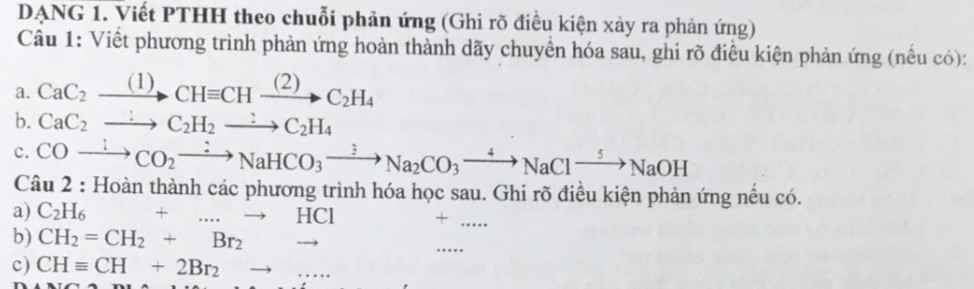 các bạn ko cần làm hết nha câu nào bt thôi thanks!
các bạn ko cần làm hết nha câu nào bt thôi thanks!
Câu 1:
a, (1) \(CaC_2+2H_2O\rightarrow Ca\left(OH\right)_2+C_2H_2\)
(2) \(C_2H_2+H_2\underrightarrow{t^o,Pd}C_2H_4\)
b, Phần này giống phần a nhé.
c, (1) \(CO+\dfrac{1}{2}O_2\underrightarrow{t^o}CO_2\)
(2) \(CO_2+NaOH\rightarrow NaHCO_3\)
(3) \(NaHCO_3+NaOH\rightarrow Na_2CO_3+H_2O\)
(4) \(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2+H_2O\)
(5) \(2NaCl+2H_2O\xrightarrow[cmn]{đpdd}2NaOH+Cl_2+H_2\)
Câu 2:
a, \(C_2H_6+Cl_2\underrightarrow{as}HCl+C_2H_5Cl\)
b, \(CH_2=CH_2+Br_2\rightarrow CH_2Br-CH_2Br\)
c, \(CH\equiv CH+2Br_2\rightarrow CHBr_2-CHBr_2\)
đốt cháy hoàn toàn canxi cần dùng vừa đủ 11,2l không khí (biết õi chiếm 20% thể tích không khí) a) tính khối lượng canxi tham gia phản ứng b) tính khối lượng canxi oxit tạo thành
Để giải bài toán này, ta cần sử dụng phương pháp phản ứng hóa học của quá trình đốt cháy canxi trong không khí:
2Ca + O2 -> 2CaO
Trong đó, 2 mol canxi kết hợp với 1 mol ôxi để tạo thành 2 mol canxi oxit. Xác định khối lượng canxi cần thiết dựa trên thể tích của không khí và sử dụng tỷ lệ mol giữa canxi và canxi oxit để tính toán khối lượng canxi tạo ra và khối lượng canxi oxit tạo thành.
a) Tính toán khối lượng canxi tham gia phản ứng:
Trước tiên, tính năng không thể tích không khí cần được sử dụng để đốt cháy canxi:
Thể tích không khí = 11,2 L ôxi * (1 - 20%) = 8,96 L khí
Lưu ý rằng ôxi chiếm 20% thể tích không khí, tức là có 80% khí là các thành phần khác trong không khí (ví dụ như N2).
Tiếp theo, ta tính số mol khí cần sử dụng để phản ứng theo áp dụng định luật Avogadro:
n(O2) = V(O2)/V(mol) = 8,96/22,4 = 0,4 mol
Do phương trình phản ứng cho biết 2 mol canxi cần phản ứng với 1 mol ôxi, vậy số mol canxi cần thiết là:
n(Ca) = 0,4/2 = 0,2 mol
Khối lượng canxi cần cho phản ứng là:
m(Ca) = n(Ca) * M(Ca) = 0,2 * 40 = 8 g
Vì vậy để đốt cháy hoàn toàn 8 g canxi cần sử dụng 11,2 L không khí (biết ôxi chiếm 20% thể tích).
b) Tính toán khối lượng canxi oxit tạo thành:
Để tính khối lượng canxi oxit tạo thành, ta sử dụng tỉ lệ mol của canxi oxit và canxi trong phương trình phản ứng:
n(CaO) = n(Ca) = 0,2 mol
Khối lượng canxi oxit tạo thành là:
m(CaO) = n(CaO) * M(CaO) = 0,2 * 56 = 11,2 g
Vì vậy khối lượng canxi oxit tạo thành là 11,2 g.
Ta có: \(V_{O_2}=11,2.20\%=2,24\left(l\right)\Rightarrow n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PT: \(2Ca+O_2\underrightarrow{t^o}2CaO\)
_____0,2___0,1____0,2 (mol)
a, \(m_{Ca}=0,2.40=8\left(g\right)\)
b, \(m_{CaO}=0,2.56=11,2\left(g\right)\)
đốt cháy 3,36 lít hỗn hợp gồm c 2 H 6 và c 3 h 4 cần dùng 61,6 lít không khí (biết VO2 chiếm 20% thể tích không khí) các khí ở đktc. a, tính tỷ lệ phần trăm thể tích mỗi khí b, hỗn hợp khí trên làm mất màu bao nhiêu gam dung dịch Brom 8%
a, \(V_{O_2}=61,6.20\%=12,32\left(l\right)\Rightarrow n_{O_2}=\dfrac{12,32}{22,4}=0,55\left(mol\right)\)
PT: \(2C_2H_6+7O_2\underrightarrow{t^o}4CO_2+6H_2O\)
\(C_3H_4+4O_2\underrightarrow{t^o}3CO_2+2H_2O\)
Ta có: \(n_{C_2H_6}+n_{C_3H_4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\left(1\right)\)
Theo PT: \(n_{O_2}=\dfrac{7}{2}n_{C_2H_6}+4n_{C_3H_4}=0,55\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{C_2H_6}=0,1\left(mol\right)\\n_{C_3H_4}=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_6}=\dfrac{0,1.22,4}{3,36}.100\%\approx66,67\%\\\%V_{C_3H_4}\approx33,33\%\end{matrix}\right.\)
b, \(C_3H_4+2Br_2\rightarrow C_3H_4Br_4\)
Ta có: \(n_{Br_2}=2n_{C_3H_4}=0,1\left(mol\right)\)
\(\Rightarrow m_{Br_2}=0,1.60=16\left(g\right)\Rightarrow m_{ddBr_2}=\dfrac{16}{8\%}=200\left(g\right)\)
a) Tính tỷ lệ phần trăm có thể phân bổ cho mỗi khí:
Ta có số mol khí của C2H6:
n(C2H6) = V(C2H6)/V(M)
n(C2H6) = 3,36/22,4 = 0,15 mol
Ta có số mol khí của C3H4:
n(C3H4) = V(C3H4)/V(M)
n(C3H4) = 3,36/22,4 = 0,15 mol
Do đó, Tỷ lệ phần trăm có thể tích cho mỗi khí là:
V(M) là khối lượng mol của hỗn hợp khí (đã được tính ở bước trước).
b) Giả sử dung dịch brom 8% là dung dịch brom trong nước có nhiệt độ 8% theo khối lượng. Dung dịch này có khả năng tác dụng với các hợp chất hữu cơ, trong đó có hidrocacbon không no và không.
Phản ứng của Br2 trong dung dịch brom với hidrocacbon không có dạng:
Br2 + C2H6 → 2 HBr + C2H4
Vì cân bằng nhiệt độ mol không khí đã biết rằng, Tỷ lệ phần trăm khối lượng của O2 trong không khí là 0, 20 * 32 g = 6,4 g.
Tính lượng brom cần để phản ứng với C2H4 trong 3,36 lít hỗn hợp:
n(C2H4) = n(C3H4) * (2 mol C2H4 / 3 mol C3H4) = 0,15 * (2/3) = 0,1 mol
Theo phương trình trên 1 mol C2H4 tác dụng với 1 mol Br2
Cần dùng n(Br2) = n(C2H4) = 0,1 mol brom trong phản ứng này.
Do đó, khối lượng brom cần sử dụng là m = n(Br2) * M(Br2) = 0,1 * 159,8 g/mol = 15,98 g brom
Do đó hỗn hợp khí trên làm mất màu 15,98 g dung dịch brom 8%.
Đốt cháy hoàn toàn 4,2g 1 HCHC X(Mx=42g/mol) thu đưỡ 13,2g Co2 và 54g H2O tìm CTPT của hợp chất X
nCO2=13.2/44=0.3(mol)-->nC=nCO2=0.3(mol)
nH2O=5,4/18=0.3(mol)--->nH=2nH2O=0.3x2=0.6(mol)
Hợp chất có thể có oxygen hoặc không
mC+mH=0.3x12+6x1=4.2g --> Hợp chất không có O
Gọi CTĐGN CxHy
x:y=0,3:0,6=1:2
---> CTĐGN (CH2)n=42-->n=42:14=3
CTPT là C3H6
dẫn 10,08l khí h2 vào một ống có chứa 48g fe2o3 và núng nóng tới nhiệt độ thích hợp. a) chất nào còn dư sau phản ứng? dư bao nhiêu gam? b) điều chế lượng hidro trên cần dùng bao nhiêu gam kẽm tác dụng với dung dịch axit clohidric
a)\(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(m\right)\)
\(n_{Fe_2O_3}=\dfrac{48}{160}=0,3\left(m\right)\)
\(PTHH:Fe_2O_3+3H_2\underrightarrow{ }2Fe+3H_2O\)
ta có tỉ lệ:\(\dfrac{0,45}{3}< \dfrac{0,3}{1}->H_2dư\)
H2 còn lại sau phản ứng
\(n_{H_2\left(dư\right)}=0,3-0,15=0,15\left(m\right)\)
\(m_{H_2\left(dư\right)}=0,15.2=0,3\left(g\right)\)
b)\(PTHH:Zn+2HCl\underrightarrow{ }ZnCl_2+H_2\)
tỉ lệ :1 2 1 1
số mol :0,15 0,3 0,15 0,15
\(m_{Zn}=0,15.65=9,75\left(g\right)\)
Cho 13g Zn tác dụng đủ vơi Axitclohiđric a)Tính thể tích khí thu được ở đktc b)Tính K2Hcl cần dùng c)Tính khối lượng muối thu được d) Lượng khí Hiđro trên khử được bao nhiêu gam đồng 2 oxit
Ta có: \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
____0,2_____0,4____0,2____0,2 (mol)
a, \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, \(m_{HCl}=0,4.36,5=14,6\left(g\right)\)
c, \(m_{ZnCl_2}=0,2.136=27,2\left(g\right)\)
d, \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
___0,2____0,2 (mol)
\(\Rightarrow m_{CuO}=0,2.80=16\left(g\right)\)
 Giúp mình câu 28
Giúp mình câu 28
Câu 28:
Ta có: \(n_{H_2O}=\dfrac{10,8}{18}=0,6\left(mol\right)\)
Gọi: nCO2 = x (mol)
m bình tăng = mCO2 + mH2O
⇒ 50,4 = 44x + 10,8 ⇒ x = 0,9 (mol)
Có: nX = 0,9 - 0,6 = 0,3 (mol)
⇒ nBr2 = 2nX = 0,6 (mol)
⇒ mBr2 = 0,6.160 = 96 (g)
Đáp án: C
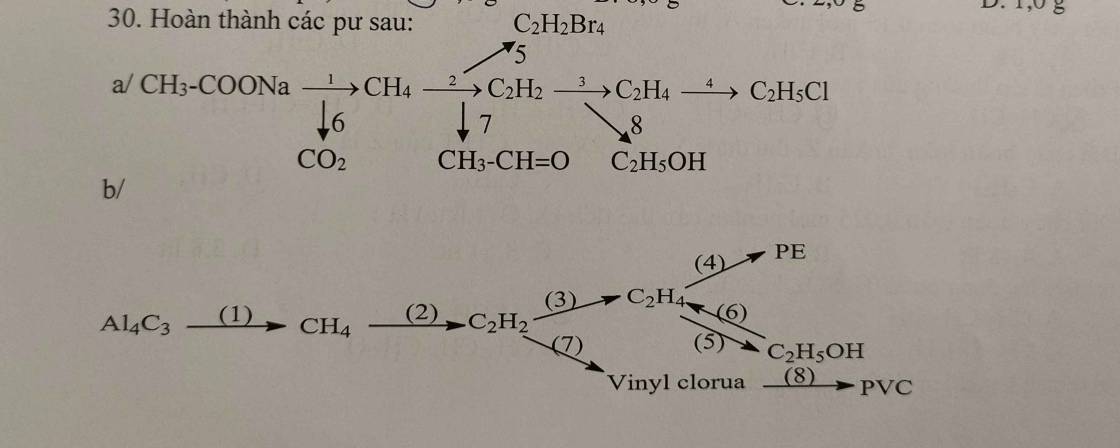 Giúp mình các phương trình này với
Giúp mình các phương trình này với
Mình đã trả lời ở câu hỏi này rồi bạn nhé.
https://hoc24.vn/cau-hoi/giup-minh-cac-phuong-trinh-nay-voi.7778830873437