Nêu Tính chất hoá học của NaHCO3, Viết PTHH mỗi tính chất
Hóa học
Tính chất hoá học của `NaHCO_3:`
`-` Tác dụng với dd axit:
`NaHCO_3 + HCl -> NaCl + CO_2 + H_2O`
`-` Tác dụng với dd bazơ (kiềm):
`NaHCO_3 + NaOH -> Na_2CO_3 + H_2O`
`2NaHCO_3 + Ba(OH)_2 -> BaCO_3 + Na_2CO_3 + 2H_2O`
`-` Bị nhiệt phân huỷ:
$2NaHCO_3 \xrightarrow{t^o} Na_2CO_3 + CO_2 + H_2O$
Đúng 2
Bình luận (0)
Chọn các chất thích hợp và hoàn thành các PTPƯ theo sơ đồ sau. Biết Y là một đơn chất. Trong hợp chất X, nguyên tố Y chiếm 63,64% về khối lượng, dung dịch A4 trong nước làm quỳ tím chuyển sang màu đỏ.
Đọc tiếp
Chọn các chất thích hợp và hoàn thành các PTPƯ theo sơ đồ sau. Biết Y là một đơn chất. Trong hợp chất X, nguyên tố Y chiếm 63,64% về khối lượng, dung dịch A4 trong nước làm quỳ tím chuyển sang màu đỏ.
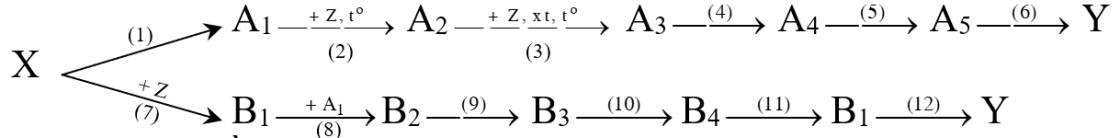
Cho a gam Fe hòa tan trong dung dịch HCl, cô cạn dung dịch sau phản ứng thì thu được 3,1 gam chất rắn. Nếu cho a gam Fe và b gam Mg cũng vào một lượng dung dịch HCl như trên,sau phản ứng thu được 0,2 mol H2 ,cô cạn phần dd thì thu được 3,34 gam chất rắn. Tính a,b?
Đọc tiếp
Cho a gam Fe hòa tan trong dung dịch HCl, cô cạn dung dịch sau phản ứng thì thu được 3,1 gam chất rắn. Nếu cho a gam Fe và b gam Mg cũng vào một lượng dung dịch HCl như trên,sau phản ứng thu được 0,2 mol H2 ,cô cạn phần dd thì thu được 3,34 gam chất rắn. Tính a,b?
hạt proton có đường kính bằng 4.10 mũ trừ 13 cm, có khối lượng bằng 1,6726.10 mũ trừ 24 gama. tính khối lượng riêng của proton, biết thể tích hình cầu có bán kính r được tính theo công thức v4/3nr mũ 3b. tính khối lượng riêng của nguyên tử oxi, biết bán kính của nguyên tử oxi bằng 0,73A (1A10 mũ trừ 10 cm), hạt nhân nguyên tử oxi gồm 8 proton và 8 noo7tron, electron có khối lượng vô cùng nhỏ
Đọc tiếp
hạt proton có đường kính bằng 4.10 mũ trừ 13 cm, có khối lượng bằng 1,6726.10 mũ trừ 24 gam
a. tính khối lượng riêng của proton, biết thể tích hình cầu có bán kính r được tính theo công thức v=4/3nr mũ 3
b. tính khối lượng riêng của nguyên tử oxi, biết bán kính của nguyên tử oxi bằng 0,73A (1A=10 mũ trừ 10 cm), hạt nhân nguyên tử oxi gồm 8 proton và 8 noo7tron, electron có khối lượng vô cùng nhỏ
trộn V1 lít CH4 với V2 lít C2H4 thu được hỗn hợp khí X có khối lượng riêng bằng khối lượng riêng của C2H2 (các thể tích khí đo ở điều kiện tiêu chuẩn).Tỉ lệ thể tích V1:V2 bằng
a. 1:3
b. 1:4
c. 1:5
d. 1:6
Ta có
`\overline(M)=(16V_1+28V_2)/(V_1+V_2)=26`
`=>10V_1=2V_2`
`=>V_1:V_2=2:10=1:5`
`->C`
Đúng 2
Bình luận (0)
trộn 2 khí O2 và CO2 theo tỉ lệ nào sau đây về thể tích để được hỗn hợp khí có tỉ khối so với không khí bằng 1,42?
a. 6:19
b. 6:38
c. 12:19
d. 12:38
em cần lời giải để ra đáp án ạ
`\overline(M)_(hh)=29.1,42=41,18`
Đặt `n_(O_2)=a;n_(CO_2)=b`
Ta có: `(32a+44b)/(a+b)=41,18`
`=>9,18a=2,82b`
`=>a/b=(2,82)/(9,18)=0,31`
Xét các đáp án ta thấy `A` là đáp án đúng nhất `(` Đáp án `D` cũng đúng vì `6:19=12:38)`
Đúng 3
Bình luận (0)
Bổ túc cân bằng, gọi tên các chất:left(Aright)xrightarrow[?]{1500^circ C}left(Bright)+left(Cright)left(Bright)+AgNO_3+NH_3xrightarrow[]{}left(Eright)+left(Dright)downarrowleft(Dright)+left(Fright)xrightarrow[]{}left(Bright)+left(Gright)downarrow2left(Bright)xrightarrow[?]{?}left(Hright)left(Hright)+left(Cright)xrightarrow[]{?}left(Iright)nleft(Iright)xrightarrow[?]{?}-left(Iright)_n-
Đọc tiếp
Bổ túc cân bằng, gọi tên các chất:
\(\left(A\right)\xrightarrow[?]{1500^\circ C}\left(B\right)+\left(C\right)\)
\(\left(B\right)+AgNO_3+NH_3\xrightarrow[]{}\left(E\right)+\left(D\right)\downarrow\)
\(\left(D\right)+\left(F\right)\xrightarrow[]{}\left(B\right)+\left(G\right)\downarrow\)
\(2\left(B\right)\xrightarrow[?]{?}\left(H\right)\)
\(\left(H\right)+\left(C\right)\xrightarrow[]{?}\left(I\right)\)
\(n\left(I\right)\xrightarrow[?]{?}-\left(I\right)_n-\)
\(2CH_4^{\left[A\right]}\xrightarrow[1500^{\circ}C]{lln}C_2H_2^{\left[B\right]}+2H_2^{\left[C\right]}\)
\(C_2H_2^{\left[B\right]}+2AgNO_3+2NH_3\xrightarrow[]{}2NH_4NO_3^{\left[E\right]}+C_2Ag_2^{\left[D\right]}\downarrow\)
\(C_2Ag_2^{\left[D\right]}+2HCl^{\left[F\right]}\xrightarrow[]{}C_2H_2^{\left[B\right]}+2AgCl^{\left[G\right]}\downarrow\)
\(2C_2H_2^{\left[B\right]}\xrightarrow[t^\circ]{NH_4Cl,CuCl}CH\equiv C-CH=CH_2^{\left[H\right]}\)
\(CH\equiv C-CH=CH_2^{\left[H\right]}+H_2^{\left[C\right]}\xrightarrow[t^\circ]{Pd\text{ / }PbCO_3}CH_2=CH-CH=CH_2^{\left[I\right]}\)
\(nCH_2=CH-CH=CH_2\xrightarrow[t^{\circ},p]{xt}\left(-CH_2-CH=CH-CH_2\right)_n^{\left[-\left(I\right)_n-\right]}\)
Gọi tên:
(A): Metan
(B): Axetylen
(C): Hiđro
(D): Bạc axetylua
(E): Amoni nitrat
(F): Axit clohiđric
(G): Bạc clorua
(H): Vinylaxetylen
(I): Buta-1,3-đien
-(I)n-: Cao su buna
Đúng 2
Bình luận (0)
\(A:CH_4;B:C_2H_2;C:H_2\\ D:C_2Ag_2;E:NH_4NO_3\\ F:HCl;G:AgCl\\H:C_4H_4;I:C_4H_6\\ 2CH_4-^{1500^0C,làm.lạnh.nhanh}->C_2H_2+3H_2\\ C_2H_2+2AgNO_3+2NH_3->C_2Ag_2+2NH_4NO_3\\ C_2Ag_2+2HCl->2AgCl+C_2H_2\\ 2C_2H_2-^{CuCl_2,NH_4Cl,100^0C}->H_2C=CH-C\equiv CH\\ H_2C=CH-C\equiv CH+H_2-^{Pd.PbCO_3,t^0}->H_2C=CH-CH=CH_2\\ H_2C=CH-CH=CH_2-^{t^0,p,xt}->-\left(H_2C-CH=CH-CH_2\right)-_n\)
Đúng 0
Bình luận (1)
.Hoà tan hoàn toàn 3,78gam một kim loại X bằng dung dịch HCl dư thu được4,704 lít khí hiđro (ở đktc). Xác định kim loại X.
\(2X+2nHCl->2XCl_n+nH_2\\n_{H_2}=\dfrac{4,704}{22,4}=\dfrac{3,78}{X}\cdot\dfrac{n}{2}\\ n:X=\dfrac{1}{9}\\ n=3;X=27\\ X:Al\left(aluminium:nhôm\right) \)
Đúng 1
Bình luận (0)
Cho 9 mol N2 và 6 mol H2 vào bình tổng hợp thu được khí NH3. Tính thànhphần % theo thể tích của các khí có trong hỗn hợp sau phản ứng và hiệu suất phản ứng. Biết rằng hỗn hợp sau phản ứng có tổng số mol là 14
\(N_2+3H_2\leftrightarrow2NH_3\\ n_{NH_3}=a\left(mol\right)\\ n_{sau}=14=9-\dfrac{1}{2}a+6-\dfrac{3}{2}a+a\\ a=1\\ n_{N_2}:1>n_{H_2}:3\\ H=\dfrac{1}{\dfrac{2}{3}.6}.100\%=25\%\)
Đúng 1
Bình luận (0)
Xác định khối lượng AgNO3 tách ra khi làm lạnh 2500 gam dung dịchAgNO3bão hòa ở 600C xuống 100C. Biết độ tan của AgNO3 ở 600C là 525 gam và 100C là 170 gam
\(C\%_{AgNO_3\left(60^0C\right)}=\dfrac{m_{AgNO_3\left(bđ\right)}}{2500}=\dfrac{525}{100+525}\\ m_{AgNO_3\left(bđ\right)}=2100\left(g\right)\\ C\%_{AgNO_3\left(10^0C\right)}=\dfrac{170}{270}=\dfrac{2100-m_{AgNO_3tách}}{2500-m_{AgNO_3tách}}\\ m_{AgNO_3tách}=1420\left(g\right)\)
Đúng 2
Bình luận (0)















