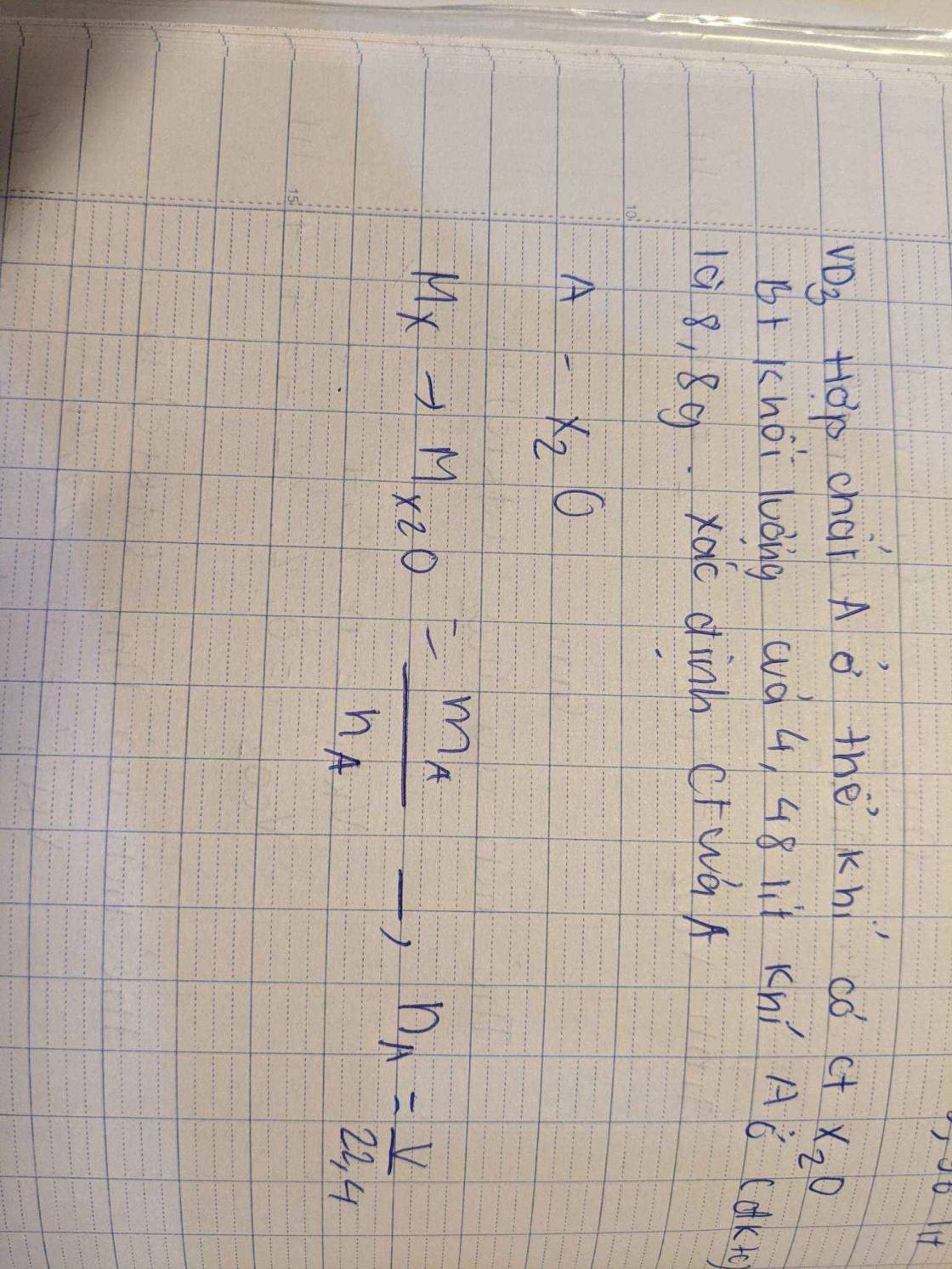Hóa học
a) \(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: K2CO3 + 2HCl ---> 2KCl + CO2 + H2O
0,6<---------------0,3
Ca(OH)2 + CO2 ---> CaCO3 + H2O
0,3------>0,3
=> m = 0,3.100 = 30 (g)
b) \(V_{ddHCl}=\dfrac{0,6}{1,5}=0,4\left(l\right)=400\left(ml\right)\)
Đúng 2
Bình luận (1)
Bài 11:
1) \(n_{hh}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{CO_2}=a\left(mol\right)\\n_{SO_2}=b\left(mol\right)\end{matrix}\right.\)
=> a + b = 0,15 (1)
PTHH:
Ca(OH)2 + CO2 ---> CaCO3 + H2O
a---------->a
Ca(OH)2 + SO2 ---> CaSO3 + H2O
b--------->b
=> 100a + 120b = 17 (2)
Từ (1), (2) => a = 0,05; b = 0,1
=> \(\left\{{}\begin{matrix}\%V_{CO_2}=\dfrac{0,05}{0,15}.100\%=33,33\%\\\%V_{SO_2}=100\%-33,33\%=66,67\%\end{matrix}\right.\)
2) \(n_{HCl}=0,1.3=0,3\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{CuO}=a\left(mol\right)\\n_{ZnO}=b\left(mol\right)\end{matrix}\right.\)
=> 80a + 81b = 21 (1)
PTHH:
CuO + 2HCl ---> CuCl2 + H2O
a------>2a
ZnO + 2HCl ---> ZnCl2 + H2O
b------>2b
=> 2a + 2b = 0,3 (2)
Từ (1), (2) => a = -8,85; b = 9 (Đề sai à mà ra nghiệm âm?)
Đúng 2
Bình luận (0)
Mình cần gấp ạ 😭 Cho 5,6 gam dung dịch KOH tác dụng với 200 gam dung dịch Cu(NO) 18,8%. sau khi phản ứng kết thúc thu được dung dịch A và chất rắn B. Nung chất rắn B đến khối lượng không đổi thu được chất rắn C. a. Tính nồng độ % các chất trong dung dịch A b. Tính khối lượng rắn C thu được sau khi nung.
\(n_{KOH}=\dfrac{5,6}{56}=0,1\left(mol\right)\) ; \(n_{Cu\left(NO_3\right)_2}=\dfrac{200.18,8\%}{188}=0,2\left(mol\right)\)
\(2KOH+Cu\left(NO_3\right)_2\rightarrow Cu\left(OH\right)_2\downarrow+2KNO_3\)
0,1 < 0,2 ( mol )
0,1 0,05 0,05 0,1 ( mol )
\(m_{ddspư}=5,6+200-0,05.98=200,7\left(g\right)\)
\(\left\{{}\begin{matrix}C\%_{KNO_3}=\dfrac{0,1.101}{200,7}.100=5,03\%\\C\%_{Cu\left(NO_3\right)_2}=\dfrac{\left(0,2-0,05\right).188}{200,7}.100=14,05\%\end{matrix}\right.\)
\(Cu\left(OH\right)_2\rightarrow\left(t^o\right)CuO+H_2O\)
0,05 0,05 ( mol )
\(m_{CuO}=0,05.80=4\left(g\right)\)
Đúng 2
Bình luận (1)
\(n_{X_2O}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\Rightarrow M_{X_2O}=\dfrac{8,8}{0,2}=44\left(g/mol\right)\)
=> 2MX + 16 = 44
=> MX = 14 (g/mol)
Vậy CTHH của chất là N2O
Đúng 0
Bình luận (0)
Giúp ê với ạ
Hãy tính;
a) Số mol của 28g Fe; 9,8g H2SO4;1,2,1023phân tử H2; 4,48 lít CO2(đktc)
b)Thể tích của hỗn hợp khí (đktc)gồm 5,6g N2; 6,4g SO2;1,8.1023phân tử CO
giúp em vs ạ em đang cần gấp ![]()
a) \(\left\{{}\begin{matrix}n_{Fe}=\dfrac{m}{M}=\dfrac{28}{56}=0,5\left(mol\right)\\n_{H_2SO_4}=\dfrac{m}{M}=\dfrac{9,8}{98}=0,1\left(mol\right)\\n_{H_2}=\dfrac{\text{Số phân tử}}{6.10^{23}}=\dfrac{1,2.10^{23}}{6.10^{23}}=0,2\left(mol\right)\\n_{CO_2}=\dfrac{V_{\left(đktc\right)}}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\end{matrix}\right.\)
b) \(\left\{{}\begin{matrix}n_{N_2}=\dfrac{m}{M}=\dfrac{5,6}{28}=0,2\left(mol\right)\\n_{SO_2}=\dfrac{m}{M}=\dfrac{6,4}{64}=0,1\left(mol\right)\\n_{CO}=\dfrac{\text{Số phân tử}}{6.10^{23}}=\dfrac{1,8.10^{23}}{6.10^{23}}=0,3\left(mol\right)\end{matrix}\right.\)
`=> n_{hh} = n_{N_2} + n_{SO_2} + n_{CO} = 0,2 + 0,1 + 0,3 = 0,6 (mol)`
`=> V_{hh} = n.22,4 = 0,6.22,4 = 13,44 (l)`
Đúng 0
Bình luận (1)
Bài 4. Để hòa tan 4 gam oxit của một kim loại hóa trị II cần phải dùng 250 ml dung dịch H2SO4
0,4M.
a) Tìm công thức hóa học của oxit
b) Tính nồng độ mol của dung dịch muối thu được
Trên 2 đĩa cân để 2 cốc đựng dung dịch HCl và H2SO4 cân ở vị trí thăng bằng
Cho vào cốc đựng dung dịch HCl 25gam CaCO3
Cho vào cốc đựng dung dịch H2SO4 a gam Al .sau phản ứng cân ở vị trí cân bằng . tính a biết phản ứng hóa học này xảy ra hoàn toàn theo phương trình
CaCO3+2 HCL-> CaCL2 + H2O + CO2 và
2 AL+ 3H2SO4 -> AL2(SO4)3 +3H2
- Cốc đựng HCl: \(n_{CaCO_3}=\dfrac{25}{100}=0,25\left(mol\right)\)
PTHH: CaCO3 + 2HCl ---> CaCl2 + CO2 + H2O
0,25--------------------------->0,25
=> mtăng = 0,25.100 - 0,25.44 = 14 (g)
- Cốc đựng H2SO4: \(n_{Al}=\dfrac{a}{27}\left(mol\right)\)
PTHH: 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
\(\dfrac{a}{27}\)--------------------------------->\(\dfrac{a}{18}\)
=> \(m_{tăng}=a-2.\dfrac{a}{18}=\dfrac{8a}{9}\left(g\right)\)
Do sau phản ứng trở về thăng bằng
=> mtăng như nhau
=> \(\dfrac{8a}{9}=14\Leftrightarrow a=15,75\left(g\right)\)
Đúng 1
Bình luận (0)