Chia 7,72 gam hỗn hợp X gồm Fe và hai oxit kim loại MO, R2O3 thành hai phần bằng nhau. Dùng một lượng vừa đủ dung dịch H2SO4 loãng hòa tan hoàn toàn phần 1, thu được khí B và dung dịch D chứa 9,7 gam muối. Dẫn toàn bộ lượng khí B sinh ra qua ống đựng 1,6 gam CuO nung nóng, đến khi thu được 1,408 gam chất rắn thì đã có 80% lượng khí B tham gia phản ứng. Mặt khác, dẫn dòng khí CO dư qua phần 2 nugn nóng, sau khi phản ứng xảy ra hoàn toàn thu được 3,46 gam chất rắn. Biết rằng nguyên tử khối của M gấp 2,37 lần nguyên tử khối của R. Cho các phản ứng được thực hiện trong điều kiện không có không khí. Xác định 2 kim loại M, R và tính % khối lượng các chất trong hỗn hợp X.
m rắn giảm = mO (oxit) => nO (oxit) = (1,6 – 1,408) : 16 = 0,012mol
Dễ thấy n = nO (oxit) = 0,012mol
=> nH2 ban đầu = 0,012 : 80% = 0,015
=> nFe = nH2= 0,015 → x = 0,015
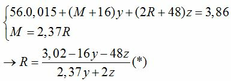
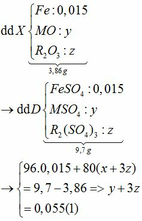
Ta có: CO + O(Oxit) → CO2
Vì: m(Rắn giảm) = mO(Oxit) → nO(Oxit) = (3,86 – 3,46) : 16 = 0,025
TH1: cả 2 oxit đều bị khử bởi CO
→ nO(Oxit) = y + 3z = 0,025 kết hợp với (1) loại
TH2: chỉ có MO bị khử bởi CO
→ nO(Oxit) = nMO = 0,025 → y = 0,025 kết hợp với (1) => z = 0,01
Kết hợp với (*) => M = 64 (Cu)
TH3: chỉ có R2O3 bị khử bởi CO
→ nO(Oxit) = 3.nR2O3 → z = 0,025/3 kết hợp với (1) => y = 0,03
Kết hợp với (*) y => M lẻ => loại
Vậy %m các chất trong X là: 21,76%; 51,81%; 26,43%




