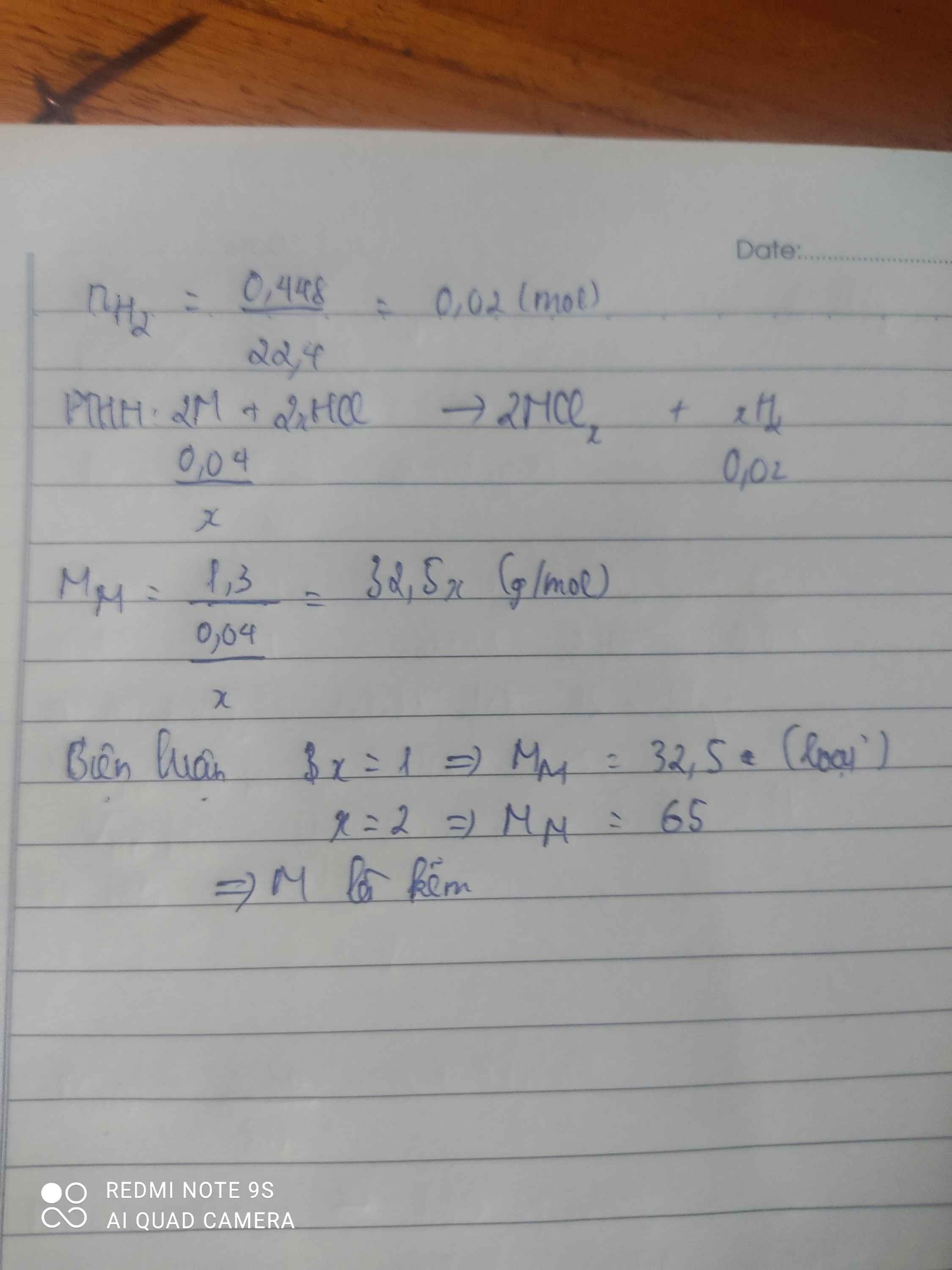đặt M hóa trị 1
2M+2HCl-to>2MCl+H2
0,04----------------------0,02 mol
n H2=\(\dfrac{0,448}{22,4}\)=0,02 mol
=> 0,04=\(\dfrac{1,3}{M_M}\)
=>MM=32,5 đvC
n 1 2 3
M 32,5 (L) 65 97,5 (L)
=> vậy M là kẽm (Zn), hóa trị 2
\(n_{H_2}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\\ Đặt:x:hoá.trị.M\left(x:nguyên,dương\right)\\ 2M+2xHCl\rightarrow2MCl_x+xH_2\\ n_M=\dfrac{2.0,02}{x}=\dfrac{0,04}{x}\left(mol\right)\\ \Rightarrow M_M=\dfrac{1,3}{\dfrac{0,04}{x}}=32,5x\left(\dfrac{g}{mol}\right)\)
Xét x=1;x=2;x=3;x=8/3 thấy x=2 thoả khi đó MM=65(g/mol)
=>M cần tìm là kẽm (Zn-65)