Các câu hỏi tương tự
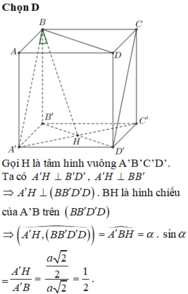
Cho hình lập phương ABCD.A’B’C’D’ có cạnh bằng a, gọi
α
là góc giữa đường thẳng AB’ và mặt phẳng (BB’D’D) Tính sin
α
Đọc tiếp
Cho hình lập phương ABCD.A’B’C’D’ có cạnh bằng a, gọi α là góc giữa đường thẳng AB’ và mặt phẳng (BB’D’D) Tính sin α
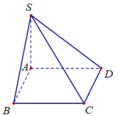
Cho hình chóp S.ABCD có đáy là hình vuông cạnh a. SA vuông góc với mặt phẳng (ABCD) và
S
A
a
6
(hình vẽ). Gọi α là góc giữa đường thẳng SB và mặt phẳng (SAC). Tính sin α ta được kết quả là A.
1
14
B.
2
2
C.
3
2
D.
1
5...
Đọc tiếp
Cho hình chóp S.ABCD có đáy là hình vuông cạnh a. SA vuông góc với mặt phẳng (ABCD) và S A = a 6 (hình vẽ). Gọi α là góc giữa đường thẳng SB và mặt phẳng (SAC). Tính sin α ta được kết quả là
A. 1 14
B. 2 2
C. 3 2
D. 1 5
Cho hình lập phương ABCD.A′B′C′D′ có độ dài cạnh bằng 3. Một mặt phẳng (α) đồng thời cắt các cạnh AA′,BB′,CC′,DD′ lần lượt tại các điểm M,N,P,Q. Diện tích tứ giác MNPQ bằng 18. Góc giữa (α) và mặt phẳng đáy bằng
Đọc tiếp
Cho hình lập phương ABCD.A′B′C′D′ có độ dài cạnh bằng 3. Một mặt phẳng (α) đồng thời cắt các cạnh AA′,BB′,CC′,DD′ lần lượt tại các điểm M,N,P,Q. Diện tích tứ giác MNPQ bằng 18. Góc giữa (α) và mặt phẳng đáy bằng
![]()
![]()
![]()
![]()
Cho hình chóp S.ABCD có đáy ABCD là hình vuông tâm O cạnh a, SA vuông góc với đáy (ABCD) Góc giữa đường thẳng SC và mặt phẳng (SAB) bằng
α
với Tính góc giữa đường thẳng SO và mặt phẳng (ABCD) A.
60
o
B.
69
,
3
o
C.
90
o
D.
45
o
Đọc tiếp
Cho hình chóp S.ABCD có đáy ABCD là hình vuông tâm O cạnh a, SA vuông góc với đáy (ABCD) Góc giữa đường thẳng SC và mặt phẳng (SAB) bằng
α
với 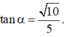 Tính góc giữa đường thẳng SO và mặt phẳng (ABCD)
Tính góc giữa đường thẳng SO và mặt phẳng (ABCD)
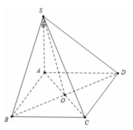
A. 60 o
B. 69 , 3 o
C. 90 o
D. 45 o
Cho hình chóp S.ABCD có đáy ABCD là hình vuông cạnh a. Cạnh bên SA vuông góc với mặt phẳng đáy, khối chóp S.ABCD có thể tích bằng
a
3
2
3
. Gọi α là góc giữa hai mặt phẳng (SAD) và (SBD). Tính cos α. A.
cos
α
3
5
B.
cos
α
6
3...
Đọc tiếp
Cho hình chóp S.ABCD có đáy ABCD là hình vuông cạnh a. Cạnh bên SA vuông góc với mặt phẳng đáy, khối chóp S.ABCD có thể tích bằng a 3 2 3 . Gọi α là góc giữa hai mặt phẳng (SAD) và (SBD). Tính cos α.
A. cos α = 3 5
B. cos α = 6 3
C. cos α = 2 2 5
D. cos α = 10 5
Hình chóp S.ABCD có đáy là hình thang vuông ABCD vuông tại A và D, có AB 2a, AD DC a, có cạnh SA vuông góc với mặt phẳng (ABCD) và SA a.a) Chứng minh mặt phẳng (SAD) vuông góc với mặt phẳng (SDC), mặt phẳng (SAC) vuông góc với mặt phẳng (SCB).b) Gọi φ là góc giữa hai mặt phẳng (SBC) và (ABCD), tính tanφ.c) Gọi (α) là mặt phẳng chứa SD và vuông góc với mặt phẳng (SAC). Hãy xác định (α) và xác định thiết diện của hình chóp S.ABCD với (α)
Đọc tiếp
Hình chóp S.ABCD có đáy là hình thang vuông ABCD vuông tại A và D, có AB = 2a, AD = DC = a, có cạnh SA vuông góc với mặt phẳng (ABCD) và SA = a.
a) Chứng minh mặt phẳng (SAD) vuông góc với mặt phẳng (SDC), mặt phẳng (SAC) vuông góc với mặt phẳng (SCB).
b) Gọi φ là góc giữa hai mặt phẳng (SBC) và (ABCD), tính tanφ.
c) Gọi (α) là mặt phẳng chứa SD và vuông góc với mặt phẳng (SAC). Hãy xác định (α) và xác định thiết diện của hình chóp S.ABCD với (α)
Cho hình chóp S.ABCD có đáy là hình vuông cạnh a,
S
A
⊥
A
B
C
D
và
S
A
a
3
. Gọi α là góc tạo bởi giữa đường thẳng SB và mặt phẳng (SAC), khi đó α thỏa mãn hệ thức nào sau đây A.
cos
α
2
8
B.
sin
α...
Đọc tiếp
Cho hình chóp S.ABCD có đáy là hình vuông cạnh a, S A ⊥ A B C D và S A = a 3 . Gọi α là góc tạo bởi giữa đường thẳng SB và mặt phẳng (SAC), khi đó α thỏa mãn hệ thức nào sau đây
A. cos α = 2 8
B. sin α = 2 8
C. sin α = 2 4
D. cos α = 2 4
Cho hình lập phương ABCD.A’B’C’D’ cạnh a.
a) Chứng minh rằng đường thẳng AC’ vuông góc với mặt phẳng (A’BD) và mặt phẳng (ACC’A’) vuông góc với mặt phẳng (A’BD).
b) Tính đường chéo AC’ của hình lập phương đã cho.
Cho hình lập phương ABCD.ABCD. Gọi
α
là góc giữa đường thẳng AC’ với mặt phẳng (ABCd). Mệnh đề nào dưới đây đúng?
A
.
2
π
9
≤
α
≤
π
4
B
.
π
4
α
π
3...
Đọc tiếp
Cho hình lập phương ABCD.A'B'C'D'. Gọi α là góc giữa đường thẳng AC’ với mặt phẳng (ABCd). Mệnh đề nào dưới đây đúng?
A . 2 π 9 ≤ α ≤ π 4
B . π 4 < α < π 3
C . π 6 < α < 2 π 9
D . π 9 ≤ α ≤ π 6