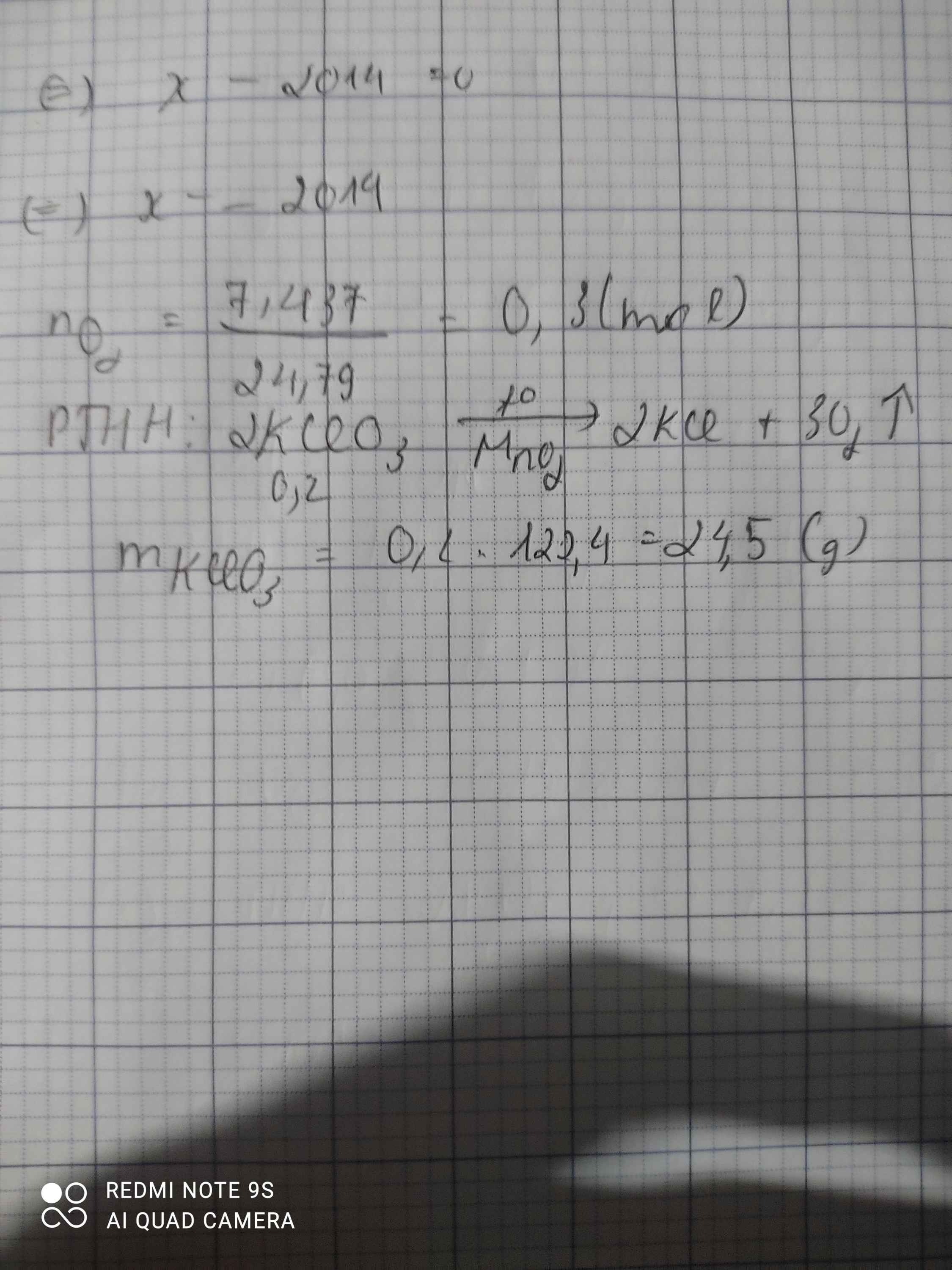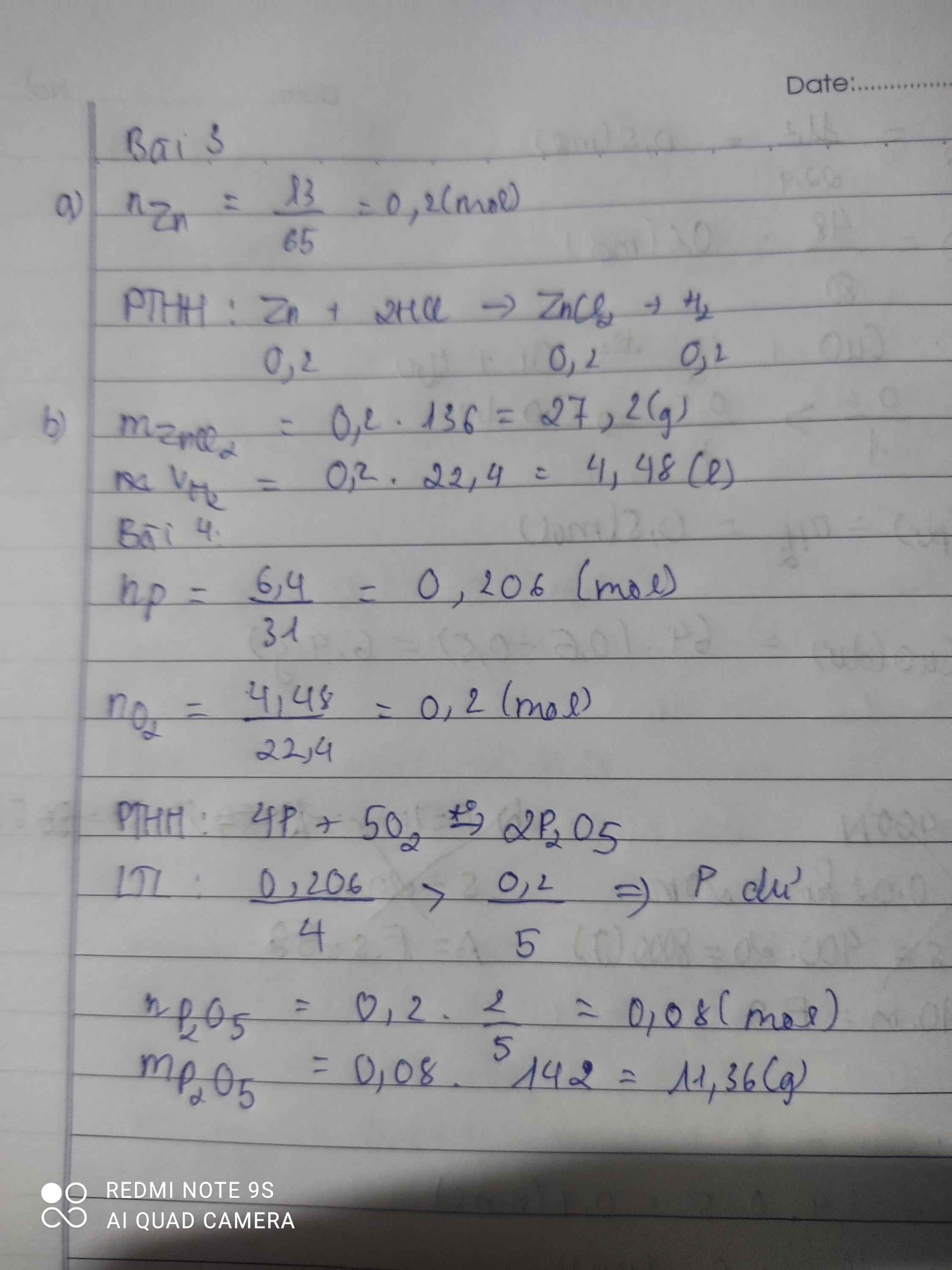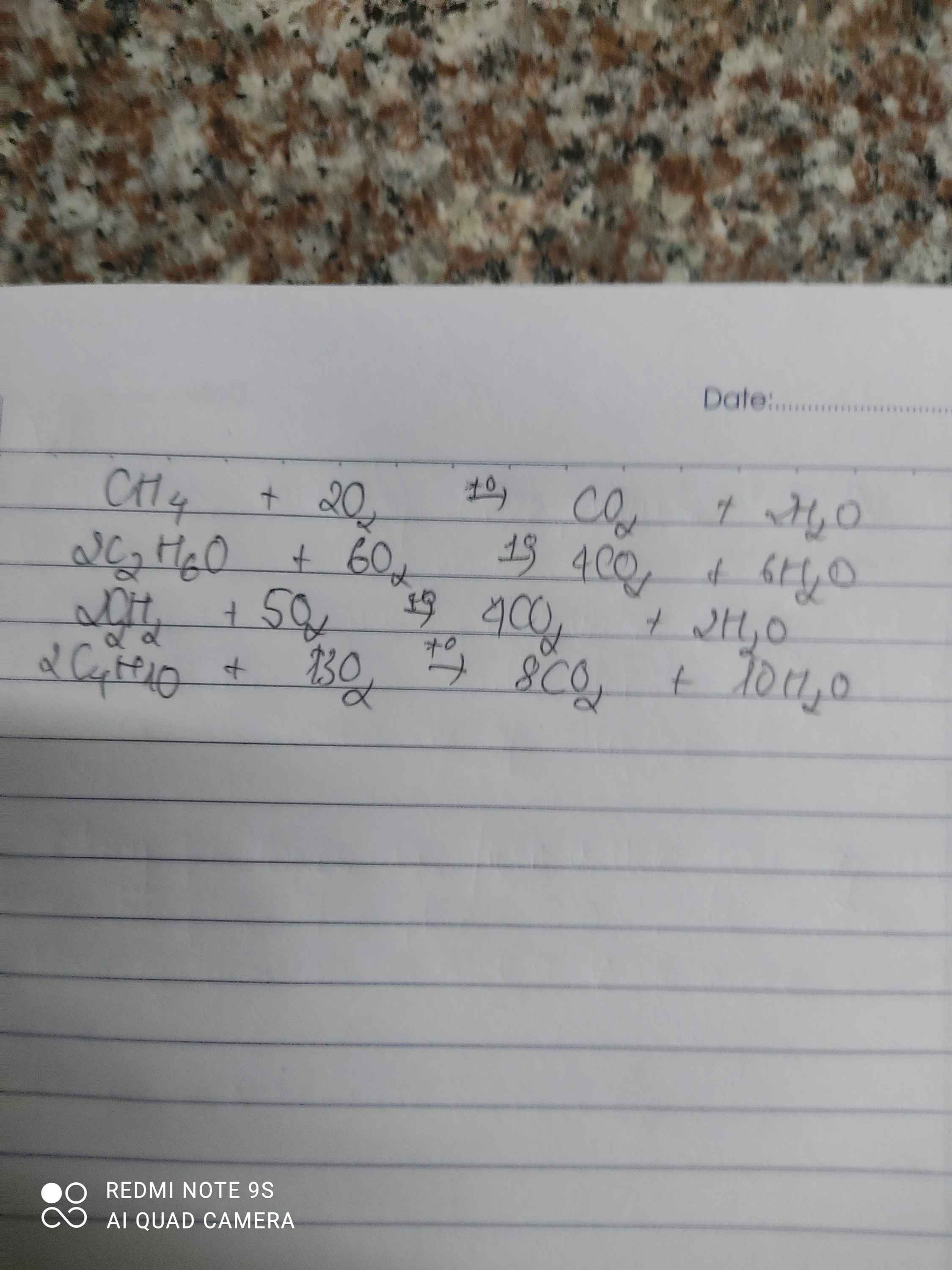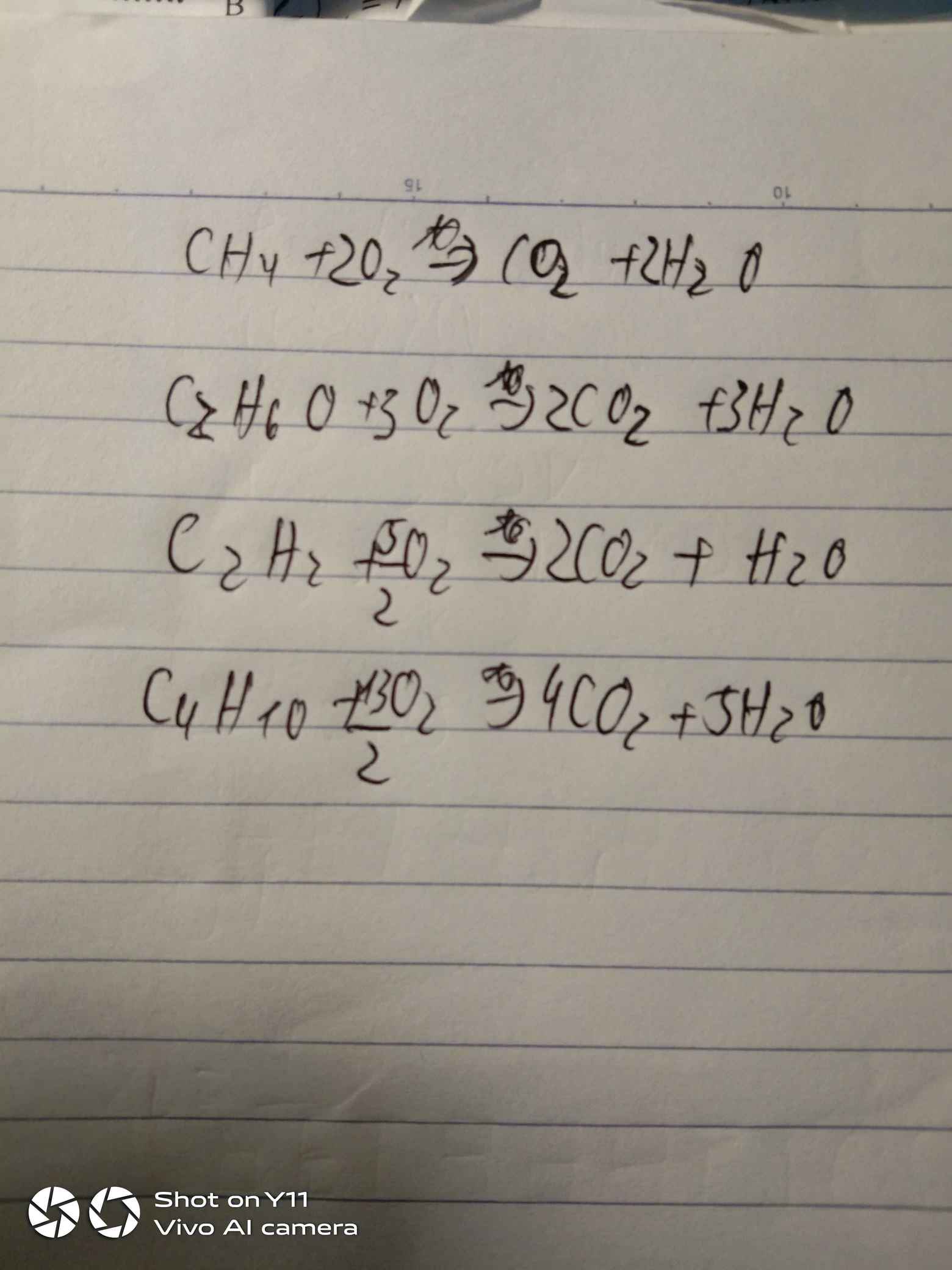Người ta nhiệt phân m gam KClO3,thu được KCl và 7,437 lít khí Oxygen O2 ở đkt . Tính giá trị của m (hay m của KClO3 ) cần dùng. Giúp mình với ạ ! 🥺
CHƯƠNG IV: OXI - KHÔNG KHÍ
Ủa em, anh đã tính chia cho 24,79 rồi cho đến khi thấy đkt
vậy là đề cho điều kiện thường đúng không em?
Đúng 2
Bình luận (0)
4. Khi đốt cháy sắt trong oxi ở nhiệt độ cao thu được oxit sắt từ Fe3O4. a) Tính khối lượng sắt và thể tích khí oxi (đktc) cần dùng để điều chế được 6,96 gam Fe3O4 . b) Tính khối lượng kali clorat KClO3 cần dùng để điều chế được lượng oxi dùng cho phản ứng trên.
a. \(n_{Fe_3O_4}=\dfrac{6,96}{232}=0,03\left(mol\right)\)
PTHH : 3Fe + 2O2 -to-> Fe3O4
0,09 0,06 0,03
\(m_{Fe}=0,09.56=5,04\left(g\right)\)
\(V_{O_2}=0,06.22,4=1,344\left(l\right)\)
b. PTHH : 2KCl + 3O2 -> 2KClO3
0,06 0,04
\(m_{KClO_3}=0,04.122,5=4,9\left(g\right)\)
Đúng 2
Bình luận (0)
4
n Fe3O4=\(\dfrac{6,96}{232}=0,03mol\)
3Fe+2O2-to>Fe3O4
0,09---0,06-----0,03 mol
=>m Fe=0,09.56=5,04g
=>VO2=0,06.22,4=1,344l
b)
2KClO3-to>2KCl+3O2
0,04----------------------0,06 mol
=>m KClO3=0,04.122,5=4,9g
Đúng 0
Bình luận (1)
\(n_{Fe_3O_4}=\dfrac{6,96}{232}=0,03\left(mol\right)\\ 3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\\ n_{Fe}=3.0,03=0,09\left(mol\right);n_{O_2}=0,03.2=0,06\left(mol\right)\\ a,\Rightarrow m_{Fe}=0,09.56=5,04\left(g\right);V_{O_2\left(đktc\right)}=0,06.22,4=1,344\left(l\right)\\ 2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\uparrow\\ n_{KClO_3}=\dfrac{2}{3}.n_{O_2}=\dfrac{2.0,06}{3}=0,04\left(mol\right)\\ \Rightarrow b,m_{KClO_3}=122,5.0,04=4,9\left(g\right)\)
Đúng 0
Bình luận (1)
Xem thêm câu trả lời
Giúp mình vs ah 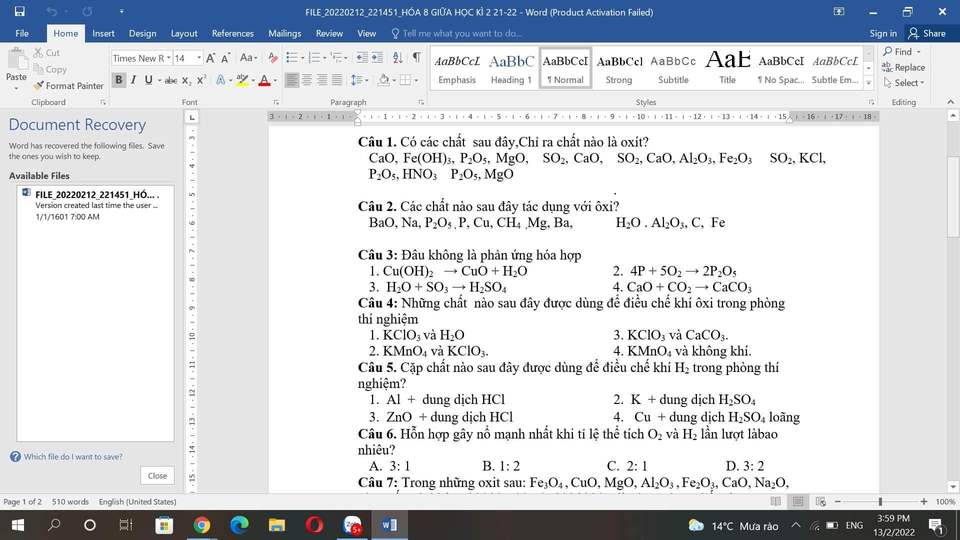
Anh nhớ em đăng 1 lần nhưng câu 1 câu 2 anh chả thấy có đánh số để chọn
Anh nhắm theo mắt anh nhé
Câu 1: Chọn nhóm SO2, CaO, Al2O3, Fe2O3
Câu 2: Na, P, Cu, CH4, Mg, Fe, C, Ba
Câu 3: 1
Câu 4: 2
Câu 5: 1
Câu 6: B
Đúng 1
Bình luận (0)
Giúp mik bài 4 nhanh vs ạk, cảm ơn ae nhìu😁
4P+5O2-to>2P2O5
0,2-------0,08 mol
n P=\(\dfrac{6,4}{31}\)=\(\dfrac{32}{155}\) mol
n O2=\(\dfrac{4,48}{22,4}=0,2mol\)
=>P dư
m P dư =\(\dfrac{9}{775}\).31=0,36g
=>m P2O5= 0,08.142=11,36g
Đúng 1
Bình luận (0)
Khí CH4 , C2H6O ( rượu hoặc cồn ) , C2H2 và C4H10 khi cháy trong oxi đều tạo thành khí cacbonic và hơi nước . Hãy viết phương trình hoá học của các phản ứng đốt cháy từng chất đó
Phân tử X có công thức là M2O là 140, trong phân tử X thì tổng số hạt mang điện nhiều hơn số hạt không mang điện là 44. Vậy X là nguyên tố nào?
Có \(\left\{{}\begin{matrix}4.p_M+2n_M+2p_O+n_O=140\\4.p_M+2p_O-2n_M-n_O=44\end{matrix}\right.\)
=> \(2p_M+p_O=46\)
=> 2.pM + 8 = 46
=> pM = 19
Vậy M là K
Đúng 2
Bình luận (0)
Nguyên tố oxi có số proton , electron , notron là bao nhiêu?
Số proton = số electron = 8
Số notron = 6
Đúng 2
Bình luận (3)
Số p = số e = 8
Tùy từng đồng vị thì có số n khác nhau :v
Đúng 2
Bình luận (0)
Xem thêm câu trả lời
1) \(2Al+3Cl_2\underrightarrow{t^o}2AlCl_3\)
2) \(2FeO+C\underrightarrow{t^o}2Fe+CO_2\)
3) \(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
4) \(CaCO_3\underrightarrow{t^o}CaO+CO_2\)
5) \(S+O_2\underrightarrow{t^o}SO_2\)
6) \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
- Pư hóa hợp: 1, 3, 5, 6
Đúng 2
Bình luận (0)