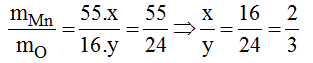Một hỗn hợp gồm có khí etilen, CO2 và hơi nước. Trình bày phương pháp thu được khí etilen tinh khiết
Bài 26: Oxit
- Dẫn hỗn hợp khí qua dung dịch \(Ca\left(OH\right)_2\)dư thì \(CO_2\) bị giữ lại
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_2+H_2O\) - Dẫn hỗn hợp khí còn lại qua dung dịch \(H_2SO_4\) đặc dư, hơi nước bị giữ lại thu được etilen tinh khiết .
Đúng 0
Bình luận (1)
Bước 1 : Dẫn hỗn hợp khí trên qua dung dịch nước vôi trong(dư) thì khí CO2 bị hấp thụ
PTHH: CO2 + Ca(OH)2 ===> CaCO3 + H2O
Bước 2: Dẫn hỗn hợp khí còn lại qua dung dịch H2SO4(đặc) thì hơi nước sẽ bị hấp thụ
=> Còn lại etilen tinh khiết
Đúng 0
Bình luận (0)
Cho khí hidro tác dụng với 3g một loại oxit sắt cho2,1 g Fe. Tìm công thức phân tử của oxit sắt
gọi hóa trị của Fe là x
Ta có PTHH:
xH2 + Fe2Ox \(\rightarrow\) xH2O + 2Fe
có : nFe = m/M = 2.1/56 =0.0375 (mol)
theo PT => nFe2Ox = 1/2 nFe = 1/2 x 0.0375=0.01875(mol)
=> MFe2Ox = m/n = 3/0.01875 =160(g)
hay 2.56+x.16=160
=> x=3
=> CTHH của oxit sắt là Fe2O3
Đúng 0
Bình luận (0)
bảo toàn khối lượng tính được m O2 bị khử
m O2= m oxit - m kim loại
tính ra n O2 ; n Fe
chia n O2 cho n Fe được tỉ lệ
Đúng 0
Bình luận (0)
0,25 mol sắt oxit chứa 7,5.10^23 nguyên tử sắt và oxit. Hãy tìm công thức sắt oxit.
Gọi CTHH của oxit sắt là FexOy
Có 0,25 mol sắt oxít chứa 7,5 . 10^23 nguyên tử sắt và oxít.
=> 1 mol sắt oxit chứa: (7,5 . 10^23)/0,25 = 30. 10^23 (nguyên tử)
Có 1 mol sắt và oxít chứa 6.10^23 nguyên tử
=> Số nguyên tử của 1mol oxit sắt là: 6. 10^23. ( x + y) = 30 . 10^23
=> x + y = 5
Mà oxi hóa trị II => x + y = 2 + y = 5 => y=3
Vậy CTHH của oxit sắt là Fe2O3.
Đúng 0
Bình luận (0)
Một Hiđroxit khối lượng mol phân tử là 78g.Tìm tên kim loại trong Hiđroxit đó
gọi CT là R(OH)x
ta có R + 17x = 78
thay x=1,2,3 vào ta thấy x=3 => R=27 =>Al
=> Al(OH)3
Đúng 0
Bình luận (1)
một oxit tạo thành bởi mangan và oxi trong đó tỉ lệ khối lượng giữa mangan và oxi là 55:24 hãy xác định công thức phân tử của oxit
ct tổng quát: MnxOy
\(\frac{m_{Mn}}{m_{O2}}\)= \(\frac{55x}{32y}\)= \(\frac{55}{24}\)
=> \(\frac{x}{y}\)= \(\frac{4}{3}\)
=> cthh : Mn4O3
Đúng 0
Bình luận (0)
Gọi công thức tổng quát của oxit: Mn2Oy
Theo đề bài ta có:
Vậy công thức phân tử của oxit là Mn2O3.
Đúng 0
Bình luận (0)
Một oxit kim loại A (ccchua có hóa trị) có tỉ lệ khối lượng Oxi=3/4A. Tìm công thức của oxit kim loại
Ai có thể cho mình biết làm cách nao để biết axit tương ứng với oxit axit không mình cảm ơn
bạn dựa vào hóa trị của phi kim trong axit có bằng hóa trị của phi kim đó trong oxit axit không
cái này thầy mình dạy đó![]()
bạn có thể hỏi giáo viên của bạn mà
Đúng 0
Bình luận (0)
Đốt 5,4 (g) Al trong bình chứa 6,72 (l) khí Oxi ( ở đktc ) thu được x (g) Al2O3.
a) Tính giá trị của x
b) Cũng lượng nhân liệu trên hòa tan hết vào dung dịch Axit Clohidric. Sau phản ứng thu được Nhôm Clorua ( AlCl3 ) và khí Hidro. Tính khí Hidro ( ở đktc )
a) PTHH: 4Al + 3O2 -> 2Al2O3
Ta có:
\(n_{Al}=\frac{5,4}{54}=0,1\left(mol\right)\\ n_{O_2}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(\frac{0,1}{4}=0,25< \frac{0,3}{3}=0,1\)
=> Al hết, O2 dư, tính theo nAl
=>\(n_{Al\left(phảnứng\right)}=\frac{4.n_{O_2}}{3}=\frac{4.0,3}{3}=0,4\left(mol\right)\)
\(n_{Al\left(dư\right)}=n_{Al\left(banđầu\right)}-n_{Al\left(phảnứng\right)}=0,1-0,4=-0,3\left(mol\right)\left(vôlí,vìsốmolkhôngbaogiờâm\right)\)
Đúng 0
Bình luận (3)
4Al + 3O2 \(\rightarrow\) 2Al2O3
0,2 0,15 0,1 (mol)
a,
n0\(_2\)= \(\frac{V}{22,4}\)= \(\frac{6,72}{22,4}\)= 0,3 mol
nAl\(_{ }\)= \(\frac{m}{M}\)= \(\frac{5,4}{27}\)=0,2 mol
So sánh :
0,3 > 0,2 \(\Rightarrow\) O2 dư tính theo Al
mAl\(_2\)O\(_3\)= n x M = 0,1 x 102 = 10,2 g
b,
2Al + 6HCl = 2AlCl3 + 3H2
0,2 0,6 0,2 0,3 (mol)
V\(_{ }\)H\(_2\)= n x 22,4 = 0,3 x 22,4 = 6,72 l
\(\)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Đốt 5,4 (g) Nhôm trong bình chứa thu được 6,72 (l) khí Oxi và x (g) Al2O3.
a. Tính giá trị của x
b. Cũng lượng nhôm trên hòa tan hết vào dung dịch HCl. Sau phản ứng thu được Nhôm Clorua (AlCl3 ) và khí Hidro. Tính khí Hidro (ở dktc)?
PTHH: 4Al + 3O2 -to-> 2Al2O3
Ta có:
\(n_{Al}=\frac{5,4}{27}=0,2\left(mol\right)\\ n_{O_2}=\frac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(\frac{n_{Al\left(đềbài\right)}}{n_{Al\left(PTHH\right)}}=\frac{0,2}{4}=0,05< \frac{n_{O_2\left(đềbài\right)}}{n_{O_2\left(PTHH\right)}}=\frac{0,3}{3}=0,1\)
=> Al phản ứng hết, O2 dư nên tính theo nAl.
Theo PTHH và đề bài, ta có:
\(n_{Al_2O_3}=\frac{2.n_{Al}}{4}=\frac{2.0,2}{4}=0,1\left(mol\right)\)
Khối lượng Al2O3 thu được:
\(x=m_{Al_2O_3}=0,1.102=10,2\left(g\right)\)
b) PTHH: 2Al + 6HCl -> 2AlCl3 + 3H2
Theo câu a lượng Al trên là 0,2 mol.
Theo PTHH và đề bài, ta có:
\(n_{H_2}=\frac{3.n_{Al}}{2}=\frac{3.0,2}{2}=0,3\left(mol\right)\)
Thể tích khí H2 thu được (ở đktc):
\(V_{H_2\left(đktc\right)}=0,3.22,4=6,72\left(l\right)\)
Đúng 0
Bình luận (0)
Bài 1:
a, Lập CTHH một loại oxit của photpho, biết rằng hóa trị của photpho là V
b, Lập CTHH của crom(III) oxit
Bài 2:
a, Hãy viết CTHH của hai oxit axit và hai oxit bazơ
b, Nhận xét về các thành phần trong công thức của các oxit đó
c, Chỉ ra cách gọi tên mỗi oxit đó
Bài 3: Cho các oxit có công thức hóa học như sau:
a, SO3 b, N2O5 c, CO2
d, Fe2O3 e, CuO f, CaO
Bài 3: Một số CTHH được viết như sau:
Na2O, NaO, CaCO3, Ca...
Đọc tiếp
Bài 1:
a, Lập CTHH một loại oxit của photpho, biết rằng hóa trị của photpho là V
b, Lập CTHH của crom(III) oxit
Bài 2:
a, Hãy viết CTHH của hai oxit axit và hai oxit bazơ
b, Nhận xét về các thành phần trong công thức của các oxit đó
c, Chỉ ra cách gọi tên mỗi oxit đó
Bài 3: Cho các oxit có công thức hóa học như sau:
a, SO3 b, N2O5 c, CO2
d, Fe2O3 e, CuO f, CaO
Bài 3: Một số CTHH được viết như sau:
Na2O, NaO, CaCO3, Ca(OH)2, HCl, CaO, Ca2O, FeO
Hãy chỉ ra những công thức hóa học viết sai
Bài 4:
Na2O viết đúng vì Na(I) và O(II),
NaO viết sai vì Na (I) và O(II)=> CTHH đúng là Na2O
CaCO3 viết đúng vì Ca(II) và nhóm CO3 (II).
Ca(OH)2 viết đúng Ca(II) và nhóm OH(I)
HCl viết đúng vì H(I) và Cl(I)
CaO viết đúng vì Ca(II) và O(II)
Ca2O viết sai vì Ca(II) và O(II)=> CTHH đúng là CaO
FeO viết đúng vì Fe(II) và O(II)
Đúng 0
Bình luận (0)
Bài 1 :
a/ P2O5 ( điphotpho pentaoxit )
b/ Cr2O3
Bài 2 :
a/ Oxit axit : SO3; CO2
Oxit bazơ : Na2O; CaO
b/ Oxit axit và oxit bazơ đều do 2 nguyên tố tạo thành và trong đó có một nguyên tố là oxi
c/ SO3 : lưu huỳnh trioxit
CO2 : cacbon đioxit
Na2O : natri oxit
CaO : canxi oxit
Bài 3 : oxit axit oxit bazơ
- SO3 - Fe2O3
- N2O5 - CuO
- CO2 - CaO
Bài 4 : CTHH viết sai :
NaO sửa lại Na2O
Ca2O sửa lại CaO
tút nhóa !!!!
Đúng 0
Bình luận (0)
Bài 1:
a) Gọi công thức dạng chung của oxit cần tìm là \(P_x^VO^{II}_y\)
Theo quy tắc hóa trị, ta có:
\(x.V=y.II\\ =>\frac{x}{y}=\frac{II}{V}=\frac{2}{5}\\ =>x=2;y=5\)
Vậy: CTHH của oxit cần tìm là P2O5 (điphotpho pentaoxit).
Đúng 0
Bình luận (0)
Xem thêm câu trả lời