Các câu hỏi tương tự
Một bình điện phân chứa dung dịch AgN
O
3
với anôt bằng bạc. Khối lượng bạc bám vào catôt của bình điện phân sau 16 phút 5 giây là 6,48 g. Biết bạc có khối lượng mol là A 108 g/mol và hóa trị n 1. Lấy số Fa – ra – đây F 96500 C/mol. Cường độ dòng điện chạy qua bình điện phân là A. 5 A. B. 6 A. C. 0,5 A. D. 4 A.
Đọc tiếp
Một bình điện phân chứa dung dịch AgN O 3 với anôt bằng bạc. Khối lượng bạc bám vào catôt của bình điện phân sau 16 phút 5 giây là 6,48 g. Biết bạc có khối lượng mol là A = 108 g/mol và hóa trị n = 1. Lấy số Fa – ra – đây F = 96500 C/mol. Cường độ dòng điện chạy qua bình điện phân là
A. 5 A.
B. 6 A.
C. 0,5 A.
D. 4 A.
Một bình điện phân chứa dung dịch AgN
O
3
với anôt bằng bạc. Khối lượng bạc bám vào catôt của bình điện phân sau 16 phút 5 giây là 6,48 g. Biết bạc có khối lượng mol là A 108 g/mol và hóa trị n 1. Lấy số Fa – ra – đây F 96500 C/mol. Cường độ dòng điện chạy qua bình điện phân là A. 5 A. B. 6 A. C. 0,5 A. D. 4 A.
Đọc tiếp
Một bình điện phân chứa dung dịch AgN O 3 với anôt bằng bạc. Khối lượng bạc bám vào catôt của bình điện phân sau 16 phút 5 giây là 6,48 g. Biết bạc có khối lượng mol là A = 108 g/mol và hóa trị n = 1. Lấy số Fa – ra – đây F = 96500 C/mol. Cường độ dòng điện chạy qua bình điện phân là
A. 5 A.
B. 6 A.
C. 0,5 A.
D. 4 A.
Một bình điện phân đựng dung dịch
AgNO
3
, cường độ dòng điện chạy qua bình điện phân là I 1A. Cho
A
A
g
108
đvc,
n
A
g
1
. Lượng Ag bám vào catốt trong thời gian 16 phút 5 giây là A. 1,08 mg B. 1,08g C. 0,54g D. 1,08kg
Đọc tiếp
Một bình điện phân đựng dung dịch AgNO 3 , cường độ dòng điện chạy qua bình điện phân là I = 1A. Cho A A g = 108 đvc, n A g = 1 . Lượng Ag bám vào catốt trong thời gian 16 phút 5 giây là
A. 1,08 mg
B. 1,08g
C. 0,54g
D. 1,08kg
Một bình điện phân đựng dung dịch
A
g
N
O
3
, cường độ dòng điện chạy qua bình điện phân là I 1 A ; Cho
A
A
g
108 đvc,
n
A
g
1. Lượng Ag bám vào catốt trong thời gian 16 phút 5 giây là A. 1,09 g B. 1,08 Kg. C. 0,54 g D. 1,08 mg
Đọc tiếp
Một bình điện phân đựng dung dịch A g N O 3 , cường độ dòng điện chạy qua bình điện phân là I = 1 A ; Cho A A g = 108 đvc, n A g = 1. Lượng Ag bám vào catốt trong thời gian 16 phút 5 giây là
A. 1,09 g
B. 1,08 Kg.
C. 0,54 g
D. 1,08 mg
Cho mạch điện như hình vẽ nguồn điện có suất điện động
ξ
12V , điện trở trong
1
Ω
,
R
2
12
Ω
là bình điện phân đựng dung dịch
A
g
N
O
3
với điện cực Anôt là bạc,
R
1
3
Ω
,
R
3...
Đọc tiếp
Cho mạch điện như hình vẽ nguồn điện có suất điện động ξ =12V , điện trở trong 1 Ω , R 2 = 12 Ω là bình điện phân đựng dung dịch A g N O 3 với điện cực Anôt là bạc, R 1 = 3 Ω , R 3 = 6 Ω . Cho Ag có A=108g/mol, n = 1. Khối lượng Ag bám vào catot sau 16 phút 5 giây là
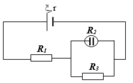
A. 0,54g
B. 0,72g
C. 0,81g.
D. 0,27g.
Một bình điện phân chứa dung dịch bạc nitrat (AgNO3) có điện trở 2,5 Ω. Anôt của bình điện phân bằng bạc và hiệu điện thế đặt vào hai điện cực của bình đ Một bình điện phân chứa dung dịch bạc nitrat (AgNO3) có điện trở 2,5 Ω. Anôt của bình iện phân là 10 V. Biết bạc có A 108 g/mol, có n 1, hằng số Faraday F 96500 C/mol. Khối lượng bạc bám vào catôt của bình điện phân sau 16 phút 5 giây là A. 2,14 mg. B. 4,32 mg. C. 4,32 g. D. 2,16 g.
Đọc tiếp
Một bình điện phân chứa dung dịch bạc nitrat (AgNO3) có điện trở 2,5 Ω. Anôt của bình điện phân bằng bạc và hiệu điện thế đặt vào hai điện cực của bình đ Một bình điện phân chứa dung dịch bạc nitrat (AgNO3) có điện trở 2,5 Ω. Anôt của bình iện phân là 10 V. Biết bạc có A = 108 g/mol, có n = 1, hằng số Faraday F = 96500 C/mol. Khối lượng bạc bám vào catôt của bình điện phân sau 16 phút 5 giây là
A. 2,14 mg.
B. 4,32 mg.
C. 4,32 g.
D. 2,16 g.
Cho mạch điện như hình vẽ nguồn điện có suất điện động
ξ
12
V
, điện trở trong
1
Ω
,
R
2
12
Ω
là bình điện phân cực dung dịch
AgNO
3
với điện cực anot là bạc,
R
1
3
Ω
, ...
Đọc tiếp
Cho mạch điện như hình vẽ nguồn điện có suất điện động ξ = 12 V , điện trở trong 1 Ω , R 2 = 12 Ω là bình điện phân cực dung dịch AgNO 3 với điện cực anot là bạc, R 1 = 3 Ω , R 2 = 6 Ω .Cho Ag có A = 108g/mol, n = 1. Khối lượng Ag bám vào Catot sau 16 phút 5 giây là
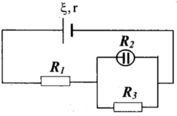
A. 0,54g
B. 0,72g
C. 0,81g
D. 0,27g
Điện phân dung dịch muối của một kim loại với anốt là kim loại đó trong 32 phút 10 giây thì thu được 2,16g kim loại đó bám vào catốt. Biết cường độ dòng điện qua bình điện phân là 1A và kim loại có hóa trị I, kim loại này là A. Al. B. Cu. C. Fe D. Ag.
Đọc tiếp
Điện phân dung dịch muối của một kim loại với anốt là kim loại đó trong 32 phút 10 giây thì thu được 2,16g kim loại đó bám vào catốt. Biết cường độ dòng điện qua bình điện phân là 1A và kim loại có hóa trị I, kim loại này là
A. Al.
B. Cu.
C. Fe
D. Ag.
Để xác định đương lượng điện hóa của đồng một học sinh đã cho dòng điện có cường độ 1,2 A chạy qua bình điện phân chứa dung dịch đồng sunphat (CuSO4) trong khoảng thời gian 5 phút và thu được 120 mg đồng bám vào catot. Lấy số Faraday F 96500 C/mol, khối lượng mol nguyên tử của đồng là A 63,5 g/mol và hóa trị n 2 thì sai số tỉ đối của kết quả thí nghiệm do học sinh này thực hiện so với kết quả tính toán theo định luật II Faraday là A. 1,3 % B. 1,2 % C. 2,2 % D. 2,3 %
Đọc tiếp
Để xác định đương lượng điện hóa của đồng một học sinh đã cho dòng điện có cường độ 1,2 A chạy qua bình điện phân chứa dung dịch đồng sunphat (CuSO4) trong khoảng thời gian 5 phút và thu được 120 mg đồng bám vào catot. Lấy số Faraday F= 96500 C/mol, khối lượng mol nguyên tử của đồng là A = 63,5 g/mol và hóa trị n = 2 thì sai số tỉ đối của kết quả thí nghiệm do học sinh này thực hiện so với kết quả tính toán theo định luật II Faraday là
A. 1,3 %
B. 1,2 %
C. 2,2 %
D. 2,3 %




