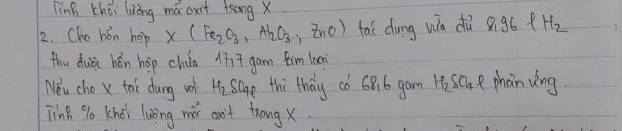chỉ có fe2o3 td bị khử bởi h2 trog X thôi, mà sau pứ thu được Hỗn Hợp chứa 17,7 gam Kim Loại là sao;-;
kim loại thì sau pứ chỉ có Fe à bạn
Gọi: \(\left\{{}\begin{matrix}n_{Fe_2O_3}=x\left(mol\right)\\n_{Al_2O_3}=y\left(mol\right)\\n_{ZnO}=z\left(mol\right)\end{matrix}\right.\)
- Cho hh pư với H2.
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
\(ZnO+H_2\underrightarrow{t^o}Zn+H_2O\)
Theo PT: \(n_{H_2}=3n_{Fe_2O_3}+n_{ZnO}=3x+z=\dfrac{8,96}{22,4}=0,4\left(mol\right)\left(1\right)\)
\(\left\{{}\begin{matrix}n_{Fe}=2n_{Fe_2O_3}=2x\left(mol\right)\\n_{Zn}=n_{ZnO}=z\left(mol\right)\end{matrix}\right.\) ⇒ 56.2x + 65z = 17,7 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\z=0,1\left(mol\right)\end{matrix}\right.\)
- Cho hh pư với H2SO4.
PT: \(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
\(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
\(ZnO+H_2SO_4\rightarrow ZnSO_4+H_2O\)
Theo PT: \(n_{H_2SO_4}=3n_{Fe_2O_3}+3n_{Al_2O_3}+n_{ZnO}=\dfrac{68,6}{98}=0,7\left(mol\right)\)
\(\Rightarrow n_{Al_2O_3}=\dfrac{0,7-0,1.3-0,1}{3}=0,1\left(mol\right)\)
⇒ mX = 0,1.160 + 0,1.102 + 0,1.81 = 34,3 (g)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe_2O_3}=\dfrac{0,1.160}{34,3}.100\%\approx46,65\%\\\%m_{Al_2O_3}=\dfrac{0,1.102}{34,3}.100\%\approx29,74\%\\\%m_{ZnO}\approx23,61\%\end{matrix}\right.\)