Cho 18,6 gam P tác dụng với 16 gam oxi. Vậy khối lượng P2O5 thu được là:( tính chi tiết giúp mình với ạ 🥺 )
CHƯƠNG III: MOL VÀ TÍNH TOÁN HÓA HỌC
\(n_P=\dfrac{18,6}{31}=0,6\left(mol\right)\\
n_{O_2}=\dfrac{16}{32}=0,5\left(mol\right)\\
pthh:4P+5O_2\underrightarrow{t^o}2P_2O_5\)
\(LTL:\dfrac{0,6}{4}>\dfrac{0,5}{5}\)
=> P dư
\(n_{P_2O_5}=\dfrac{2}{5}n_{O_2}=0,2\left(mol\right)\\
m_{P_2O_5}=0,2.142=28,4g\)
Đúng 1
Bình luận (0)
Phân hủy hoàn toàn 36, 75 gam Kali clorat
a, tính thể tích khí oxi sinh ra (ở đktc )
b, dùng lượng khí Oxi sinh ra để oxi hóa hoàn toàn một lượng nhôm vừa đủ nhiệt độ cao. Tính khối lượng nhôm tham gia phản ứng. Tính khối lượng sản phẩm thu được
`KClO_3` $\xrightarrow{t^o}$ `KCl + 3 / 2 O_2`
`0,3` `0,15` `(mol)`
`n_[KClO_3]=[36,75]/[122,5]=0,3(mol)`
`a)V_[O_2]=0,15.22,4=10,08(l)`
`b)`
`3O_2 + 4Al` $\xrightarrow{t^o}$ `2Al_2 O_3`
`0,15` `0,2` `0,1` `(mol)`
`@ m_[Al]=0,2.27=5,4(g)`
`@ m_[Al_2 O_3]=0,1.102=10,2(g)`
Đúng 1
Bình luận (0)
cho Zn tác dụng vừa đủ với dung dịch HCl. Sau phản ứng thu được 2.479 lít khí H Đốt cháy hết lượng khí hydrogen sinh ra thì cần bao nhiêu thể tích khí oxygen (đkc)
\(n_{H_2}=\dfrac{2,479}{24,79}=0,1mol\)
\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\)
0,1 0,05 ( mol )
\(V_{O_2}=0,05.24,79=1,2395l\)
Đúng 7
Bình luận (0)
Câu 5: a) Nồng độ phần trăm của dung dịch là gì?Tính nồng độ phần trăm của dung dịch KCl biết rằng trong 600g dung dịch có 20 g KClb) Hòa tan 1,5 mol CuSO4 vào nước thu được 750 ml dung dịch.Tính nồng độ mol của dung dịch CuSO4 Câu 6: a) Nồng độ phần trăm của dung dịch là gì?Tính nồng độ phần trăm của dung dịch NaCl biết rằng trong 200g dung dịch có 30 g NaCl. b) Hòa tan 1 mol FeSO4 vào nước thu được 200 ml dung dịch.Tính nồng độ mol của dung dịch FeSO4
Đọc tiếp
Câu 5:
a) Nồng độ phần trăm của dung dịch là gì?Tính nồng độ phần trăm của dung dịch KCl biết rằng trong 600g dung dịch có 20 g KCl
b) Hòa tan 1,5 mol CuSO4 vào nước thu được 750 ml dung dịch.Tính nồng độ mol của dung dịch CuSO4
Câu 6:
a) Nồng độ phần trăm của dung dịch là gì?Tính nồng độ phần trăm của dung dịch NaCl biết rằng trong 200g dung dịch có 30 g NaCl.
b) Hòa tan 1 mol FeSO4 vào nước thu được 200 ml dung dịch.Tính nồng độ mol của dung dịch FeSO4
5 Nồng độ phần trăm là gì? Trong hóa học, nồng độ phần trăm của dung dịch được kí hiệu là C% cho ta biết số gam chất tan có trong 100 gam dung dịch là bao nhiêu
C%=\(\dfrac{20}{620}.100=3,22\%\)
CM=\(\dfrac{1,5}{0,75}\)=2M
6 ko giải thích lại
C%=\(\dfrac{30}{230}100=13\%\)
CM=\(\dfrac{1}{0,2}\)=5M
Đúng 3
Bình luận (0)
Một tinh thể ngậm nước X có công thức M2(SO4)3.nH2O (với M là kim loại chưa biết, n là số tự nhiên). Trong X, % khối lượng của lưu huỳnh là 16,55%; % khối lượng của oxi là 60,69%. Tìm CTHH của X.
Có: \(\dfrac{\%S}{\%O}=\dfrac{16,55\%}{60,69\%}\)
=> \(\dfrac{m_S}{m_O}=\dfrac{1655}{6069}\Rightarrow\dfrac{32.3}{16.\left(12+n\right)}=\dfrac{1655}{6069}\)
=> n = 10
X có CTHH là M2(SO4)3.10H2O
Có: \(\%S=\dfrac{32.3}{2.M_M+468}.100\%=16,55\%\)
=> MM = 56 (g/mol)
=> M là Fe
CTHH: Fe2(SO4)3.10H2O
Đúng 2
Bình luận (0)
Giúp mk vs ạ, mk cảm ơn trc.
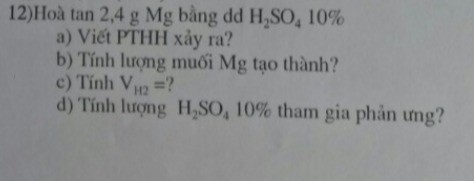
Mg+H2SO4->MgSO4+H2
0,1----0,1------0,1---------0,1
n Mg=0,1 mol
=>m MgSO4=0,1.120=12g
=>VH2=0,1.22,4=2,24l
=>m H2SO4=0,1.98=9,8g
=>mdd=98g
Đúng 4
Bình luận (0)
Giúp mk vs ạ, mk cảm ơn trc.
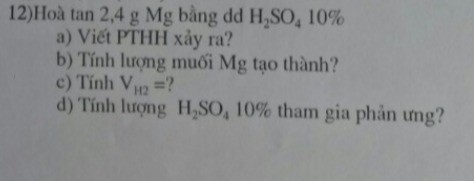
`a) PTHH:`
`Mg + H_2 SO_4 -> MgSO_4 + H_2`
`0,1` `0,1` `0,1` `0,1` `(mol)`
`n_[Mg] = [ 2,4 ] / 24 = 0,1 (mol)`
`b) m_[MgSO_4] = 0,1 . 120 = 12 (g)`
`c) V_[H_2] = 0,1 . 22,4 = 2,24 (l)`
`d) m_[dd H_2 SO_4] = [ 0,1 . 98 ] / 10 . 100 = 98 (g)`
Đúng 2
Bình luận (0)
Mg+H2SO4->MgSO4+H2
0,1----0,1------0,1---------0,1
n Mg=0,1 mol
=>m MgCl2=0,1.120=12g
=>VH2=0,1.22,4=2,24l
=>m H2SO4=0,1.98=9,8g
=>mdd=98g
Đúng 0
Bình luận (1)
`a) PTHH:`
`Zn + 2HCl -> ZnCl_2 + H_2↑`
`0,15` `0,3` `0,15` `(mol)`
`b) n_[Zn] = 13 / 65 = 0,2 (mol)`
Ta có: `[ 0,2 ] / 1 > [ 0,3 ] / 2`
`-> Zn` dư, `HCl` hết
`=> V_[H_2] = 0,15 . 22,4 = 3,36 (l)`
Đúng 2
Bình luận (0)
B1:
\(nP=\dfrac{6,2}{31}=0,2\left(mol\right)\)
\(nO_2=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH:
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
4 5 2 (mol)
0,2 0,25 0,1 (mol)
LTL : 0,2/4 < 0,3/5
=> P đủ , O2 dư
mO2(dư) = ( 0,3-0,25 ) . 32 = 1,6 (g)
chất được tạo thành là : P2O5
mP2O5 = 0,1 . 142 = 14,2 (g)
B2:bn lm tương tự cách lm b1
B3:\(nZn=\dfrac{13}{65}=0,2\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
1 2 1 1 (mol)
0,15 0,3 0,15 0,15
LTL : 0,2/1 > 0,3/2
=> HCl đủ , Zn dư
=> tính nH2 theo nHCl
=> nH2 = 0,15 (mol)
=> VH2= 0,15 . 22,4 = 3,36 (l)
Đúng 2
Bình luận (0)
bài 2 :
\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\\
n_{O_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\\
pthh:3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(LTL:\dfrac{0,15}{3}< \dfrac{0,5}{2}\)
=> O2 dư
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
0,15 0,05
=> \(m_{Fe_3O_4}=0,05.232=11,6g\)
Đúng 0
Bình luận (0)
Cho 7,8 gam kim loại kali tác dụng hoàn toàn với nước thu được dung dịch kali hidroxit và khí Hidro.
a. Viết PTHH xảy ra. Cho biết màu giấy quỳ tím thay đổi thế nào khi cho vào sản phẩm thu được, tại sao?
b. Tính thể tích khí Hạ sinh ra (ở đktc).
c. Tính khối lượng kali hidroxit
d. Cho toàn bộ khí H, vừa thu được khử vừa đủ với một lượng Fe3O4 ở nhiệt độ cao. Tính khối lượng Fe thu được. Biết hiệu suất phản ứng đạt 85 %. Cần câu D thôi nha. Giúp mình với ( Đáp án thôi cũng được)
Đọc tiếp
Cho 7,8 gam kim loại kali tác dụng hoàn toàn với nước thu được dung dịch kali hidroxit và khí Hidro. a. Viết PTHH xảy ra. Cho biết màu giấy quỳ tím thay đổi thế nào khi cho vào sản phẩm thu được, tại sao? b. Tính thể tích khí Hạ sinh ra (ở đktc). c. Tính khối lượng kali hidroxit d. Cho toàn bộ khí H, vừa thu được khử vừa đủ với một lượng Fe3O4 ở nhiệt độ cao. Tính khối lượng Fe thu được. Biết hiệu suất phản ứng đạt 85 %. Cần câu D thôi nha. Giúp mình với ( Đáp án thôi cũng được)
\(n_K=\dfrac{7,8}{39}=0,2\left(mol\right)\\
pthh:2K+2H_2O\rightarrow2KOH+H_2\uparrow\)
QT chuyển xanh
\(pthh:2K+2H_2O\rightarrow2KOH+H_2\)
0,2 0,2 0,1
\(V_{H_2}=0,1.22,4=2,24\left(L\right)\\
m_{KOH}=0,2.56=11,2\left(g\right)\)
\(pthh:Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O\)
0,1 0,075
=> \(m_{Fe}=\left(0,075.56\right).80\%=3,36g\)
Đúng 2
Bình luận (3)






















