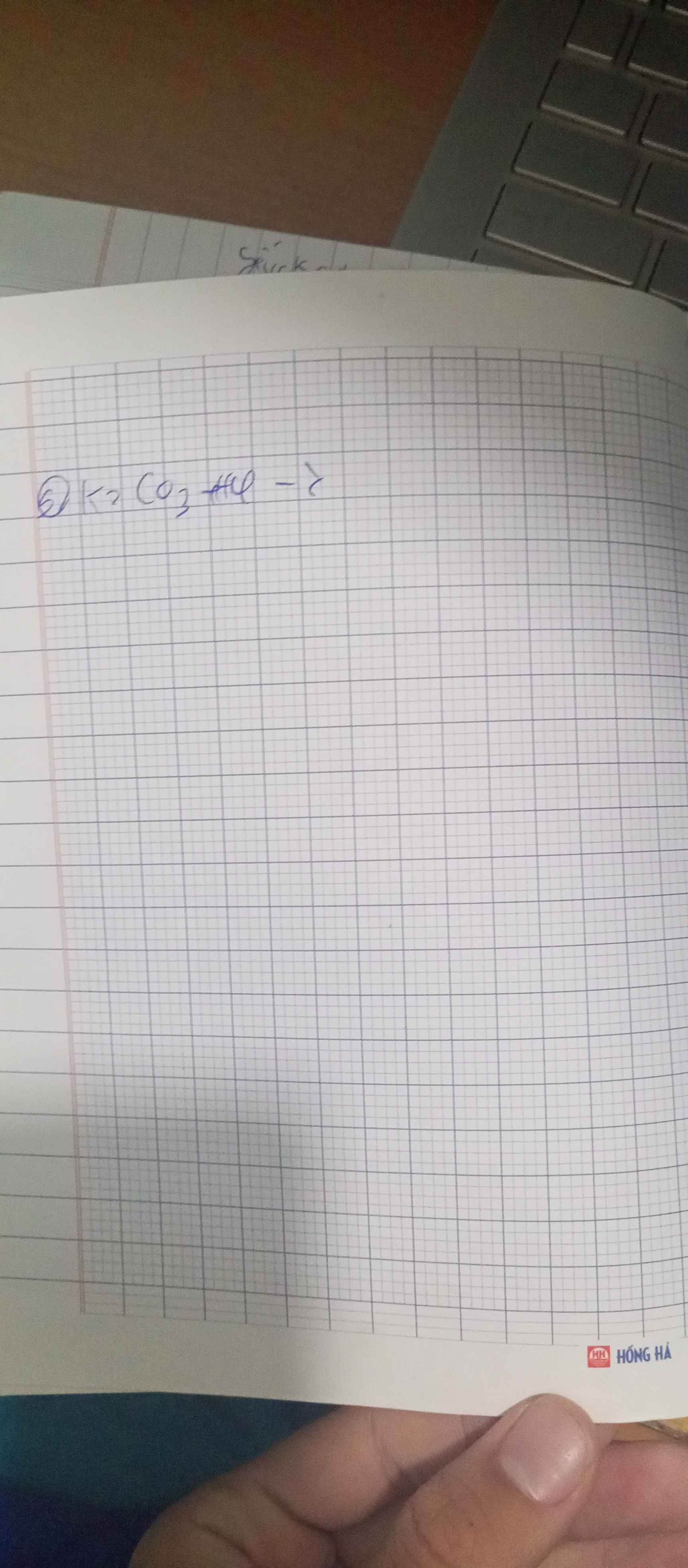Bài 4: Phản ứng trao đổi trong dung dịch các chất điện li
\(a,K_2CO_3+CaCl_2\rightarrow CaCO_3+2KCl\\ CO^{2-}_3+Ca^{2+}--->CaCO_3\\ b,CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\\ CaCO_3+2H^+--->Ca^{2+}+CO_2+H_2O\\ c,FeSO_4+2NaOH\rightarrow Fe\left(OH\right)_2+Na_2SO_4\\ Fe^{2+}+2OH^---->Fe\left(OH\right)_2\\ d,CuS+2HCl\rightarrow CuCl_2+H_2S\\ CuS+2H^+--->H_2S+Cu^{2+}\)
Đúng 2
Bình luận (0)
a) \(K_2CO_3+CaCl_2\rightarrow CaCO_3+2KCl\)
b) \(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\)
c) \(FeSO_4+2NaOH\rightarrow Fe\left(OH\right)_2+Na_2SO_4\)
d) \(CuS+2HCl\rightarrow CuCl_2+H_2S\)
Đúng 1
Bình luận (1)
Ion RG:
a) \(Ca^{2+}+CO_3^{2-}\rightarrow CaCO_3\)
b) \(CaCO_3+2H^+\rightarrow Ca^{2+}+H_2O+CO_2\)
c) \(Fe^{2+}+2OH^-\rightarrow Fe\left(OH\right)_2\)
d) \(CuS+2H^+\rightarrow Cu^{2+}+H_2S\)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Viết phương trình dạng phân tử và ion rút gọn
NaCl+AgNo3->
Hcl+AgNo3->
H2SO4+Ba(NO3)->
NaOH+CuSo4->
KOH+FeCl3->
HCl+NaOH->
H2SO4+KOH->
HNO3+Ba(OH)->
K2CO3+HCL->
FeS+HCl->
đang cần gấp ạ
Phương trình dạng phân tử :
\(1) NaCl + AgNO_3 \to AgCl + NaNO_3\\ 2) HCl + AgNO_3 \to AgCl + HNO_3\\ 3) H_2SO_4 + Ba(NO_3)_2 \to BaSO_4 + 2HNO_3\\ 4)2NaOH + CuSO_4 \to Cu(OH)_2 + Na_2SO_4\\ 5) 3KOH + FeCl_3 \to Fe(OH)_3 + 3KCl\\ 6) HCl + NaOH \to NaCl + H_2O\\ 7) H_2SO_4 + 2KOH \to K_2SO_4 + 2H_2O\\ 8) 2HNO_3 + Ba(OH)_2 \to Ba(NO_3)_2 + 2H_2O\\ 9)K_2CO_3 + 2HCl \to 2KCl + CO_2 + H_2O \\ 10) FeS + 2HCl \to FeCl_2 + H_2S\)
Phương trình dạng ion rút gọn :
\(Cl^- + Ag^+ \to AgCl\\ Cl^- + Ag^+ \to AgCl\\ SO_4^{2-} + Ba^{2+} \to BaSO_4\\ 2OH^- + Cu^{2+} \to Cu(OH)_2\\ Fe^{3+} + 3OH^- \to Fe(OH)_3\\ H^+ + OH^- \to H_2O\\ CO_3^{2-} + 2H^+ \to CO_2 + H_2O\\ FeS + 2H^+ \to Fe^{2+} + H_2S\)
Đúng 1
Bình luận (0)
\(1) NaCl + AgNO_3 \to AgCl + NaNO_3\\ 2) HCl + AgNO_3 \to AgCl + HNO_3\\ 3) H_2SO_4 + Ba(NO_3)_2 \to BaSO_4 + 2HNO_3\\ 4)2NaOH + CuSO_4 \to Cu(OH)_2 + Na_2SO_4\\ 5) 3KOH + FeCl_3 \to Fe(OH)_3 + 3KCl\\ 6) HCl + NaOH \to NaCl + H_2O\\ 7) H_2SO_4 + 2KOH \to K_2SO_4 + 2H_2O\\ 8) 2HNO_3 + Ba(OH)_2 \to Ba(NO_3)_2 + 2H_2O\\ 9)K_2CO_3 + 2HCl \to 2KCl + CO_2 + H_2O\)
Đúng 1
Bình luận (0)
Một dung dịch X chứa các ion Cl−, Na+ , Fe3+. Để kết tủa hết ion Cl− trong 10 ml dung dịch X cần dùng hết 40 ml dung dịch AgNO3 1M. Khi cô cạn 100 ml dung dịch X thì thu được 22,1 gam hỗn hợp hai muối khan.a) Tính nồng độ mol/l mỗi muối có trong dung dịch X.b) Lấy 10 ml dung dịch X trên tác dụng với 20 ml dung dịch NaOH 2M. Tính nồng độ mol/l các ion thu được sau phản ứng. Tính khối lượng kết tủa tạo thành. (Coi như thể tích dung dịch là không đổi)c) Để làm tan hết kết tủa tạo thành ở câu b cần...
Đọc tiếp
Một dung dịch X chứa các ion Cl−, Na+ , Fe3+. Để kết tủa hết ion Cl− trong 10 ml dung dịch X cần dùng hết 40 ml dung dịch AgNO3 1M. Khi cô cạn 100 ml dung dịch X thì thu được 22,1 gam hỗn hợp hai muối khan.
a) Tính nồng độ mol/l mỗi muối có trong dung dịch X.
b) Lấy 10 ml dung dịch X trên tác dụng với 20 ml dung dịch NaOH 2M. Tính nồng độ mol/l các ion thu được sau phản ứng. Tính khối lượng kết tủa tạo thành. (Coi như thể tích dung dịch là không đổi)
c) Để làm tan hết kết tủa tạo thành ở câu b cần dùng 100 ml dung dịch H2SO4 x(M). Tính x và xác định pH của dung dịch H2SO4.
a)
- Xét 10ml dd X
\(n_{AgNO_3}=1.0,04=0,04\left(mol\right)\)
\(AgNO_3\rightarrow Ag^++NO_3^-\)
0,04----->0,04
\(Ag^++Cl^-\rightarrow AgCl\)
0,04->0,04
100 ml dd X chứa \(\left\{{}\begin{matrix}Cl^-:0,4\left(mol\right)\\Na^+:a\left(mol\right)\\Fe^{3+}:b\left(mol\right)\end{matrix}\right.\)
Bảo toàn điện tích: a + 3b = 0,4 (1)
mmuối = 23a + 56b + 0,4.35,5 = 22,1
=> 23a + 56b = 7,9 (2)
(1)(2) => a = 0,1 (mol); b = 0,1 (mol)
\(\left\{{}\begin{matrix}C_{M\left(NaCl\right)}=\dfrac{0,1}{0,1}=1M\\C_{M\left(FeCl_3\right)}=\dfrac{0,1}{0,1}=1M\end{matrix}\right.\)
b) 10 ml dd X chứa \(\left\{{}\begin{matrix}Cl^-:0,04\left(mol\right)\\Na^+:0,01\left(mol\right)\\Fe^{3+}:0,01\left(mol\right)\end{matrix}\right.\)
nNaOH = 0,02.2 = 0,04 (mol)
\(NaOH\rightarrow Na^++OH^-\)
0,04---->0,04-->0,04
\(Fe^{3+}+3OH^-\rightarrow Fe\left(OH\right)_3\)
0,01--->0,03----->0,01
=> \(m_{Fe\left(OH\right)_3}=0,01.107=1,07\left(g\right)\)
dd sau pư chứa \(\left\{{}\begin{matrix}Cl^-:0,04\left(mol\right)\\Na^+:0,05\left(mol\right)\\OH^-:0,01\left(mol\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}C_{Cl^-}=\dfrac{0,04}{0,01+0,02}=\dfrac{4}{3}M\\C_{Na^+}=\dfrac{0,05}{0,01+0,02}=\dfrac{5}{3}M\\C_{OH^-}=\dfrac{0,01}{0,01+0,02}=\dfrac{1}{3}M\end{matrix}\right.\)
c)
\(n_{H_2SO_4}=0,1x\left(mol\right)\)
\(H_2SO_4\rightarrow2H^++SO_4^{2-}\)
0,1x----->0,2x
\(Fe\left(OH\right)_3+3H^+\rightarrow Fe^{3+}+3H_2O\)
0,01--->0,03
=> 0,2x = 0,03
=> x = 0,15
pH = -log(0,15) = 0,824
Đúng 1
Bình luận (0)
Tổng số nguyên tử trong phân tử natri nitrat là
A. 4. B. 5. C. 6.
\(NatriNitrat:NaNO_3\\ \Rightarrow Tổngsốnguyêntửlà:1+1+3=5\left(nguyêntử\right)\\ \Rightarrow ChọnB\)
Đúng 0
Bình luận (0)
Cho 6,9 gam Na vào 1 lít nước, cho thêm 13,5 gam CuCl2 vào dung dịch thu được. pH của dung dịch sau phản ứng là
\(n_{Na}=\dfrac{6,9}{23}=0,3\left(mol\right)\)
\(n_{CuCl_2}=\dfrac{13,5}{135}=0,1\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2
_____0,3---------------->0,3
2NaOH + CuCl2 --> Cu(OH)2 + 2NaCl
_0,2<----0,1
=> nNaOH dư = 0,1(mol)
=> \(C_{M\left(OH^-\right)}=\dfrac{0,1}{1}=0,1M\)
=> pH = 14 + log(0,1) = 13
Đúng 2
Bình luận (0)
nCuCl2=13,5135=0,1(mol)nCuCl2=13,5135=0,1(mol)
PTHH: 2Na + 2H2O --> 2NaOH + H2
_____0,3---------------->0,3
2NaOH + CuCl2 --> Cu(OH)2 + 2NaCl
_0,2<----0,1.
=> nNaOH dư = 0,1(mol)
=>
Đúng 1
Bình luận (0)
Viết phương trình phân tử, phương trình ion đầy đủ và phương trình ion rút gọn cho phân ứng sau nó có FeSo4 + NaoH
\(FeSO_4+2NaOH\rightarrow Fe\left(OH\right)_2\downarrow+Na_2SO_4\)
\(Fe^{2+}+SO_4^{2-}+Na^++2OH^-\rightarrow Fe\left(OH\right)_2\downarrow+Na^++SO_4^{2-}\)
\(Fe^{2+}+2OH^-\rightarrow Fe\left(OH\right)_2\downarrow\)
Đúng 1
Bình luận (0)
\(\left(1\right)CuSO_4+BaCl_2\rightarrow BaSO_4+CuCl_2\\ SO_4^{2-}+Ba^{2+}\rightarrow BaSO_4\\ \left(2\right)HNO_3+NaHCO_3\rightarrow NaNO_3+CO_2+H_2O\\ H^++HCO_3^-\rightarrow CO_2+H_2O\)
Đúng 2
Bình luận (0)
Hoàn thành các pt phản ứng và viêt pt ion rút gọn:
1)NaHPO4+NaOH->
2)Cu+HNO3->
3)Na2HPO4+HCl(tỉ lệ 1:1)
4)NaH2PO4+Ca(OH)2 (tỉ lệ 1:1)
Câu 1: Tính nồng độ ion trong các dung dịch sau:
a. Dung dịch NaCl 0,05M
b. Dung dịch NaHSO\(_4\) 0,2M
Giúp mk vs ạ thanks trước