Nhóm chất nào sau đây tác dụng được với H2SO4 loãng
A.CuO,BaCl2,NaCl,FeCO3
B. Cu,Cu(OH)2,Na2CO3,KCl
C. Fe,ZnO,MgCl2,NaOH
D. Mg,BaCl2,K2CO3,Al2O3
giải thích vì sao
Nhóm chất nào sau đây tác dụng được với H2SO4 loãng
A.CuO,BaCl2,NaCl,FeCO3
B. Cu,Cu(OH)2,Na2CO3,KCl
C. Fe,ZnO,MgCl2,NaOH
D. Mg,BaCl2,K2CO3,Al2O3
giải thích vì sao
D
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(BaCl_2+H_2SO_4\rightarrow BaSO_4\downarrow+2HCl\)
\(K_2CO_3+H_2SO_4\rightarrow K_2SO_4+CO_2+H_2O\)
\(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
Nguyên tố A có số nguyên tử là 11 hãy cho biết: a) Cấu tạo nguyên tử của nguyên tố A, vị trí của A trong bản tuần hoàn các Nguyên Tố Hoá Học b) Dự đoán: Tính chất của A làm kim loại hay phi kim c) So sánh tính chất hoá học của A với các nguyên tố lân cận
a: Cấu tạo nguyên tử của A là 11 proton và 11 electron
Cấu hình: \(1s^22s^22p^63s^1\)
Vị trí: Chu kì 3, nhóm IA
b: A là kim loại vì có 1 e lớp ngoài cùng
Cho 69,6g MnO2 tác dụng với dung dịch HCl đặc dư thu được một lượng khí X. Dẫn khí X vào 500ml dung dịch NaOH 4M thu được dung dịch A. Tính nồng độ mol của các chất trong dung dịch A. Giả thiết rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể.
a) Phương trình hóa học của phản ứng:
b) Theo pt (1): nCl2 = nMnCl2 = nMnO2 = 0,8 mol
Theo pt (2): nNaCl = nNaClO = nCl2 = 0,8 mol
nNaOH pư = 2. nCl2 = 2. 0,8 = 1,6 mol
⇒ nNaOH dư = 2 - 1,6 = 0,4 mol
Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM (NaCl) = CM (NaClO) = CM(MnCl2) = 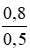
CM (NaOH)dư = 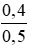
tích cho mình nha![]()
hỗn hợp chứa 16,8 gam FeO và Cu phản ứng tối đa với 50mk H2SO4 2,OM ( loãng )
a) có khí nào thoát ra sau phản ứng không
b) tính %(m) FeO
c) tính khối lượng chất tan trong dung dịch sau pứ
làm giúp e mn ơii
cho 100ml dung dịch HCL 2M phản ứng với lượng vừa đủ V ml dung dịch NA2CO3 1M. 1. tính v? 2. tính khối lượng muối thu được 3. tính thể tích khí thu được ở đktc
1) $n_{HCl} = 0,1.2 = 0,2(mol)$
$Na_2CO_3 + 2HCl \to 2NaCl + CO_2 + H_2O$
Theo PTHH :
$n_{Na_2CO_3} = \dfrac{1}{2}n_{HCl} = 0,1(mol)$
$V_{dd\ Na_2CO_3} = \dfrac{0,1}{1} = 0,1(lít) = 100(ml)$
2)
$n_{NaCl} = n_{HCl} = 0,2(mol)$
$m_{NaCl} = 0,2.58,5 = 11,7(gam)$
3)
$n_{CO_2} = n_{Na_2CO_3} = 0,1(mol)$
$V_{CO_2} = 0,1.22,4 = 2,24(lít)$
100ml =0,1l
\(n_{HCl}=2.0,1=0,2\left(mol\right)\)
Pt : \(HCl+Na_2CO_3\rightarrow2NaCl+CO_2+H_2O|\)
1 1 2 1 1
0,2 0,2 0,4 0,2
1) \(n_{Na2CO3}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(V_{ddNa2CO3}=\dfrac{0,2}{1}=0,2\left(l\right)\)
2) \(n_{NaCl}=\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
⇒ \(m_{NaCl}=0,4.58,5=23,4\left(g\right)\)
3) \(n_{CO2}=\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
\(V_{CO2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
Chúc bạn học tốt
1. \(n_{HCl}=0,1.2=0,2\left(mol\right)\)
PTHH: 2HCl + Na2CO3 → 2NaCl + CO2 + H2O
Mol: 0,2 0,1 0,2 0,1
\(V_{ddNa_2CO_3}=\dfrac{0,1}{1}=0,1\left(l\right)\)
2. \(m_{NaCl}=0,2.58,5=11,7\left(g\right)\)
3. \(V_{CO_2}=0,1.22,4=2,24\left(l\right)\)
cho z gam hỗn hợp gồm znso3 zn cuso3 feso3 tác dụng vừa hết với dd hcl dư thu được 19,6 gam hỗn hợp khí b chiếm 11,2l khí nếu cô cạn dung dịch sau phản ứng thì thu được 67g muối khan. tìm giá trị z help !
$ZnSO_3 + 2HCl \to ZnCl_2 +S O_2 + H_2O$
$Zn + 2HCl \to ZnCl_2 + H_2$
$CuSO_3 + 2HCl \to CuCl_2 +S O_2 + H_2O$
$FeSO_3 + 2HCl \to FeCl_2 +S O_2 + H_2O$
Gọi $n_{SO_2} = a ; n_{H_2} = b$
Ta có :
$a + b = 0,5$
$64a + 2b = 19,6$
Suy ra a = 0,3 ; b = 0,2
Theo PTHH :
$n_{HCl} = 2n_{khí} = 1(mol)$
$n_{H_2O} = n_{SO_2} = 0,3(mol)$
Bảo toàn khối lượng :
$z = 19,6 + 0,3.18 + 67 - 1.36,5 = 55,5(gam)$
1. Nhận biết
- H2CO3; HCl; HNO3; Cu(OH)2 ; Zn(OH)2 và Fe(OH)3- H2PO4; H2SO4; HCl; KCl; K2CO3; CaCO32. Xác định vị trí; cấu tạo; tính chất và so sánh- Nguyên tố có 8 e lớp ngoài cùng và có 3 lớp e- Nguyên tố có số e = 19
\(n_{Fe} = a(mol) ; n_{Mg} = b(mol)\\ \Rightarrow 56a + 24b = 16,8 - 6,4 = 10,4(1)\\ Fe + 2HCl \to FeCl_2 + H_2\\ Mg + 2HCl \to MgCl_2 + H_2\\ n_{H_2} = a + b = \dfrac{6,72}{22,4} = 0,3(2)\)
Từ (1)(2) suy ra: a = 0,1 ; b = 0,2
Vậy :
\(\%m_{Fe} = \dfrac{0,1.56}{16,8}.100\% = 33,33\%\\ \%m_{Mg} = \dfrac{0,2.24}{16,8}.100\% = 28,57\%\\ \%m_{Cu} = 100\% - 33,33\% - 28,57\% = 38,1\%\)
a) Ta có: \(\dfrac{16\cdot5}{2.M_X+16\cdot5}\cdot100=56,34\) \(\Rightarrow M_X=31\)
\(\Rightarrow\) X là Photpho
b)
- Hợp chất oxit: P2O5
- Hợp chất với hidro: PH3