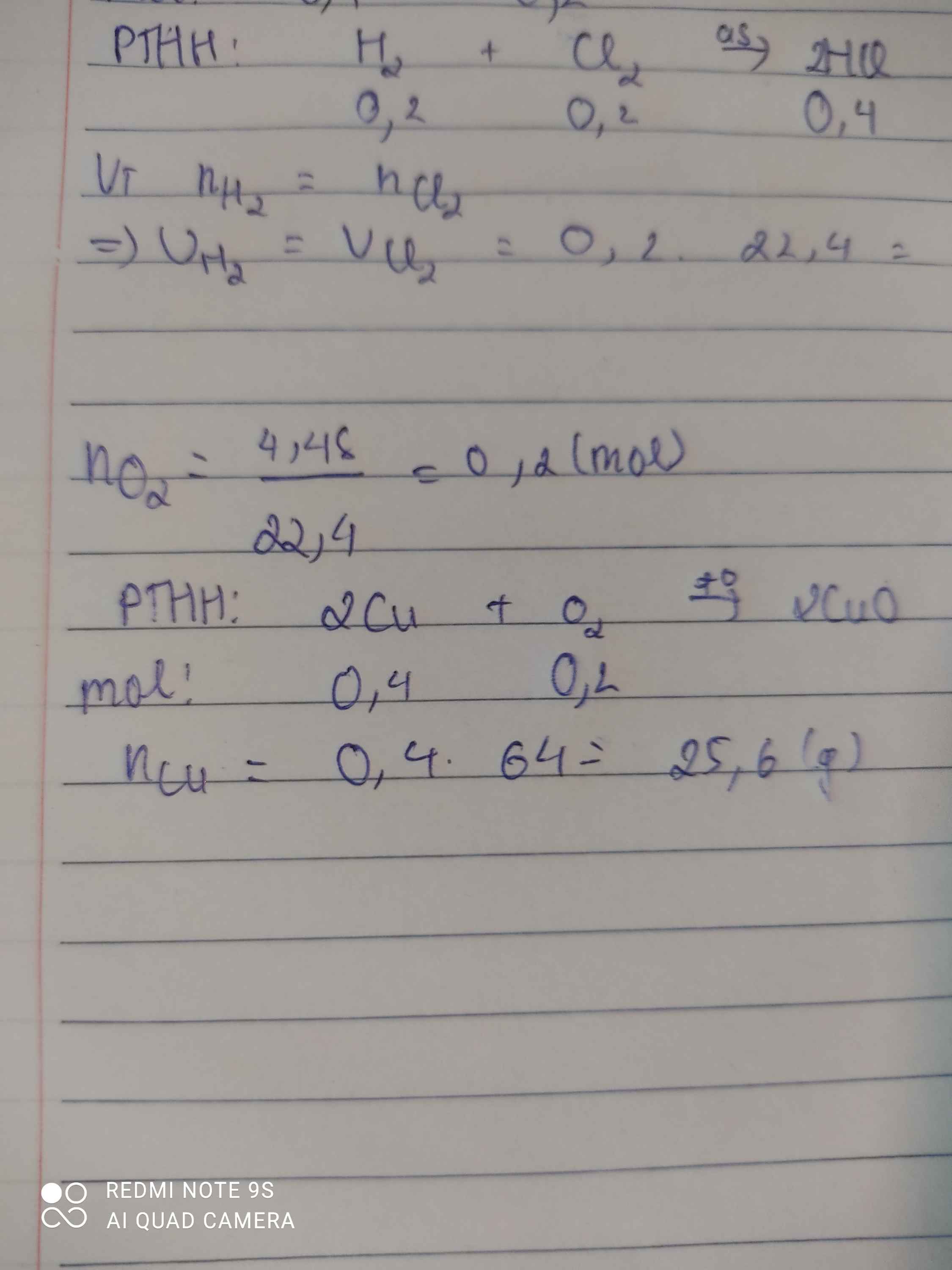Một acid có thành phần % về khối lượng là 1,0% H; 35,32% Cl và
63,68% O. Biết khối lượng mol của acid là 100,5 g. Tìm CTHH của hợp chất.
Bài 21: Tính theo công thức hóa học
\(m_H=\dfrac{1.100,5}{100}=1\left(g\right)1\Rightarrow n_H=\dfrac{1}{1}=1\left(mol\right)\)
\(m_{Cl}=\dfrac{35,32.100,5}{100}=35,5\left(g\right)\Rightarrow n_{Cl}=\dfrac{35,5}{35,5}=1\left(mol\right)\)
\(m_O=\dfrac{63,68.100,5}{100}=64\left(g\right)\Rightarrow n_O=\dfrac{64}{16}=4\left(mol\right)\)
=> CTHH: HClO4
Đúng 3
Bình luận (4)
Đốt cháy hoàn toàn V(lit) khi thiên nhiên ( có chứa 90% CH4 :5% C2H4,và 5% C2H8) cần dùng vừa đủ 246,4lit không khí ( có chứa 80% N2 và 20% O2) thu được khí CO2 và H2O
a) Tìm V?
b) Tính thể tích hỗn hợp khí thu được sau phản ứng
Biết các khí được đo ở cùng điều kiện về nhiệt độ và áp suất.
a) Giả sử các khí được đo ở điều kiện sao cho 1 mol khí chiếm thể tích 1 lít
Gọi số mol hỗn hợp khí là a (mol) => \(\left\{{}\begin{matrix}n_{CH_4}=0,9a\left(mol\right)\\n_{C_2H_4}=0,05a\left(mol\right)\\n_{C_3H_8}=0,05a\left(mol\right)\end{matrix}\right.\)
\(n_{O_2}=\dfrac{246,4.20\%}{1}=49,28\left(mol\right)\)
=> \(n_{N_2}=\dfrac{246,4}{1}-49,28=197,12\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,9a->1,8a---->0,9a--->1,8a
C2H4 + 3O2 --to--> 2CO2 + 2H2O
0,05a->0,15a------>0,1a-->0,1a
C3H8 + 5O2 --to--> 3CO2 + 4H2O
0,05a-->0,25a----->0,15a-->0,2a
=> 1,8a + 0,15a + 0,25a = 49,28
=> a = 22,4 (mol) => V = 22,4.1 = 22,4 (l)
b) Sau phản ứng thu được \(\left\{{}\begin{matrix}N_2:197,12\left(mol\right)\\CO_2:25,76\left(mol\right)\\H_2O:47,04\left(mol\right)\end{matrix}\right.\)
- Nếu H2O ở thể lỏng
=> hh khí gồm N2, CO2
=> \(V_{hh}=\left(197,12+25,76\right).1=222,88\left(l\right)\)
- Nếu H2O ở thể khí
=> hh gồm N2, CO2, H2O
=> \(V_{hh}=\left(197,12+25,76+47,04\right).1=269,92\left(l\right)\)
Đúng 1
Bình luận (0)
giúp mình với ạ
Đốt cháy 11.2 lít khí H2 trong 22,4 lít O2(đktc) để tạo thành nước.Tính:a) Chất nào còn thừa sau phản ứng và có khối lượng bằng bao nhiêu?b) tính khối lượng sản phẩm thu đc sau phản ứng? M.n giúp mình bài 2 trc đk mình đang gấp lắm Cho 15,6 gam Zn vào trong dung dịch H2SO4 loãng chứa 39,2 gam H2SO4 a- Tính thể tích H2 thu đc (đktc). Biết rằng H2 bị hao hụt 5%b- Chất nào còn dư sau phản ứng? Khối lượng còn dư là bao nhiêu gam?
Đọc tiếp
Đốt cháy 11.2 lít khí H2 trong 22,4 lít O2(đktc) để tạo thành nước.Tính:
a) Chất nào còn thừa sau phản ứng và có khối lượng bằng bao nhiêu?
b) tính khối lượng sản phẩm thu đc sau phản ứng?
M.n giúp mình bài 2 trc đk mình đang gấp lắm
Cho 15,6 gam Zn vào trong dung dịch H2SO4 loãng chứa 39,2 gam H2SO4
a- Tính thể tích H2 thu đc (đktc). Biết rằng H2 bị hao hụt 5%
b- Chất nào còn dư sau phản ứng? Khối lượng còn dư là bao nhiêu gam?
Bài 2:
\(n_{Zn}=\dfrac{15,6}{65}=0,24\left(mol\right);n_{H_2SO_4}=\dfrac{39,2}{98}=0,4\left(mol\right)\\ Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ a,Vì:\dfrac{0,4}{1}>\dfrac{0,24}{1}\Rightarrow H_2SO_4dư\\ n_{H_2\left(LT\right)}=n_{H_2SO_4\left(p.ứ\right)}=n_{Zn}=0,24\left(mol\right)\\ a,n_{H_2\left(TT\right)}=50\%.0,24=0,12\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc,thực.tế\right)}=0,12.22,4=2,688\left(l\right)\\ b,n_{H_2SO_4\left(dư\right)}=0,4-0,24=0,16\left(mol\right)\\ \Rightarrow m_{H_2SO_4\left(dư\right)}=0,16.98=15,68\left(g\right)\)
Đúng 3
Bình luận (0)
Bài trên
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right);n_{O_2}=\dfrac{22,4}{22,4}=1\left(mol\right)\\ a,PTHH:2H_2+O_2\rightarrow\left(t^o\right)2H_2O\\ Vì:\dfrac{1}{1}>\dfrac{0,5}{2}\Rightarrow O_2thừa\\ n_{O_2\left(thừa\right)}=1-\dfrac{0,5}{2}=0,75\left(mol\right)\\ \Rightarrow m_{O_2\left(thừa\right)}=0,75.32=24\left(g\right)\\ b,n_{H_2O}=n_{H_2}=0,5\left(mol\right)\Rightarrow m_{H_2O}=0,5.18=9\left(g\right)\)
Đúng 2
Bình luận (0)
Một loại đồng oxit màu đen có khối lượng mol phân tử là 20g/mol, có thành phần về khối lượng là 80% Cu và 20% O. Công thức của oxit
Đồng oxit nào mà có M= 20(g/mol) được em.
Nhưng em bảo 80% Cu, 20% O thì anh thấy chắc là CuO rồi nè
Đúng 3
Bình luận (0)
sửa đề M = 80 g/mol
\(n_{Cu}=\dfrac{80.80\%}{64}=1\left(mol\right)\\ n_{O_2}=\dfrac{80-64}{16}=1\left(mol\right)\\ Cthh:CuO\)
Đúng 2
Bình luận (0)
Đốt dây đồng ở ĐKTC trong 4,48 (L) O2 ( ở đktc) thu được oxi đồng ( CuO) Lập pt hóa học và khối lượng đã phản ứng
\(n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: 2Cu + O2 ---to→ CuO
Mol: 0,4 0,2
\(m_{Cu}=64.0,4=25,6\left(g\right);m_{O_2}=0,2.32=6,4\left(g\right)\)
Đúng 0
Bình luận (0)
\(n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH : 2Cu +O2 -> 2CuO
0,4 0,2 (mol)
\(m_{Cu}=0,4.64=25,6\left(g\right)\)
Đúng 1
Bình luận (0)
Tính thành phần phần trăm về khối lượng của các nguyên tố có trong công thức K2SO3
\(\%K=\dfrac{m_K}{M_{K_2SO_3}}=\dfrac{78}{158}=49,36\%\\ \%S=\dfrac{m_S}{M_{K_2SO_3}}=\dfrac{32}{158}=20,25\%\\ \%O=100\%-\%K-\%S=100\%-49,36\%-20,25\%=30,39\%\)
Đúng 3
Bình luận (1)
Hãy tìm công thức hoá học của khí A. Biết rằng : - khí A nặng hơn khí Hiđro 8, 5 lần - Thành phần theo khối lượng của khí A là 82,35%N và 17,65%H
\(d_{\dfrac{A}{H_2}}=8,5\\ M_{H_2}=2\left(\dfrac{g}{mol}\right)\\ \Rightarrow M_A=d_{\dfrac{A}{H_2}}.M_{H_2}=8,5.2=17\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow m_N=\%N.M_A=82,35\%.17=14\left(g\right)\\ m_H=m_A-m_N=17-14=3\left(g\right)\\ \Rightarrow n_N=\dfrac{m}{M}=\dfrac{14}{14}=1\left(mol\right)\\ n_H=\dfrac{m}{M}=\dfrac{3}{1}=3\left(mol\right)\\ CTHH:NH_3\)
Đúng 2
Bình luận (1)
\(M_A=M_{H_2}.8,5=2.8,5=17(g/mol)\)
Đặt CTHH của \(A\) là \(N_xH_y\)
Ta có : \(\dfrac{14x.100}{17}=82,35\)
\(-> x=1\)
Ta có : \(\dfrac{y.100}{17}=17,65\)
\(->y=3\)
Vậy CTHH của \(A\) là \(NH_3\)
Đúng 1
Bình luận (3)
Hãy tính thành phần phần trăm theo khối lượng nguyên tố Nitơ trong phân Amoni sunfat
Amoni sunfat: (NH4)2SO4
\(\%N=\dfrac{14\times2\times100}{8+14\times2+32+16\times4}=21.21\%\)
Đúng 1
Bình luận (0)
Cách tính số phân tử của 1 chất? Vd: Tính số phân tử khí hidro(H2)?
Ta nhân với số N hay số Avogadro (6.1023)
Số phân tử H2 = 6.1023 phân tử
Đúng 0
Bình luận (4)