Nhỏ từ từ dung dịch Ba(OH)2 vào ống nghiệm chứa dung dịch H2SO4 và Al2(SO4)3. Đồ thị biểu diễn sự phụ thuộc khối lượng kết tủa theo thể tích dung dịch Ba(OH)2 như sau. Tính giá trị m max. (Trình bày chi tiết giúp em theo pthh với!)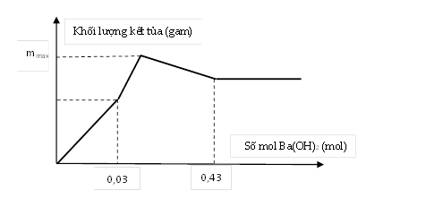
Bài 18. Nhôm
Nhỏ từ từ dung dịch Ba(OH)2 vào ống nghiệm chứa dung dịch HCl (a mol) và Al2(SO4)3 (b mol). Đồ thị biểu diễn sự phụ thuộc khối lượng kết tủa theo thể tích dung dịch Ba(OH)2 như sau. Tính giá trị của a:b? ( trình bày chi tiết giúp em theo pthh với!)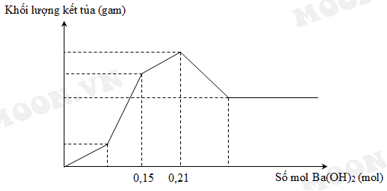
Nhỏ từ từ dung dịch Ba(OH)2 vào dung dịch chứa đồng thời HCl và Al2(SO4)3. Khối lượng kết tủa phụ thuộc vào số mol Ba(OH)2 được biểu diễn như hình sau. Tìm tổng (x+y). (Làm theo phương trình hóa học giúp mình nhé!)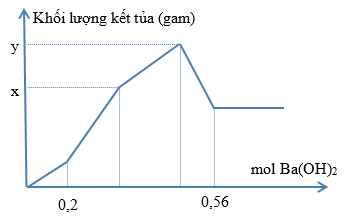
Đoạn OA :
\(Ba\left(OH\right)_2+2HCl\text{→}BaCl_2+2H_2O\)
0,2 0,2 (mol)
\(3BaCl_2+Al_2\left(SO_4\right)_3\text{→}3BaSO_4+2AlCl_3\)
0,2 0,6 \(\dfrac{0,4}{3}\) (mol)
Đoạn AB :
\(3Ba\left(OH\right)_2+Al_2\left(SO_4\right)_3\text{→}3BaSO_4+2Al\left(OH\right)_3\)
3a 3a 2a (mol)
Đoạn BC :
\(2AlCl_3+3Ba\left(OH\right)_2\text{→}2Al\left(OH\right)_3+3BaCl_2\)
\(\dfrac{0,4}{3}\) 0,2 \(\dfrac{0,4}{3}\) (mol)
Đoạn CD :
\(2Al\left(OH\right)_3+Ba\left(OH\right)_2\text{→}Ba\left(AlO_2\right)_2+4H_2O\)
(\(\dfrac{0,4}{3}\)+2a) (\(\dfrac{0,2}{3}\) + a) (mol)
$\Rightarrow n_{Ba(OH)_2} = 0,2 + 3a + 0,2 + \dfrac{0,2}{3} + a = 0,56 \Rightarrow a = \dfrac{7}{300}$
Suy ra:
$x = 0,6.233 + 3a.233 + 2a.78 = 139,8 + 855a = 159,75(gam)$
$y = x + \dfrac{0,4}{3}.78 = 170,15(gam)$
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 16,6g hỗn hợp cùng Na và Ca vào H2O thu được 8,96l khí H2 (đktc)
a) Tính khối lượng từng kim loại trong hỗn hợp ban đầu
b)Tính khối lượng các bazơ tạo thành
a, PT: \(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\)
Gọi: \(\left\{{}\begin{matrix}n_{Na}=x\left(mol\right)\\n_{Ca}=y\left(mol\right)\end{matrix}\right.\)
⇒ 23x + 40y = 16,6 (1)
Ta có: \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Theo PT: \(n_{H_2}=\dfrac{1}{2}n_{Na}+n_{Ca}=\dfrac{1}{2}x+y=0,4\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,3\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Na}=0,2.23=4,6\left(g\right)\\m_{Ca}=0,3.40=12\left(g\right)\end{matrix}\right.\)
b, Theo PT: \(\left\{{}\begin{matrix}n_{NaOH}=n_{Na}=0,2\left(mol\right)\\n_{Ca\left(OH\right)_2}=n_{Ca}=0,3\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{NaOH}=0,2.40=8\left(g\right)\\m_{Ca\left(OH\right)_2}=0,3.74=22,2\left(g\right)\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Câu hỏi nhỏ: Sục hỗn hợp khí (CO, CO2) vào dung dịch Ba(AlO2)2 thu được kết tủa H và dung dịch G. Hỏi thành phần của H, G? (P/s: Đề bài chưa nói hỗn hợp khí dư hay hết)
H : $Al(OH)_3 ; BaCO_3$(có thể có)
G : $Ba(HCO_3)_2$ (có thể có)
$Ba(AlO_2)_2 + CO_2 + 3H_2O \to 2Al(OH)_3 + BaCO_3$
$BaCO_3 + CO_2 + H_2O \to Ba(HCO_3)_2$
Đúng 2
Bình luận (0)
H : Al(OH)3;BaCO3Al(OH)3;BaCO3(có thể có)
G : Ba(HCO3)2Ba(HCO3)2 (có thể có)
Ba(AlO2)2+CO2+3H2O→2Al(OH)3+BaCO3Ba(AlO2)2+CO2+3H2O→2Al(OH)3+BaCO3
BaCO3+CO2+H2O→Ba(HCO3)2
Đúng 0
Bình luận (0)
Nhỏ từ từ dung dịch Ba(OH)2 đến dư vào dung dịch hỗn hợp Al2(SO4)3 và Na2SO4 ta có đồ thị biểu diễn sự phụ thuộc khối lượng kết tủa theo số mol Ba(OH)2 như sau. Tìm x, t? (P/s: Làm theo phương trình giúp mình nhé!)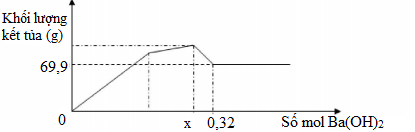
Nhỏ từ từ dung dịch Ba(OH)2 vào dung dịch chứa (a mol Na2SO4, b mol Al2(SO4)3). Đồ thu biểu diễn như sau. Tìm a, b. ( Làm theo phương trình hóa học giúp mình nhé!)
Tại thời điểm khối lượng 36,51 gam là lượng kết tủa lớn nhất gồm Al(OH)3, BaSO4. Còn tại thời điểm 34,95 gam là lượng kết tủa chỉ gồm có BaSO4.
PTHH: \(Na_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4\downarrow+2NaOH\)
\(Al_2\left(SO_4\right)_3+3Ba\left(OH\right)_2\rightarrow2Al\left(OH\right)_3\downarrow+3BaSO_4\downarrow\)
\(2Al\left(OH\right)_3+Ba\left(OH\right)_2\rightarrow Ba\left(AlO_2\right)_2+4H_2O\)
\(n_{BaSO_4}=\dfrac{34,95}{233}=0,15\left(mol\right)\\ n_{Al\left(OH\right)_3}=\dfrac{36,51-34,95}{78}=0,02\left(mol\right)\)
BTNT Al: \(b=n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Al\left(OH\right)_3}=0,01\left(mol\right)\)
BT =SO4: \(a=n_{Na_2SO_4}=n_{BaSO_4}-3n_{Al_2\left(SO_4\right)_3}=0,12\)
Đúng 2
Bình luận (0)
Cho 86,3 gam hỗn hợp X gồm Na, K, Ba và Al2O3 ( trong đó oxi chiếm 19,47% về khối lượng) tan hết vào nước, thu được dung dịch Y và 13,44 lít khí H2 ( đktc). Cho V lít dd HCl 2M vào dd, sau khi các phản ứng xảy ra hoàn toàn thu được 46,8 gam kết tủa. Tính thể tích dd HCl đã dùng.
$n_O = \dfrac{86,3.19,47\%}{16} = 1,05(mol)$
Coi hỗn hợp gồm $Na(a\ mol) , Al(b\ mol)$ và O(1,05 mol)
Ta có :
$23a + 27b + 1,05.16 = 86,3(1)$
Bảo toàn electron : $n_{Na} + 3n_{Al} = 2n_O + 2n_{H_2}$
$\Rightarrow a + 3b = 1,05.2 + 0,6.2(2)$
Từ (1)(2) suy ra $a = \dfrac{199}{70} ; b = \dfrac{16}{105}$
Suy ra Y gồm :
$AlO_2^- : \dfrac{16}{105}(mol)$
$Na^+ : \dfrac{199}{70}(mol)$
$OH^- : \dfrac{199}{70} - \dfrac{16}{105} = \dfrac{113}{42}(mol)$
$n_{Al(OH)_3} = \dfrac{46,8}{78} = 0,6(mol)$
Suy ra :
$n_{HCl} = n_{H^+} = n_{OH^-} + 4n_{AlO_2^-} - 3n_{Al(OH)_3} = 1,5(mol)$
$V_{dd\ HCl} = \dfrac{1,5}{2} = 0,75(lít)$
Đúng 1
Bình luận (0)
Cho hỗn hợp A gồm 2 muối là MHCO3 và X2CO3. Lấy 24,2 gam hỗn hợp A tác dụng với lượng vừa đủ dung dịch HCl, thu được tối đa 6,72 lít khí (đktc). Đem toàn bộ lượng muối tạo thành tác dụng vừa đủ với dd NaOH, rồi cô cạn thu được m gam 1 muối duy nhất. a) Xác định công thức và tính khối lượng của 2 muối trong A. b) Tính m (Giúp mình bài này với)
Dẫn khí H2 dư đi qua hỗn hợp A gồm CuO, Fe2O3, K2O, Al2O3, MgO nung nóng, sau phản ứng thu được hỗn hợp rắn B. Cho hỗn hợp B vào dung dịch Ba(OH)2, sau phản ứng hoàn toàn thu được dung dịch C (chứa 2 chất tan) và chất rắn D. Sục khí CO2 dư vào dung dịch C thì thu được kết tủa G. Cho D vào dung dịch H2SO4 đặc, nóng thì được dung dịch E, khí F mùi hắc và chất rắn chứa 1 kim loại. Xác định thành phần A, B, C, D, F, G và viết phương trình xảy ra.
Đọc tiếp
Dẫn khí H2 dư đi qua hỗn hợp A gồm CuO, Fe2O3, K2O, Al2O3, MgO nung nóng, sau phản ứng thu được hỗn hợp rắn B. Cho hỗn hợp B vào dung dịch Ba(OH)2, sau phản ứng hoàn toàn thu được dung dịch C (chứa 2 chất tan) và chất rắn D. Sục khí CO2 dư vào dung dịch C thì thu được kết tủa G. Cho D vào dung dịch H2SO4 đặc, nóng thì được dung dịch E, khí F mùi hắc và chất rắn chứa 1 kim loại. Xác định thành phần A, B, C, D, F, G và viết phương trình xảy ra.











