Đốt cháy hoàn toàn 6 g C trong bình kín đựng 22,4 lít khí O2, sau phản ứng thể tích khí trong bình là (các thể tích được đo ở đktc)
Đốt cháy hoàn toàn 6 g C trong bình kín đựng 22,4 lít khí O2, sau phản ứng thể tích khí trong bình là (các thể tích được đo ở đktc)
PTHH: C + \(O_2\) ---> \(CO_2\)
0,5 mol 0,5 mol 0,5 mol
+ Số mol của C:
\(n_C\) = \(\dfrac{m}{M}\) = \(\dfrac{6}{12}\) = 0,5 (mol)
+ Số mol của \(O_2\)
\(n_{O_2}\) = \(\dfrac{V}{22,4}\) = \(\dfrac{22,4}{22,4}\) = 1 (mol)
Tỉ lệ: C \(O_2\)
0,5 < 1
=> C hết; \(O_2\) dư
+ Thể tích \(CO_2\)
\(V_{O_2}\) = n . 22,4 = 0,5 . 22,4 = 11,2 (lít)
Vậy: thể tích khí \(CO_2\) sau phản ứng là 11,2 lít
\(n_C=\dfrac{6}{12}=0,5\left(mol\right)\)
\(n_{O_2}=\dfrac{22,4}{22,4}=1mol\)
pt : \(C+O_2\rightarrow CO_2\)
Theo pt \(\dfrac{n_C}{n_{O_2}}=0,5:1=1:2\)
=> Oxi dư
\(n_{O_2}\) dư = 1 - 0,5 = 0,5 (mol)
=> \(V_{O_2}dư=11,2lit\)
Theo pt : \(n_{CO_2}=0,5\left(mol\right)\)
=> VCO2 = 11,2 lít
Vậy trong bình còn lại 11,2 lí CO2 và 11,2 lít O2
Bài 2 :
\(2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ 2Cu + O_2 \xrightarrow{t^o} 2CuO\\ C + O_2 \xrightarrow{t^o} CO_2\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\\ \)
Bài 3 :
\(a) 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ b) n_{Al} = \dfrac{10,8}{27}=0,4(mol)\\ n_{H_2} = \dfrac{3}{2}n_{H_2} = 0,6(mol)\\ V_{H_2} = 0,6.22,4 = 13,44(lít)\\ c) Fe_3O_4 + 4H_2 \xrightarrow{t^o} 3Fe + 4H_2O\\ n_{Fe} = \dfrac{3}{4}n_{H_2} =0,45(mol)\\ m_{Fe} = 0,45.56 = 25,2(gam)\)
Bài 4 :
\(a) 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ b) n_{KMnO_4} =\dfrac{18,96}{158}=0,12(mol)\\ n_{O_2}= \dfrac{1}{2}n_{KMnO_4} =0,06(mol)\\ V_{O_2} = 0,06.22,4= 1,344(lít)\\ c) n_{Al} = \dfrac{1,62}{27} = 0,06(mol)\\ 4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3\\ \dfrac{n_{Al}}{4} = 0,015 < \dfrac{n_{O_2}}{3} = 0,02 \to O_2\ dư\\ n_{Al_2O_3} = \dfrac{1}{2}n_{Al} = 0,03(mol)\\ \)
\(m_{Al_2O_3} = 0,03.102 = 3,06(gam)\)
Biết nguyên tử B có tổng số hạt là 21. Số hạt không mang điện chiếm 33.33%. Xác định số hạt mang điện.
7
14
5
21
Theo bài ta có :\(2p+n=21\left(p=e\right)\)
Mặt khác: số hạt không mang điện chiếm 33.33%
=> \(n=33,33\%.21\approx7\)
\(\Rightarrow p=e=\dfrac{21-7}{2}=7\)
Vậy số hạt mang điện là 14
N= 33,33%.21=7(hạt)
Số hạt mang điện: 21-7=14(hạt)
=>CHỌN 14
Cho m gam Ba(OH)2 tác dụng vừa đủ với 200g dd HCl 7,3% thu được muối và nước. Tính khối lượng Ba(OH)2 đã tham gia phản ứng?
\(n_{HCl}=\dfrac{200\cdot7.3\%}{36.5}=0.4\left(mol\right)\)
\(Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\)
\(0.2..................0.4\)
\(m_{Ba\left(OH\right)_2}=0.2\cdot171=34.2\left(g\right)\)
Viết phương trình chữ của phản ứng trên. Biết vỏ quả trứng (thành phần chủ yếu là calcium carbonate) đã phản ứng với hydrochloric acid tạo calcium choloride .nước và khí carbonate dioxide cho biete cu=64;fe=56;ca=40;n=14;s=32;o=16;k=39;ci=35,5
Giúp mik vs ạ
Hóa Trị của S trong các hợp chất H2S , SO3 , S02
a) 2-4-6 b)2-6-4
C)1-3-2 b)2-6-6
a) Tính hóa trị của nguyên tố Fe trong hợp chất Fe2O3 biết O hóa trị 2
b)Tính hóa trị của nhóm nguyên tử (PO4) trong hợp chất Na3PO4 biết Na hóa trị 1
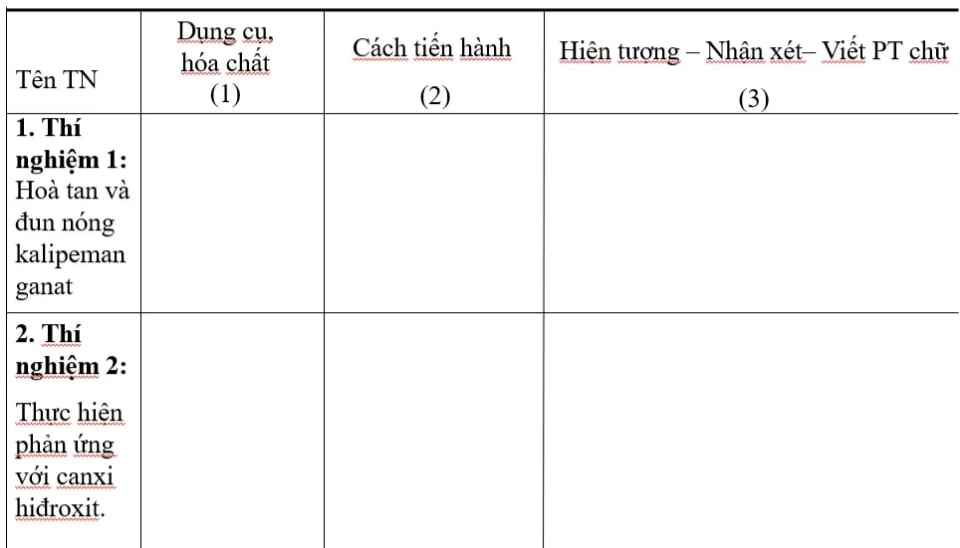
phương trình chứ khi hòa tan và đun nóng kali pemangnnat
Kali pemanganat \(--->\) Kali manganat + Mangan đioxit + Oxi