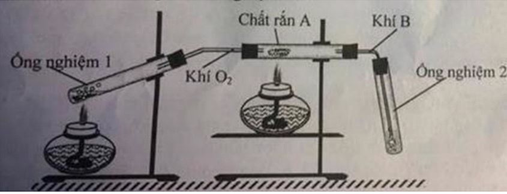
Nung X1 gam Cu với X2 gam O2 thì được chất rắn A1. Đun nóng A1 trong X3 gam H2SO4 98%. Sau khi hòa tan hết thu được dung dịch A2 và khí A3. Hấp thụ toàn bộ A3 bằng 200ml NaOH 0.15M tạo ra dung dịch chứa 2.3g muối. Khi cô cạn dung dịch A2 thu 30g tinh thể CuSO4.5H2O. Nếu cho A2 tác dụng dung dịch NaOH 1M thì để tạo ra chất kết tủa nhiều nhất phải dùng hết 300ml NaOH. Viết phương trình. Tính X1,X2,X3
\(2Cu+O_2\underrightarrow{t^o}2CuO\)
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
\(Cu+2H_2SO_{4\left(đ,n\right)}\rightarrow CuSO_4+SO_2+2H_2O\)
\(2NaOH+SO_2\rightarrow Na_2SO_3+H_2O\)
\(Na_2SO_3+SO_2+H_2O\rightarrow2NaHSO_3\)
\(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
nNaOH = 0,2.0,15 = 0,03 (mol)
Gọi \(\left\{{}\begin{matrix}n_{Na_2SO_3}=a\left(mol\right)\\n_{NaHSO_3}=b\left(mol\right)\end{matrix}\right.\)
Bảo toàn Na: 2a + b = 0,03
Và 126a + 104b = 2,3
=> a = 0,01 (mol); b = 0,01 (mol)
=> \(n_{SO_2}=0,02\left(mol\right)\)
\(n_{CuSO_4.5H_2O}=\dfrac{30}{250}=0,12\left(mol\right)\Rightarrow n_{CuSO_4}=0,12\left(mol\right)\)
nNaOH = 0,3.1 = 0,3 (mol)
PTHH: \(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
0,06---->0,03
\(2NaOH+CuSO_4\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
0,24<------0,12
=> A2 chứa \(\left\{{}\begin{matrix}CuSO_4:0,12\left(mol\right)\\H_2SO_4:0,03\left(mol\right)\end{matrix}\right.\)
Bảo toàn Cu: nCu(bd) = 0,12 (mol)
=> X1 = 0,12.64 = 7,68 (g)
Bảo toàn S: \(n_{H_2SO_4\left(bđ\right)}=0,12+0,03+0,02=0,17\left(mol\right)\)
=> \(m_{H_2SO_4}=0,17.98=16,66\left(g\right)\Rightarrow X_3=\dfrac{16,66.100}{98}=17\left(g\right)\)