- Gọi tỉ lệ khối lượng giữa hai đồng vị là x:
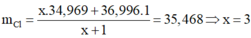
- Gọi tỉ lệ khối lượng giữa hai đồng vị là x:
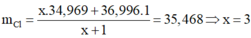
Khí clo có khối lượng nguyên tử bằng 35,468 u. Khí này là hỗn hợp đồng vị bền là 35Cl = 34,969 u và 37Cl = 36,996 u. Tỉ lệ khối lượng giữa hai đồng vị này trong khí clo là
A. 2,8
B. 3,0
C. 3,1
D. 3,2
Khí Clo là hỗn hợp của hai đồng vị bền là C 35 l = 34,969 u hàm lượng 75,4% và C 17 l = 36,966 u hàm lượng 24,6%.
Tính khối lượng nguyên tử của nguyên tố hoá học clo.
Khí clo trong tự nhiên có thể coi là hỗn hợp của hai đồng vị chính là C35 có khối lượng nguyên tử là 34,969 u và C37 có khối lượng nguyên tử là 36,996 u. Cho khối lượng nguyên tử của clo trong tự nhiên là 35,453. Xác định tí lệ % số hạt C35 trong tự nhiên.
A.78,5%
B. 79,5%
C. 68,5%
D. 70,5%
Ban đầu có một mẫu chất phóng xạ X nguyên chất, là đồng vị phân rã β- tạo thành chất Y bền, với chu kì bán rã 18 ngày. Sau thời gian t, trong mẫu chất tồn tại cả hai loại X và Y. Tỉ lệ khối lượng chất X so với khối lượng chất Y là 5/3. Coi tỉ số khối lượng giữa các nguyên tử bằng tỉ số số khối giữa chúng. Giá trị của t gần với giá trị nào sau đây nhất?
A. 10,0 ngày
B. 13,5 ngày
C. 11,6 ngày
D. 12,2 ngày
Ban đầu có một mẫu chất phóng xạ X nguyên chất, là đồng vị phân rã β- tạo thành chất Y bền, với chu kì bán rã 18 ngày. Sau thời gian t, trong mẫu chất tồn tại cả hai loại X và Y. Tỉ lệ khối lượng chất X so với khối lượng chất Y là 5/3. Coi tỉ số khối lượng giữa các nguyên tử bằng tỉ số số khối giữa chúng. Giá trị của t gần với giá trị nào sau đây nhất?
A. 10,0 ngày
B. 13,5 ngày
C. 11,6 ngày
D. 12,2 ngày
Người ta gọi khối lượng nguyên tử của một nguyên tố hoá học là khối lượng trung bình của một nguyên tử chất đó (tính theo đơn vị u). Vì trong một khối chất hoá học trong thiên nhiên bao giờ cũng chứa một số đồng vị của chất đó với những tỉ lệ xác định, nên khối lượng nguyên tử của mội nguyên tố hoá học không bao giờ là một số nguyên, trong khi đó, số khối của một hạt nhân bao giờ cũng là một số nguyên.
Neon thiên nhiên có ba thành phần là N 10 20 e ; N 10 21 e ; N 10 22 e và trong đó thành phần N 10 21 e chỉ chiếm 0,26 %, còn lại chủ yếu là hai thành phần kia. Khối lượng nguyên tử của neon là 20,179. Tính tỉ lệ phần trăm của các thành phần N 10 20 e ; N 10 22 e
Ban đầu, một lượng chất iôt có số nguyên tử của đồng vị bền I 53 127 và đồng vị phóng xạ I 53 131 lần lượt chiếm 60% và 40% tổng số nguyên tử trong khối chất. Biết chất phóng xạ I 53 127 phóng xạ β- và biến đổi thành xenon Xe 54 131 với chu kì bán rã là 9 ngày. Coi toàn bộ khí xenon và êlectron tạo thành đều bay ra khỏi khối chất iôt. Sau 9 ngày (kể từ lúc ban đầu), so với tổng số nguyên tử còn lại trong khối chất thì số nguyên tử đồng vị phóng xạ I 53 127 còn lại chiếm
A. 25%.
B. 20%.
C. 15%.
D. 30%.
Ban đầu, một lượng chất iôt có số nguyên tử của đồng vị bền I 53 127 và đồng vị phóng xạ I 53 131 lần lượt chiếm 60% và 40% tổng số nguyên tử trong khối chất. Biết chất phóng xạ I 53 131 phóng xạ β - và biến đổi thành xenon Xe 54 131 với chu kì bán rã là 9 ngày. Coi toàn bộ khí xenon và êlectron tạo thành đều bay ra khỏi khối chất iôt. Sau 9 ngày (kể từ lúc ban đầu), so với tổng số nguyên tử còn lại trong khối chất thì số nguyên tử đồng vị phóng xạ I 53 131 còn lại chiếm
A. 25%.
B. 20%.
C. 15%.
D. 30%.
Ban đầu, một lượng chất iôt có số nguyên tử của đồng vị bền 53 127 I và đồng vị phóng xạ 53 131 I lần lượt chiếm 60% và 40% tổng số nguyên tử trong khối chất. Biết chất phóng xạ 53 127 I phóng xạ β- và biến đổi thành xenon 54 131 X e với chu kì bán rã là 9 ngày. Coi toàn bộ khí xenon và êlectron tạo thành đều bay ra khỏi khối chất iôt. Sau 9 ngày (kể từ lúc ban đầu), so với tổng số nguyên tử còn lại trong khối chất thì số nguyên tử đồng vị phóng xạ 53 131 I còn lại chiếm
A. 25%
B. 20%
C. 15%
D. 30%