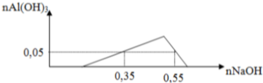
Dung dịch Y gồm: a mol Al3+, b mol Cl-, 0,15 mol H+ và 0,03 mol SO42-. Cho 180ml dung dịch Z gồm NaOH 1,2M và Ba(OH)2 0,1M vào dung dịch Y, sau khi các phản ứng xảy ra hoàn toàn, thu được 5,598 gam kết tủa. Giá trị của a, b lần lượt là:
A. 0,030 và 0,180
B. 0,030 và 0,018
C. 0,180 và 0,030
D. 0,018 và 0,144
Chọn A
Bảo toàn điện tích : 3a + 0,15 = b + 0,03.2 => 3a + 0,09= b mol
Z : nOH = 0,252 mol ; nBa2+ = 0,018 mol < nSO4
=> kết tủa gồm Al(OH)3 và BaSO4 => nAl(OH)3 = 0,018 mol
Giả sử có hiện tượng hòa tan kết tủa => nAl(OH)3 = 4nAl3+ - (nOH- - nH+)
=> nAl3+ = a = 0,03 mol => b = 0,18 mol