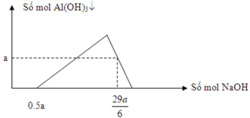
Cho m gam hỗn hợp gồm một kim loại kiềm M và Al vào nước dư thu được dung dịch A; 0,4687m gam chất rắn không tan và 7,2128 lít H2 (đktc). Cho từ từ dung dịch HCl có số mol lớn hơn 0,18 mol vào dung dịch A, ngoài kết tủa còn thu được dung dịch B. Cô cạn dung dịch B thu được 11,9945gam chất rắn khan. Giá trị m gần nhất với giá trị nào sau đây?
A. 18gam
B. 17gam
C. 15gam
D. 14gam
Đáp án C
M + H2O -> MOH + ½ H2
MOH + Al + H2O -> MAlO2 + 3/2H2
Do còn chất rắn không tan => Al dư
=> nM = nMAlO2 = 1/2nH2 = 0,161 mol
MAlO2 + HCl -> MCl + Al(OH)3
,nHCl = x > 0,18 mol => nAl(OH)3 = 1/3 (4nAlO2 – nH+) = (0,644 – x)/3
Và nAlCl3 = 1/3(nHCl – nAlO2) = (x – 0,161)/3 mol ; nMCl = nMAlO2 = 0,161 mol
=> mAlCl3 + mMCl = 11,9945g = 44,5(x – 0,161) + 0,161.(M + 35,5)
=> 44,5x + 0,161M = 13,4435
Do x > 0,18 => M < 33,75 => M là Na ( Li không tan nhiều trong nước)
=> nNa = 0,161 và nAl pứ = 0,161
=> m – 0,4687m = 0,161.23 + 0,161.27 => m = 15,15g
=>C