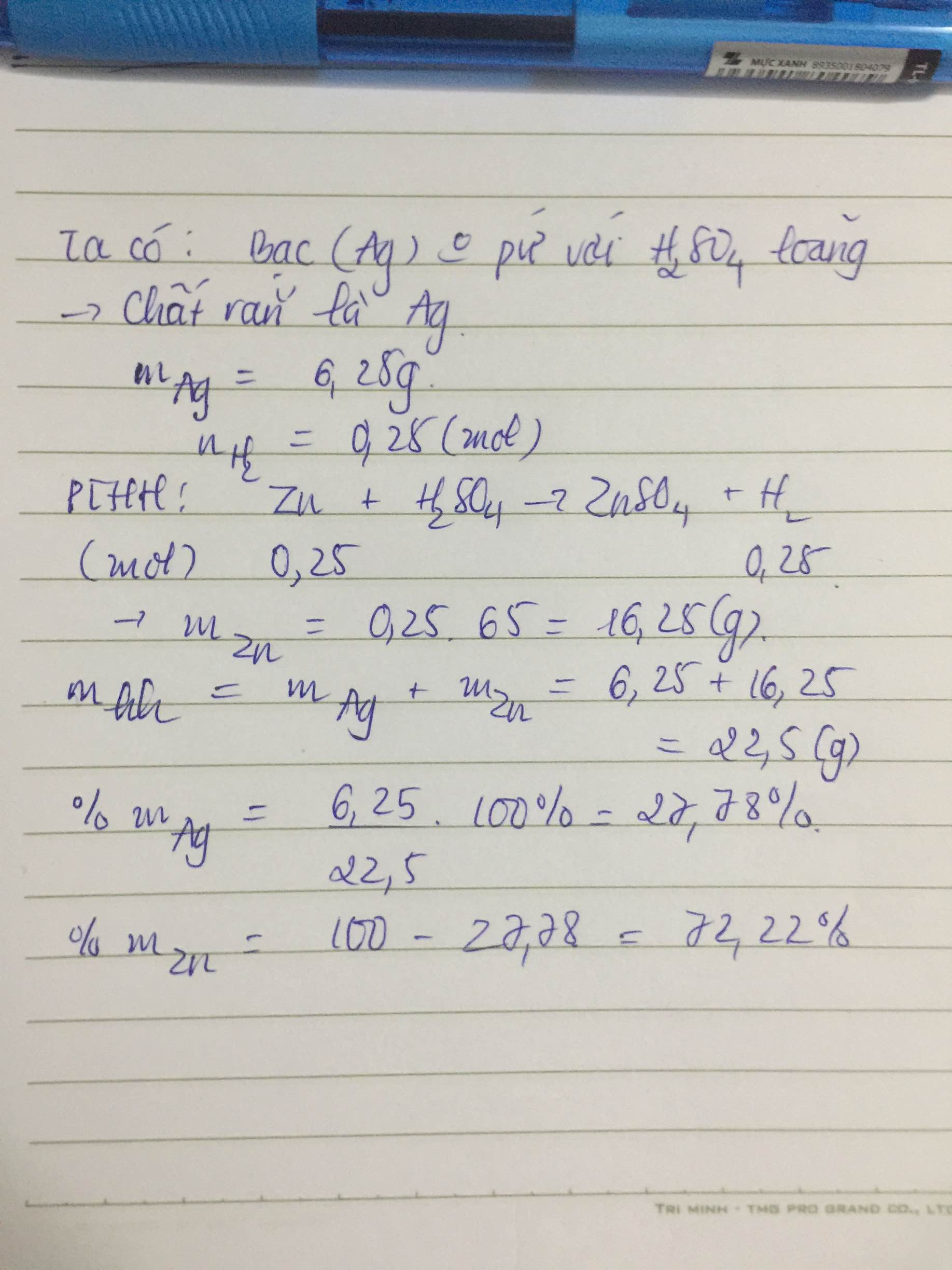\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
0,25 0,25 (Mol)
\(\Rightarrow n_{Zn}=0,25\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,25.65=16,25\left(g\right)\)
Chấ rắn không tan là Ag
\(\Rightarrow m_{Ag}=6,25\left(g\right)\)
\(\%m_{Zn}=\dfrac{16,25}{16,25+6,25}.100\%\approx72,22\%\)
\(\%m_{Ag}=\dfrac{6,25}{6,25+16,25}.100\%\approx27,78\%\)
Vì bạc không tác dụng với dung dịch H2SO4 nên chất rắn không tan là Bạc và ta chỉ có phương trình phản ứng của Kẽm:
Zn + H2SO4 → Zn2SO4 + H2
mol 0,25 0,25
Mol H2= V/22,4= 5,6/22,4= 0,25 (mol)
mZn= n.M = 0,25. 65=16,25(g)
➞ mHỗn hợp= mZn+mAg= 16,25+6,25= 22,5(g)
⇒ %mZn= (16,25/22,5).100%= 72,2%
%mAg= 100%-72,2%= 27,8%
Bài giải của mình nếu có sai sót thì mong các bạn bình luận góp ý để giúp mình hoàn thiện hơn trong những lần sau, còn nếu đúng thì bài làm của mình bạn kham khảo nha.