Các câu hỏi tương tự
cân bằng phản ứng oxi hóa - khử theo phương pháp thăng bằng electron 1H2SO4+H2S->S+H2O
2 s+HNO3->H2SO4+NO
3I2+HNO3->HIO3+NO+H2O
4 NH3+O2->No+H2O
5 C+HNO3->NO2+CO2+H2O
6H2SO4+HI->I2+H2S+H2O
7P+KClO3->P2O5+KCl
8 NH3+CuO->Cu+H2O+N2
Trong những phản ứng sau đây, phản ứng nào là phản ứng oxi hóa – khử? Giải thích. a) SO3 + H2O → H2SO4 b) CaCO3 + 2HCl → CaCl2 + CO2 + H2O c) C + H2O → CO + H2 d) CO2 + Ca(OH)2 → CaCO3 + H2O e) Ca + 2H2O → Ca(OH)2 + H2 f) 2KMnO4 → K2MnO4 + MnO2 + O2
Đọc tiếp
Trong những phản ứng sau đây, phản ứng nào là phản ứng oxi hóa – khử? Giải thích.
a) SO3 + H2O → H2SO4
b) CaCO3 + 2HCl → CaCl2 + CO2 + H2O
c) C + H2O → CO + H2
d) CO2 + Ca(OH)2 → CaCO3 + H2O
e) Ca + 2H2O → Ca(OH)2 + H2
f) 2KMnO4 → K2MnO4 + MnO2 + O2
e) Tính nhiệt tạo thành tiêu chuẩn (nhiệt sinh chuẩn) của khí CO từ các dữ kiện thực nghiệm
dưới đây.
C (s) + O2 (g) → CO2 (g) ΔrH298
o = − 94,05 𝑘𝑐𝑎𝑙
2CO (g) + O2 (g) → 2CO2 (g) ΔrH298
o = − 135,28 𝑘𝑐𝑎𝑙
Trong các phản ứng hoá hợp dưới đây, phản ứng nào là phản ứng oxi hoá-khử A. 2SO2 + O2 2SO3. B. P2O5 + 3H2O 2H3PO4. C. CaCO3 + H2O + CO2 Ca(HCO3)2 D. BaO + H2O Ba(OH)2.
Đọc tiếp
Trong các phản ứng hoá hợp dưới đây, phản ứng nào là phản ứng oxi hoá-khử
A. 2SO2 + O2 ![]() 2SO3.
2SO3.
B. P2O5 + 3H2O ![]() 2H3PO4.
2H3PO4.
C. CaCO3 + H2O + CO2 ![]() Ca(HCO3)2
Ca(HCO3)2
D. BaO + H2O ![]() Ba(OH)2.
Ba(OH)2.
Cho các cân bằng:
H
2
(
k
)
+
I
2
(
k
)
⇌
2
HI
(
1
)
2
NO
(
k
)
+
O
2
⇄
2
NO
2
...
Đọc tiếp
Cho các cân bằng:
H 2 ( k ) + I 2 ( k ) ⇌ 2 HI ( 1 )
2 NO ( k ) + O 2 ⇄ 2 NO 2 ( 2 )
CO ( k ) + Cl 2 ( k ) ⇄ COCl 2 ( 3 )
N 2 ( k ) + 3 H 2 ( k ) ⇄ 2 NH 3 ( k ) ( 4 )
CaCO 3 ( r ) ⇄ CaO ( r ) + CO 2 ( k ) ( 5 )
CO ( k ) + H 2 O ( k ) ⇄ CO 2 ( k ) + H 2 ( k ) ( 6 )
Các cân bằng chuyển dịch theo chiều thuận khi tăng áp suất là:
A.1,3
B.3,4,5
C.1,2,3
D.2,3,4
Cho các phản ứng hóa học sau:(1)
CaCO
3
→
t
∘
CaO
+
CO
2
(2)
2
KClO
3
...
Đọc tiếp
Cho các phản ứng hóa học sau:
(1) CaCO 3 → t ∘ CaO + CO 2
(2) 2 KClO 3 → t ∘ 2 KCl + 3 O 2
(3) 2 NaNO 3 → t ∘ 2 NaNO 2 + O 2
(4) 2 Al ( OH ) 3 → t ∘ Al 2 O 3 + 3 H 2 O
(5) 2 NaHCO 3 → t ∘ Na 2 CO 3 + H 2 O + CO 2
Phản ứng oxi hóa – khử là
A. (1), (4).
B. (2), (3).
C. (3), (4).
D. (4), (5).
Cho phản ứng sau: A. 2HgO 2Hg + O2.
QUẢNG CÁO
B. CaCO3 CaO + CO2. C. 2Al(OH)3 Al2O3 + 3H2O. D. 2NaHCO3 Na2CO3 + CO2 + H2O. Phản ứng nào là phản ứng oxi hóa – khử.
Đọc tiếp
Cho phản ứng sau:
A. 2HgO 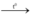 2Hg + O2.
2Hg + O2.
B. CaCO3 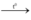 CaO + CO2.
CaO + CO2.
C. 2Al(OH)3 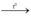 Al2O3 + 3H2O.
Al2O3 + 3H2O.
D. 2NaHCO3 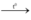 Na2CO3 + CO2 + H2O.
Na2CO3 + CO2 + H2O.
Phản ứng nào là phản ứng oxi hóa – khử.
ABài 1.Cân bằng phản ứng oxi hóa khử theo phương pháp thăng bằng electron :
1.H2S + SO2 = S + H2O
2.H2S + HClO = HCl + H2SO4
3.S + H2SO4 = SO2 + H2O
4.Fe3O4 + CO = Fe + CO2
5.P + H2SO4 = H3PO4 + SO2 + H2O
6. C + H2SO4 = CO2 + SO2 +H2O
Cho các cân bằng hóa học sau:(1)
2
S
O
2
(
k
)
+
O
2
(
k
)
⇌
2
S
O
3
(k)(2)
N
2
(
k
)
+
3
H
2
⇌
2
N
H
3
(k)(3)...
Đọc tiếp
Cho các cân bằng hóa học sau:
(1) 2 S O 2 ( k ) + O 2 ( k ) ⇌ 2 S O 3 (k)
(2) N 2 ( k ) + 3 H 2 ⇌ 2 N H 3 (k)
(3) C O 2 ( k ) + H 2 ( k ) ⇌ C O ( k ) + H 2 O (k)
(4) 2 H I ( k ) ⇌ H 2 ( k ) + I 2 (k)
Khi thay đổi áp suất, các cân bằng hóa học đều không bị chuyển dịch là
A. (1) và (3)
B. (2) và (4)
C. (1) và (2)
D. (3) và (4)






