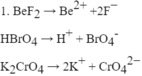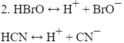Các câu hỏi tương tự
Câu2: Viết phương trình điện li của những chất sau: a) Các chất điện li mạnh: Ba(NO3)2, HNO3, KOH. b) chất điện li yếu: HCLO, HNO2, H2CO3
Dung dịch axit mạnh một nấc X nồng độ 0,010 mol/l có pH = 2 và dung dịch bazơ mạnh một nấc Y nồng độ 0,010 mol/l có pH = 12. Vậy:
A. X và Y là các chất điện li mạnh.
B. X và Y là các chất điện li yếu.
C. X là chất điện li mạnh, Y là chất điện li yếu.
D. X là chất điện li yếu, Y là chất điện li mạnh.
Viết phương trình điện li của những chất sau:
Các chất điện li mạnh: Ba(NO3)2 0.10 M; HNO3 0,020 M; KOH 0,010 M. Tính nồng độ mol của từng ion trong dung dịch.
Cho các phát biểu sau: (a) Chất điện li bao gồm axit, bazơ, muối (b) Dãy các chất: HF, NaF, NaOH đều là chất điện li mạnh (c) Dãy các chất: C2H5OH, C6H12O6, CH3CHO là các chất điện li yếu (d) Những chất khi tan trong nước cho dung dịch dẫn điện được gọi là những chất điện li Số phát biểu đúng là: A. 2 B. 3 C. 4 D. 1
Đọc tiếp
Cho các phát biểu sau:
(a) Chất điện li bao gồm axit, bazơ, muối
(b) Dãy các chất: HF, NaF, NaOH đều là chất điện li mạnh
(c) Dãy các chất: C2H5OH, C6H12O6, CH3CHO là các chất điện li yếu
(d) Những chất khi tan trong nước cho dung dịch dẫn điện được gọi là những chất điện li
Số phát biểu đúng là:
A. 2
B. 3
C. 4
D. 1
Viết phương trình điện li của các chất sau: K2S, Na2HPO4, NaH2PO4, Pb(OH)2, HBrO, HF, HClO4.
Lấy 5 axit bất kì, mỗi axit khối lượng 10g( gồm 3 chất điện li mạnh, 2 chất điện li yếu hoà tan vào 100g nước) a) Viết pt phân li các chất trên b)?Tính số mol các ion biết các chất điện li chủ yếu chỉ phân li 10% c) Trong bài, xác định chất nào dẫn điện tốt nhất, dẫn điện kém nhất, vì sao?
Viết phương trình điện li của những chất sau: Các chất điện li yếu HClO; HNO2.
Sự điện li, chất điện li là gì? Những loại chất nào là chất điện li? Thế nào là chất điện li mạnh, chất điện li yếu? Lấy thí dụ và viết phương trình điện li của chúng?
Viết phương trình điện li của axit yếu
C
H
3
C
O
O
H
trong dung dịch. Nếu hoà tan ít tinh thể chất điện li mạnh
C
H
3
C
O
O
N
a
vào dung dịch axit trên thì nồng độ
H
+
tăng hay giảm ? Giải thích dựa vào nguyên lí chuyển dịch cân bằng Lơ Satơliê.
Đọc tiếp
Viết phương trình điện li của axit yếu C H 3 C O O H trong dung dịch. Nếu hoà tan ít tinh thể chất điện li mạnh C H 3 C O O N a vào dung dịch axit trên thì nồng độ H + tăng hay giảm ? Giải thích dựa vào nguyên lí chuyển dịch cân bằng Lơ Satơliê.