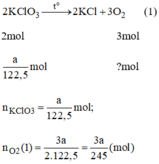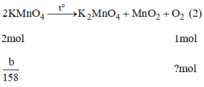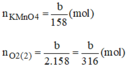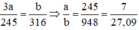Các câu hỏi tương tự
Phương trình nhiệt phân theo sơ đồ sau 2KMnO 4 K 2 MnO 4 + MnO 2 + O 2 . a) Tính thể tích khí oxi (đktc) thu được khi nhiệt phân 63,2 g KMnO 4 . b) Tính khối lượng Al 2 O 3 được tạo thành khi cho lượng khí oxi sinh ra ở trên tác dụng hết với Al.
Đọc tiếp
Phương trình nhiệt phân theo sơ đồ sau
2KMnO 4 K 2 MnO 4 + MnO 2 + O 2 .
a) Tính thể tích khí oxi (đktc) thu được khi nhiệt phân 63,2 g KMnO 4 .
b) Tính khối lượng Al 2 O 3 được tạo thành khi cho lượng khí oxi sinh ra ở trên tác dụng hết với Al.
Nung a gam KClO3 và b gam KMnO4 thì thu được cùng một lượng oxi. Tính tỉ lệ a/b.
Nung m(g) hỗn hợp A gồm KMnO4 và KClO3 thu đc chất rắn B và khí oxi, lúc đó KClO3 bị phân hủy hoàn toàn còn KMnO4 k bị phân hủy hoàn toàn. Trong B có 0,894 gam KCl chiếm 8,132% khối lượng. Trộn lượng oxi trên với không khí theo tỉ lệ thể tích 1:3 trong 1 bình kín thu đc hỗn hợp khí X. Cho vào bình 0,528 gam cacbon rồi đốt cháy hết cacbon thu đc hỗn hợp khí Y gồm 3 khí trong đó CO2 chiếm 22,92% thể tích.Tính m?(Coi không khí gồm 20% thể tích là oxi còn lại là nito)
Đọc tiếp
Nung m(g) hỗn hợp A gồm KMnO4 và KClO3 thu đc chất rắn B và khí oxi, lúc đó KClO3 bị phân hủy hoàn toàn còn KMnO4 k bị phân hủy hoàn toàn. Trong B có 0,894 gam KCl chiếm 8,132% khối lượng. Trộn lượng oxi trên với không khí theo tỉ lệ thể tích 1:3 trong 1 bình kín thu đc hỗn hợp khí X. Cho vào bình 0,528 gam cacbon rồi đốt cháy hết cacbon thu đc hỗn hợp khí Y gồm 3 khí trong đó CO2 chiếm 22,92% thể tích.Tính m?(Coi không khí gồm 20% thể tích là oxi còn lại là nito)
nung a (mol) KClO3 và b (mol) KMnO4 thu được cùng lượng ôxi. Tính tỉ lệ a/b
giúp mình với
a. Nung nóng 12,25(g) KClO3 trong ống nghiệm có mặt MnO2 làm chất xúc tác. Hãy tính thể tích oxi(ĐKTC) thu được. (Cho K 39 ; Cl 35,5 ; O 16)b. Cho 33,6 gam Sắt vào bình chứa dung dịch axit clohđric. Tính khối lượng các sản phẩm tạo thành? (Cho Fe 56 ; H 1 ; Cl 35,5 ; O 16)
Đọc tiếp
a. Nung nóng 12,25(g) KClO3 trong ống nghiệm có mặt MnO2 làm chất xúc tác. Hãy tính thể tích oxi(ĐKTC) thu được. (Cho K = 39 ; Cl = 35,5 ; O= 16)
b. Cho 33,6 gam Sắt vào bình chứa dung dịch axit clohđric. Tính khối lượng các sản phẩm tạo thành? (Cho Fe = 56 ; H = 1 ; Cl = 35,5 ; O= 16)
Câu 8: Dẫn 2,24 l khí H2 qua ống sứ nung nóng đựng 4 gam CuO. Khối lượng Cu thu được là.A. 3,2 g. B. 0,32 g. C. 1,6 g. D. 2,4 g.Câu 9: Thành phần của không khí gồm những khí gì?A. 20% khí oxi, 79% khí nitơ, 1% các khí khác. B. 21% khí nitơ, 78% khí oxi, 1% các khí khác.C. 1% khí nitơ, 78% khí oxi, 21% các khí khác. D. 21% khí oxi, 78% khí nitơ, 1% các khí khác.Câu 10: Dung dich Axit làm giấy quỳ tím chuyển thành màu gì?A. Đỏ. B. Xanh. C. Vàng. D. Không đổi màu.Câu 11. Muối nào sao đây là muối ax...
Đọc tiếp
Câu 8: Dẫn 2,24 l khí H2 qua ống sứ nung nóng đựng 4 gam CuO. Khối lượng Cu thu được là.
A. 3,2 g. B. 0,32 g. C. 1,6 g. D. 2,4 g.
Câu 9: Thành phần của không khí gồm những khí gì?
A. 20% khí oxi, 79% khí nitơ, 1% các khí khác. B. 21% khí nitơ, 78% khí oxi, 1% các khí khác.
C. 1% khí nitơ, 78% khí oxi, 21% các khí khác. D. 21% khí oxi, 78% khí nitơ, 1% các khí khác.
Câu 10: Dung dich Axit làm giấy quỳ tím chuyển thành màu gì?
A. Đỏ. B. Xanh. C. Vàng. D. Không đổi màu.
Câu 11. Muối nào sao đây là muối axit.
A. CaCO3 B. Ca(HCO3)2 C. CaCl2 D. CaSO4
Câu 12. Bazơ nào sau đây tan được trong nước
A. Fe(OH)3 B. Cu(OH)2 C. NaOH D. Al(OH)3
Câu 13. Muối là hợp chất trong thành phần phân tử có:
A. Nguyên tử kim loại liên kết với nhóm hiđrôxít (–OH). B. Nguyên tử kim loại liên kết với nguyên tử oxi.
C. Nguyên tử kim loại liên kết với gốc axít. D. Nguyên tử kim loại liên kết với nguyên tử Clo.
Câu 14. Nồng độ % của dung dịch là:
A. Số gam chất tan có trong 100g dung dịch. B. Số gam chất tan có trong 100g dung môi.
C. Số gam chất tan có trong 1lít dung dịch.
D. Số gam chất tan tan trong 100 gam dung môi để tạo thành dung dịch bão hoà.
Câu 15. Biết độ tan của KCl ở 30oC là 37. Khối lượng nước bay hơi ở 30oC từ 200g dung dịch KCl 20% để
được dung dịch bão hòa là:
A. 52 gam. B. 148 gam. C. 48 gam D. 152 gam
Câu 16. Khử 12g sắt (III) oxit bằng khí hiđro ở nhiệt độ cao. Thể tích khí hiđro(ở đktc) cần dùng là:
A. 5,04 lít B. 7,56 lít C. 10,08 lít D. 8,2 lít
Câu 17. Có thể thu khí hidro bằng phương pháp đẩy nước và đẩy không khí vì hidro:
A. Là chất khí B. Nhẹ hơn không khí và ít tan trong nước
C. Nặng hơn không khí D. Có nhiệt độ hóa lỏng thấp
Câu 18. Số mol Na2CO3 có trong 100 ml dung dịch 2M là:
A. 0,1 mol B. 0,15 mol C. 0,25 mol D. 0,2 mol
Câu 19. Một hợp chất hữu cơ A có chứa: 54,5%C, 9,1%H còn lại là oxi và MA = 88 đvC. Vậy A là
A. C2H4O2. B. C2H6O. C. C3H6O. D. C4H8O2.
Câu 20. Số gam NaCl trong 50 gam dung dịch NaCl 40% là
A. 40 gam B. 30 gam C. 20 gam D. 50 gam
bài 3:Nung hoàn toàn 2,45 gam một hợp chất A thu được một hợp chất B chứa 52,35% K; 47,65% Cl về khối lượng; đồng thời thấy thoát ra 672 ml khí O (ở đktc)
a) Hỏi trong A có những nguyên tố nào? Giải thích?
b) Tìm công thức hóa học của A biết khối lượng mol của A bằng 122,5
Câu 18. Hợp chất X được tạo bảo 2 nguyên tố là N là O. Biết tỉ lệ về khối lượng của N với O là 7: 20. CTHH của X là A. NO. B. N2O. C. NO2. D. N2O5.Câu 19. Hợp chất X được tạo bảo 2 nguyên tố là Fe là O. Biết tỉ lệ về khối lượng của Fe với O là 7:3. CTHH của X là A. FeO. B. Fe2O3. C. Fe3O4. D. Fe3O7.Câu 20. Một hợp chất hóa học được tạo bởi 2 nguyên tố Na và Cl có thành phần % khối lượng Na là 39,32%, còn lại là thành phần % khối lượng của Cl. Biết khối lượng mol của hợp chất là 58,5. Công thức h...
Đọc tiếp
Câu 18. Hợp chất X được tạo bảo 2 nguyên tố là N là O. Biết tỉ lệ về khối lượng của N với O là 7: 20. CTHH của X là
A. NO. B. N2O. C. NO2. D. N2O5.
Câu 19. Hợp chất X được tạo bảo 2 nguyên tố là Fe là O. Biết tỉ lệ về khối lượng của Fe với O là 7:3. CTHH của X là
A. FeO. B. Fe2O3. C. Fe3O4. D. Fe3O7.
Câu 20. Một hợp chất hóa học được tạo bởi 2 nguyên tố Na và Cl có thành phần % khối lượng Na là 39,32%, còn lại là thành phần % khối lượng của Cl. Biết khối lượng mol của hợp chất là 58,5. Công thức hóa học của hợp chất đó là
A. NaCl2. B. NaCl3. C. NaCl. D. Na2Cl.
Câu 21. Phản ứng nào sau đây là phản ứng hóa hợp?
A. 2Cu + O2 → 2CuO. B. CaCO3 → CaO + CO2.
C. 2K + 2H2O → 2KOH + H2. D. 2KClO3 → 2KCl + 3O2.
Câu 22. Phản ứng nào sau đây là phản ứng có sự oxi hóa?
A. 2Cu + O2 → 2CuO. B. CaCO3 → CaO + CO2.
C. 2K + 2H2O → 2KOH + H2. D. 2KClO3 → 2KCl + 3O2.
Câu 23. Phản ứng nào sau đây là phản ứng điều chế khí O2?
A. 2Cu + O2 → 2CuO. B. CaCO3 + HCl → CaCl2 + CO2 + H2O.
C. 2K + 2H2O → 2KOH + H2. D. 2KClO3 → 2KCl + 3O2.
Câu 24. Phản ứng nào sau đây là phản ứng phân hủy?
A. 2Cu + O2 → 2CuO. B. 2KClO3 → 2KCl + 3O2.
C. 2K + 2H2O → 2KOH + H2. D. CO2 + CaO → CaCO3.
giúp mik vs ạ
cho 3.24 g Al tác dụng với oxi vừa đủ th được Al2O3
a. tính Vo2 =?b. tính m Al2O3=? c. trong Vkk cần dùng ( biết Vo2= 21% Vkk) d. tính khối lượng KMNO4 cần dùng để điều chế lượng oxit ở câu a( Al = 27 , O = 16 , K = 39 , MN = 55 )