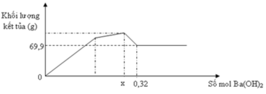
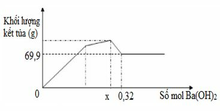
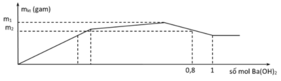
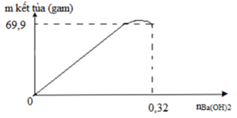
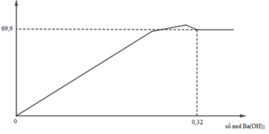
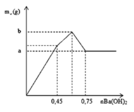
Tại n Ba ( OH ) 2 = 0 , 32 mol thì lượng kết tủa ổn định sau khi đã giảm
→ lúc này OH hòa tan hết Al(OH)3
Lượng kết tủa chỉ có BaSO4: 0,3 mol
Ta có: 4OH−+Al3+→AlO2−+2H2O
→ n Al 3 + = 0 , 16 mol
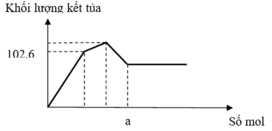
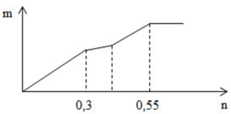
Tại vị trí gấp khúc đầu tiên: đồ thì tăng chậm hơn giai đoạn đầu
→ chứng tỏ lúc này có sự hòa tan Al(OH)3 nhưng lượng kết tủa tăng vì đang tạo thêm BaSO4
Giai đoạn đầu tăng đều vì có sự tăng đồng thời Al(OH)3 và BaSO4
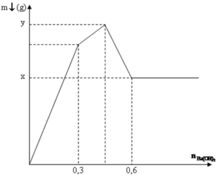
Đến n Ba ( OH ) 2 = x thì lượng BaSO4 tối đa và chỉ còn sự tan Al(OH)3dẫn đến đồ thị đi xuống
→ x = n BaSO 4 = 0 , 3 mol
Đáp án C